ALSARKARE
ETEX
40 mg
Antihipertensivo.
Composición.
ALSARKARE Comprimidos Recubiertos 40 mg contiene: Valsartán 40mg. Excipientes: Lactosa monohidratada, celulosa microcristalina, almidón de maíz, crospovidona, povidona, Dióxido de Silicio coloidal anhidro, estearato de magnesio, Instacoat universal (ICG-U-10281 amarillo [Hipromelosa, Macrogol, Dióxido de Titanio, Talco, Óxido de Hierro Amarillo]) c.s.
Farmacología.
Farmacodinamia. Grupo farmacoterapéutico: Antagonistas de la angiotensina II, Código ATC. C09CA03. Mecanismo de acción: Efectos farmacodinámicos: Valsartán es un potente antagonista oral, activo y específico de los receptores de la angiotensina II (Ang II). Actúa selectivamente sobre el subtipo de receptor de AT1, que es responsable de las acciones conocidas de la angiotensina II. El aumento en las concentraciones plasmáticas de Ang II, tras un bloqueo del receptor de AT1 con Valsartán, podría estimular al receptor de AT2 no bloqueado, lo cual parece contrarrestar el efecto del receptor de AT1. Valsartán no exhibe ninguna actividad agonista parcial en el receptor de AT1, y tiene mucho mayor (aproximadamente 20.000 veces) afinidad por el receptor de AT1 que por el receptor de AT2. No se sabe si Valsartán se une o bloquea otros receptores hormonales o canales iónicos con importancia conocida en la regulación cardiovascular. Valsartán no inhibe la ECA (también conocida como cininasa II), que transforma la Ang I en Ang II y degrada la bradiquinina. Como no hay un efecto en la ECA, ni tampoco potenciación de bradiquinina o sustancia P, es poco probable que los antagonistas de la angiotensina II se asocien con tos. En estudios clínicos en los que se comparó Valsartán con un inhibidor de la ECA, la incidencia de tos seca fue significativamente menor (P < 0,05) en los pacientes tratados con Valsartán que en aquellos que recibieron un inhibidor de la ECA (2,6% frente a 7,9%, respectivamente). En un estudio clínico de pacientes con antecedentes de tos seca durante la terapia con algún inhibidor de la ECA, 19,5% de los sujetos del estudio que recibieron Valsartán y 19,0% de aquellos que recibieron algún diurético tiazídico experimentaron tos, en comparación con 68,5% de los sujetos tratados con algún inhibidor de la ECA (P < 0,05). Farmacocinética: Absorción: Tras la administración oral de Valsartán en monoterapia, las concentraciones plasmáticas máximas de Valsartán se alcanzan en un plazo de 2-4 horas con la formulación en comprimidos y de 1-2 horas con la formulación en solución. La biodisponibilidad absoluta media es de 23% y 39% con las formulaciones en tabletas y solución, respectivamente. Los alimentos disminuyen el nivel de exposición (medido por el ABC) a Valsartán en aproximadamente 40%, y su concentración plasmática máxima (Cmáx) en aproximadamente 50%, aunque a partir de aproximadamente 8 h después de su administración, las concentraciones plasmáticas de Valsartán son similares en los grupos postprandiales y en ayunas. Sin embargo, esta reducción en el ABC no se ve acompañada de una reducción clínicamente significativa en el efecto terapéutico, por lo cual Valsartán puede administrarse con o sin alimentos. Distribución: El volumen de distribución en estado estable de Valsartán tras su administración intravenosa es de aproximadamente 17 litros, lo cual indica que Valsartán no se distribuye ampliamente en los tejidos. Valsartán tiene un alto grado de unión a proteínas séricas (94-97%), principalmente a la albúmina sérica. Metabolismo: Valsartán no experimenta un alto grado de biotransformación, ya que sólo alrededor de 20% de la dosis se recupera en forma de metabolitos. Se ha identificado un metabolito hidroxi en el plasma a concentraciones bajas (menos de 10% del ABC de Valsartán). Este metabolito es farmacológicamente inactivo. Eliminación: Valsartán muestra una cinética de descomposición multiexponencial (t½a < 1 h y t½b aproximadamente 9 h). Valsartán se elimina principalmente mediante excreción biliar en las heces (aproximadamente 83% de la dosis) y por vía renal en la orina (aproximadamente 13% de la dosis), principalmente como fármaco inalterado. Tras su administración intravenosa, la depuración plasmática de Valsartán es de aproximadamente 2 L/h y su depuración renal es de 0,62 L/h (aproximadamente 30% de la depuración total). La vida media de Valsartán es de 6 horas. Poblaciones especiales de pacientes: Niños: En un estudio realizado en 26 pacientes pediátricos hipertensos (de 1 a 16 años de edad) que recibieron una dosis única de una suspensión de Valsartán (media: 0,9 a 2 mg/kg, con una dosis máxima de 80 mg), la depuración (litros/h/kg) de Valsartán fue similar en todo el rango de edad de 1 a 16 años, y a la de los adultos que recibieron la misma formulación. Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 mL/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Personas de edad avanzada: En algunos sujetos de edad avanzada, se observó una exposición sistémica a Valsartán algo mayor que en los sujetos jóvenes; sin embargo, no se ha demostrado que esto tenga alguna significancia clínica. Insuficiencia renal: Como era de esperarse de un compuesto cuya depuración renal representa sólo el 30% de la depuración plasmática total, no se observó correlación alguna entre la función renal y la exposición sistémica a Valsartán. Por lo tanto, no es necesario ajustar la dosis en pacientes con insuficiencia renal (depuración de creatinina > 10 mL/min). Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 mL/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. Valsartán tiene un alto grado de unión a proteínas plasmáticas, por lo cual es poco probable que se elimine a través de diálisis. Insuficiencia hepática: Aproximadamente 70% de la dosis absorbida se elimina en la bilis, fundamentalmente en forma inalterada. Valsartán no experimenta ninguna biotransformación notable. Se observó una duplicación de la exposición (ABC) en pacientes con insuficiencia hepática leve a moderada, en comparación con sujetos sanos. Sin embargo, no se observó correlación alguna entre la concentración plasmática de Valsartán y el grado de disfunción hepática. No se ha estudiado Valsartán en pacientes con disfunción hepática grave. Otras características de los pacientes: Pacientes con insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, el tiempo promedio para alcanzar la concentración máxima y la vida media de eliminación de Valsartán son similares a los observados en voluntarios sanos. Los valores de ABC y Cmáx de Valsartán casi son proporcionales al aumentar la dosis en el rango clínico de dosificación (40 a 160 mg administrados dos veces al día). El factor de acumulación promedio es de aproximadamente 1,7. La depuración aparente de Valsartán tras su administración oral es de aproximadamente 4,5 L/h. La edad no afecta la depuración aparente en pacientes con insuficiencia cardiaca. Información no clínica: Los datos pre-clínicos no revelaron riesgos especiales para los seres humanos, según los estudios convencionales de seguridad farmacológica, toxicidad de dosis repetidas, genotoxicidad y potencial carcinogénico. En ratas, la administración de dosis tóxicas para las madres (600 mg/kg/día) durante los últimos días de la gestación y la lactancia condujo a una menor supervivencia, un menor aumento en el peso y un retraso en el desarrollo (desprendimiento del pabellón auricular y apertura del canal auditivo) en la descendencia. Estas dosis administradas en ratas (600 mg/kg/día) son aproximadamente 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En estudios pre-clínicos de seguridad, las dosis elevadas de Valsartán (200 a 600 mg/kg de peso corporal) administradas en ratas ocasionaron una disminución de los parámetros de glóbulos rojos (eritrocitos, hemoglobina, hematocrito), así como indicios de cambios en la hemodinamia renal (ligero aumento en las concentraciones plasmáticas de urea, e hiperplasia tubular renal y basofilia en machos). Estas dosis administradas en ratas (200 y 600 mg/kg/día) son aproximadamente 6 y 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En monos tití que recibieron dosis similares, los cambios fueron semejantes aunque más graves, sobre todo en los riñones, donde los cambios evolucionaron a una nefropatía con aumentos en las concentraciones de urea y creatinina. En ambas especies, también se observó hipertrofia de las células renales yuxtaglomerulares. Se consideró que todos los cambios fueron ocasionados por la acción farmacológica de Valsartán, la cual produce hipotensión prolongada, especialmente en monos tití. En lo que respecta a las dosis terapéuticas de Valsartán en seres humanos, la hipertrofia de las células renales yuxtaglomerulares no parece tener relevancia alguna. Población pediátrica: La administración oral diaria de Valsartán a ratas recién nacidas/jóvenes (entre los 7 y 70 días de vida), a dosis tan bajas como 1 mg/kg/día (aproximadamente 10-35% de la dosis máxima recomendada para uso pediátrico de 4 mg/kg/día en forma de exposición sistémica) produjo un daño renal irreversible y persistente. Estos efectos previamente mencionados representan un efecto farmacológico exagerado ya esperado de los inhibidores de la enzima convertidora de angiotensina II y de los bloqueadores tipo I de la angiotensina II; esos efectos se observan al tratar a ratas durante los primeros 13 días de vida. Este periodo coincide con las 36 semanas de gestación en los seres humanos, que en ocasiones pueden extenderse hasta 44 semanas después de la concepción en seres humanos. En el estudio con Valsartán administrado a ratas jóvenes, las ratas recibieron dosis hasta el día 70, por lo cual no es posible excluir la existencia de efectos en la maduración renal (4-6 semanas después del parto). La maduración de la función renal es un proceso continuo que se presenta durante el primer año de vida en los seres humanos. Por consiguiente, no es posible excluir que esto tenga relevancia clínica en niños menores de 1 año de edad, mientras que por otro lado, los datos preclínicos no indican la existencia de un problema de seguridad en niños mayores de 1 año de edad.
Indicaciones.
Hipertensión: Tratamiento de la hipertensión. Insuficiencia cardiaca: Tratamiento de la insuficiencia cardiaca clase II-IV de la NYHA (New York Heart Association) en pacientes que estén recibiendo uno de los tratamientos habituales, como diuréticos, digitálicos y o bien, inhibidores de la enzima convertidora de angiotensina IECA o bien betabloqueadores pero no ambos; no es obligatorio que el paciente esté recibiendo todos estos tratamientos habituales. Post-infarto de miocardio (40 mg): ALSARKARE está indicado para mejorar la supervivencia después de un infarto de miocardio en pacientes clínicamente estables con síntomas, signos clínicos o signos radiológicos de insuficiencia ventricular izquierda o con disfunción sistólica del ventrículo izquierdo.
Dosificación.
Alsarkare puede administrarse de manera independiente a una comida, pero debe administrarse con agua. Vía de administración: Para uso oral. Adultos: Hipertensión: La dosis inicial recomendada de Valsartán consiste en 80 mg administrados una vez al día. El efecto antihipertensivo se presenta sustancialmente dentro del plazo de 2 semanas, y los efectos máximos se alcanzan en 4 semanas. En algunos pacientes cuya presión arterial no se encuentre controlada adecuadamente, se puede aumentar la dosis a 160 mg, y a un máximo de 320 mg. Valsartán también puede administrarse junto con otros agentes antihipertensivos. La adición de un diurético, como hidroclorotiazida, disminuirá aún más la presión arterial en estos pacientes. Infarto de miocardio reciente: En pacientes clínicamente estables, se puede iniciar la terapia desde 12 horas después de un infarto de miocardio. Después de administrar una dosis inicial de 20 mg dos veces al día, se debe ajustar la dosis de Valsartán a 40 mg dos veces al día durante las próximas semanas. La dosis inicial se suministra con el comprimido ranurado de 40 mg. La dosis máxima objetivo consiste en 160 mg administrados dos veces al día. En general, se recomienda que los pacientes alcancen un nivel posológico de 80 mg administrados dos veces al día hacia las dos semanas después de haber iniciado el tratamiento, y que la dosis máxima objetivo, de 160 mg administrados dos veces al día, sea alcanzada a los 3 meses según la tolerabilidad del paciente. Si se presenta una hipotensión sintomática o una disfunción renal, se debe contemplar una reducción de la dosis. Valsartán puede utilizarse en pacientes tratados con otras terapias administradas post-infarto de miocardio, como por ejemplo, trombolíticos, ácido acetilsalicílico, betabloqueantes, estatinas y diuréticos. No se recomienda la combinación con inhibidores de la ECA (Enzima convertidora de Angiotensina) (ver Advertencias). La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. Insuficiencia cardiaca: La dosis inicial recomendada de Valsartán consiste en 40 mg administrados dos veces al día. El ajuste ascendente hasta 80 mg y 160 mg administrados dos veces al día debe hacerse a intervalos de cuando menos dos semanas a la dosis más alta, según la tolerabilidad del paciente. Se debe contemplar una reducción en la dosis de diuréticos concomitantes. La dosis diaria máxima administrada en estudios clínicos consiste en 320 mg en dosis divididas. Valsartán puede administrarse junto con otras terapias para insuficiencia cardiaca. Sin embargo, no se recomienda la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán (ver Advertencias). La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. Niños: Niños y adolescentes de 6 a 18 años de edad: La dosis inicial consiste en 40 mg administrados una vez al día para niños que pesen menos de 35 kg, y de 80 mg administrados una vez al día para los niños que pesen 35 kg o más. Se debe ajustar la dosis según la respuesta de la presión arterial. Para conocer las dosis máximas estudiadas en estudios clínicos, consulte la siguiente tabla. No se han estudiado dosis más altas que las incluidas en el listado adjunto, por lo cual las mismas no se recomiendan.

Niños menores de 6 años de edad: No se han establecido los perfiles de seguridad y eficacia de Valsartán en niños de 1 a 6 años de edad. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia renal: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia hepática: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis. Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg. Insuficiencia cardiaca e infarto de miocardio reciente en pacientes pediátricos: No se recomienda el uso de Valsartán en el tratamiento de la insuficiencia cardiaca o del infarto de miocardio reciente en niños y adolescentes menores de 18 años de edad, debido a la falta de datos sobre seguridad y eficacia. Personas de edad avanzada: No es necesario ajustar la dosis en personas de edad avanzada. Insuficiencia renal: No es necesario ajustar la dosis en pacientes con una depuración de creatinina > 10 ml/min (ver Advertencias). Insuficiencia hepática: Valsartán está contraindicado en pacientes con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones y Advertencias). En pacientes con insuficiencia hepática leve a moderada sin colestasis, la dosis de Valsartán no debe exceder 80 mg.
Contraindicaciones.
Valsartán está contraindicado en: Hipersensibilidad a la sustancia activa o a cualquiera de los excipientes, Insuficiencia hepática grave, cirrosis biliar y colestasis, El segundo y el tercer trimestre de embarazo (ver Advertencias; Embarazo y lactancia).
Reacciones adversas.
Datos de estudios clínicos y datos posteriores a la comercialización: En estudios clínicos controlados realizados en pacientes adultos con hipertensión, la incidencia global de reacciones adversas (RA) fue similar con el placebo y es consistente con el perfil farmacológico de Valsartán. La incidencia de RA no pareció relacionarse con la dosis o con la duración del tratamiento, ni tampoco mostró asociación alguna con el sexo, la edad o la raza. Se ha evaluado el efecto antihipertensivo de Valsartán en dos estudios clínicos aleatorizados, y doble ciegos que se realizaron en 561 pacientes pediátricos de 6 a 18 años de edad. Con la excepción de trastornos gastrointestinales aislados (como dolor abdominal, náuseas, vómito) y mareos, no se identificaron diferencias relevantes en cuanto al tipo, la frecuencia y la intensidad de las reacciones adversas entre el perfil de seguridad de los pacientes pediátricos de 6 a 18 años de edad, y las reacciones previamente reportadas en pacientes adultos. La evaluación neurocognitiva y del desarrollo de los pacientes pediátricos de 6 a 16 años de edad no reveló efectos adversos globales clínicamente relevantes después de administrar un tratamiento con Valsartán durante un máximo de un año. En un estudio aleatorizado, doble ciego y realizado en 90 niños de 1 a 6 años de edad, el cual fue seguido por un estudio abierto de extensión de un año de duración, se observaron dos muertes y casos aislados de aumentos manifiestos en las concentraciones de aminotransferasas hepáticas. Estos casos se produjeron en una población que presentaba comorbilidades significativas. No se ha establecido una relación causal con Valsartán. En un segundo estudio en el que se aleatorizó a 75 niños de 1 a 6 años de edad, no se presentaron aumentos significativos en las concentraciones de aminotransferasas hepáticas ni muertes al administrar el tratamiento con Valsartán. Los casos de hiperkalemia se observaron con mayor frecuencia en niños y adolescentes de 6 a 18 años de edad con nefropatía crónica subyacente. El perfil de seguridad observado en estudios clínicos controlados, que se realizaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca, varía del perfil global de seguridad observado en pacientes hipertensos. Esto puede relacionarse con la enfermedad subyacente de los pacientes. A continuación se enumeran las reacciones adversas que se presentaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca: A continuación se listan las reacciones adversas reportadas a partir de estudios clínicos, experiencia posterior a la comercialización y hallazgos de laboratorio, según su clase de sistema orgánico. Para todas las reacciones adversas reportadas a partir de la experiencia posterior a la comercialización y los hallazgos de laboratorio, no es posible aplicar cualquier frecuencia de reacciones adversas, por lo cual se mencionan con una frecuencia "desconocida". Las reacciones adversas se clasifican según su frecuencia utilizando la siguiente convención: Muy comunes ≥1/10. Comunes ≥1/100 a < 1/10. Poco comunes ≥1/1.000 a < 1/100. Raras ≥1/10000 a < 1/1.000. Muy raras < 1/10.000. Frecuencia desconocida (no se pueden estimar a partir de los datos disponibles). Hipertensión: Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: disminución en las concentraciones de hemoglobina, disminución de hematocrito, neutropenia, trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos vasculares: Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco común: dolor abdominal. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática, incluyendo un aumento en las concentraciones séricas de bilirrubina. Trastornos de la piel y el tejido subcutáneo: Frecuencia desconocida: angioedema, exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo. Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Frecuencia desconocida: insuficiencia y deterioro renal, aumento en las concentraciones séricas de creatinina. Trastornos generales y afecciones en el sitio de administración: Poco común: fatiga. Antecedentes recientes de infarto de miocardio y/o insuficiencia cardiaca (estudio realizado en pacientes adultos solamente): Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Poco común: hiperkalemia. Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del sistema nervioso: Comunes: mareos, vértigo postural. Poco comunes: síncope, cefalea. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos cardiacos: Poco común: insuficiencia cardíaca. Trastornos vasculares: Comunes: hipotensión, hipotensión ortostática. Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco comunes: náuseas, diarrea. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática. Trastornos de la piel y el tejido subcutáneo. Poco común: angioedema. Frecuencia desconocida: exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo: Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Comunes: insuficiencia y deterioro renal. Poco comunes: insuficiencia renal aguda, aumento en las concentraciones séricas de creatinina. Frecuencia desconocida: aumento en las concentraciones sanguíneas de nitrógeno ureico. Trastornos generales y afecciones en el sitio de administración: Poco comunes: astenia, fatiga.
Advertencias.
Hiperkalemia: No se recomienda el uso concomitante con complementos de potasio, diuréticos ahorradores de potasio, sustitutos de la sal que contengan potasio u otros agentes que puedan aumentar las concentraciones de potasio (heparina, etc.). Se debe instituir un seguimiento de las concentraciones de potasio, según sea necesario (ver Interacciones). Función renal deteriorada: Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 ml/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. No es necesario ajustar la dosis en pacientes adultos con una depuración de creatinina > 10 ml/min. Insuficiencia hepática: En pacientes con insuficiencia hepática leve a moderada sin colestasis, Valsartán debe utilizarse con precaución. Pacientes con depleción de sodio y/o volumen: En pacientes con una depleción grave de sodio y/o volumen, como aquellos que reciben dosis altas de diuréticos, se pueden presentar casos raros de hipotensión sintomática después de iniciar la terapia con Valsartán. Se debe corregir la depleción de sodio y/o volumen antes de iniciar el tratamiento con Valsartán, reduciendo por ejemplo la dosis de diuréticos. Estenosis de la arteria renal: En pacientes con estenosis bilateral de la arteria renal, o estenosis de un riñón único, no se ha establecido el uso seguro de Valsartán. La administración a corto plazo de Valsartán, a doce pacientes con hipertensión renovascular secundaria a una estenosis unilateral de la arteria renal, no indujo cambios significativos en la hemodinámica renal, la creatinina sérica o el nitrógeno ureico en sangre (BUN). Sin embargo, otros agentes que afectan al sistema de renina-angiotensina podrían aumentar las concentraciones sanguíneas de urea y las concentraciones séricas de creatinina en pacientes con estenosis unilateral de la arteria renal, por lo cual se recomienda instaurar un seguimiento de la función renal en los pacientes tratados con Valsartán. Trasplante renal: Actualmente no se tiene experiencia sobre el uso seguro de Valsartán en pacientes que se han sometido recientemente a un trasplante de riñón. Hiperaldosteronismo primario: Los pacientes con hiperaldosteronismo primario no deben recibir tratamiento con Valsartán, ya que su sistema de renina-angiotensina no se encuentra activado. Estenosis de la válvula aórtica y mitral, miocardiopatía hipertrófica obstructiva: Al igual que con otros vasodilatadores, se recomienda tener precaución especial en los pacientes que padezcan estenosis aórtica o mitral, o miocardiopatía hipertrófica obstructiva (HOCM). Embarazo: No se debe iniciar la administración de antagonistas de los receptores de la angiotensina II (ARAII) durante el embarazo. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alterna (ver Contraindicaciones; Embarazo y lactancia). Infarto de miocardio reciente: La combinación de Captopril y Valsartán no ha demostrado ningún beneficio clínico adicional, sino más bien aumentó el riesgo de desarrollar eventos adversos, en comparación con el tratamiento con sus respectivas monoterapias. Por lo tanto, no se recomienda la combinación de Valsartán con ningún inhibidor de la ECA. Se debe tener precaución al iniciar la terapia en pacientes con antecedentes recientes de infarto de miocardio. La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con antecedentes recientes de infarto de miocardio comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán no ha demostrado beneficio clínico alguno. Esta combinación aparentemente aumenta el riesgo de desarrollar eventos adversos, por lo cual no se recomienda. Se debe tener precaución al iniciar la terapia en pacientes con insuficiencia cardiaca. La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con insuficiencia cardiaca comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Otras afecciones con estimulación del sistema de renina-angiotensina: En aquellos pacientes cuya función renal pueda depender de la actividad del sistema de renina-angiotensina (por ejemplo, pacientes con insuficiencia cardiaca congestiva grave), el tratamiento con inhibidores de la enzima convertidora de angiotensina se ha asociado con el desarrollo de oliguria y/o azotemia progresiva y, en casos raros, con insuficiencia renal aguda y/o la muerte. Como Valsartán es un antagonista de la angiotensina II, no es posible excluir que el uso de Valsartán pueda asociarse con un deterioro de la función renal. Lactosa: El producto contiene lactosa. Los pacientes con problemas hereditarios poco usuales de intolerancia a la galactosa, insuficiencia de lactasa de Lapp o malabsorción de glucosa y galactosa, no deberán tomar este medicamento. Población pediátrica: Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio durante el tratamiento con Valsartán. En especial, esto se aplica cuando Valsartán se administra en presencia de otras afecciones (fiebre, deshidratación) que puedan deteriorar la función renal. Función hepática deteriorada: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones). Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg.
Interacciones.
No se recomienda el uso concomitante: Litio: Se han reportado aumentos reversibles en las concentraciones séricas de litio y toxicidad durante el uso concomitante de inhibidores de la ECA. Debido a la falta de experiencia sobre el uso concomitante de Valsartán y litio, no se recomienda esta combinación. Si fuera necesaria la combinación, se recomienda vigilar rigurosamente las concentraciones séricas de litio. Diuréticos ahorradores de potasio, complementos de potasio, sustitutos de la sal que contienen potasio y otras sustancias que pueden aumentar las concentraciones de potasio: Si se considera necesario administrar en combinación con Valsartán algún medicamento que afecte las concentraciones de potasio, se recomienda vigilar las concentraciones plasmáticas de potasio. Se requiere tener precaución con el uso concomitante de: Medicamentos antiinflamatorios no esteroideos (AINEs), incluyendo inhibidores selectivos de la COX-2, ácido acetilsalicílico > 3 g/día y AINEs no selectivos: Cuando los antagonistas de la angiotensina II se administran simultáneamente con AINEs, se puede presentar una atenuación del efecto antihipertensivo. Además, el uso concomitante de antagonistas de la angiotensina II y AINEs podría conducir a un mayor riesgo de experimentar un agravamiento de la función renal y un aumento en las concentraciones séricas de potasio. Por lo tanto, se recomienda vigilar la función renal al inicio del tratamiento e implementar una hidratación adecuada del paciente. Falta de interacciones: En estudios de interacción farmacológica realizados con Valsartán, no se han encontrado interacciones de significancia clínica con Valsartán o con cualquiera de las siguientes sustancias: cimetidina, warfarina, furosemida, digoxina, atenolol, indometacina, hidroclorotiazida, amlodipino, glibenclamida. Población pediátrica: En el tratamiento de la hipertensión en niños y adolescentes, donde las anormalidades renales subyacentes son comunes, se recomienda tener precaución con el uso concomitante de Valsartán y otras sustancias que inhiben el sistema de renina-angiotensina-aldosterona, ya que podría aumentar las concentraciones séricas de potasio. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Embarazo y lactancia: Fertilidad: Valsartán no produjo efectos adversos en el desempeño reproductivo de las ratas macho o hembra que recibieron dosis orales de hasta 200 mg/kg/día. Esta dosis equivale a 6 veces la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). Embarazo: No se recomienda el uso de antagonistas de los receptores de la angiotensina II (ARAII) durante el primer trimestre de embarazo (ver Advertencias). El uso de ARAII se contraindica durante el segundo y el tercer trimestre de embarazo (ver Contraindicaciones; Advertencias y precauciones). La evidencia epidemiológica sobre el riesgo de teratogenicidad tras la exposición a inhibidores de la ECA durante el primer trimestre de embarazo no han sido concluyentes; sin embargo, no es posible descartar un pequeño aumento en el riesgo. Aunque no se dispone de datos epidemiológicos específicos sobre el riesgo de administrar ARAII, es posible que existan riesgos similares para esta clase de fármacos. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alternativa. Se sabe que la exposición a la terapia con AIIRA durante el segundo y el tercer trimestre induce fetotoxicidad humana (disminución de la función renal, oligohidramnios, retraso en la osificación del cráneo) y toxicidad neonatal (insuficiencia renal, hipotensión, e hiperkalemia). Si se ha producido una exposición a ARAII a partir del segundo trimestre de embarazo, se recomienda practicar un ultrasonido de la función renal y el cráneo. Se debe vigilar estrechamente a los lactantes cuyas madres hayan tomado ARAII (ver Contraindicaciones y Advertencias). Lactancia: Debido a que no se dispone de información sobre el uso de Valsartán durante la lactancia, no se recomienda administrar Valsartán, y es preferible administrar tratamientos alternativos con perfiles de seguridad mejor establecidos durante la lactancia, especialmente en recién nacidos o prematuros. Capacidad para realizar tareas que requieren discernimiento, habilidades motrices o cognitivas: No se han llevado a cabo estudios sobre los efectos en la capacidad para conducir. Al conducir u operar maquinaria, se debe tener en cuenta que, ocasionalmente, se pueden presentar mareos o cansancio.
Conservación.
Almacenar a temperaturas inferiores a 30°C. Vencimiento: La fecha de caducidad se indica en el envase. Uso y manejo: No hay requisitos especiales para el uso o el manejo de este producto. Incompatibilidades: No se dispone de datos relevantes.
Sobredosificación.
Síntomas y signos: La sobredosis con Valsartán es capaz de ocasionar una hipotensión manifiesta, que podría conducir a bajos niveles de conciencia, un colapso circulatorio y/o choque. Tratamiento: Las medidas terapéuticas dependen del momento de la ingestión y el tipo y la intensidad de los síntomas; la estabilización del estado circulatorio es de primordial importancia. Si se presenta hipotensión, se debe colocar al paciente en posición horizontal y se debe llevar a cabo una corrección del volumen sanguíneo. Es poco probable que Valsartán se elimine a través de hemodiálisis.
Presentación.
Blister de Alu/Alu. Comprimidos recubiertos 40 mg.
ALSARKARE
ETEX
80 mg
Antihipertensivo.
Composición.
ALSARKARE COMPRIMIDOS RECUBIERTOS 80 mg contiene: Valsartán 80 mg. Excipientes: Lactosa monohidratada, celulosa microcristalina, almidón de maíz, crospovidona, povidona, Dióxido de Silicio coloidal anhidro, estearato de magnesio, Instacoat universal (ICE-U-0116 rosa [Hipromelosa, Macrogol, Dióxido de Titanio, Óxido de Hierro Rojo, Óxido de Hierro Negro, Óxido de Hierro Amarillo]) c.s.
Farmacología.
Farmacodinamia: Grupo farmacoterapéutico: Antagonistas de la angiotensina II, Código ATC. C09CA03. Mecanismo de acción: Efectos farmacodinámicos: Valsartán es un potente antagonista oral, activo y específico de los receptores de la angiotensina II (Ang II). Actúa selectivamente sobre el subtipo de receptor de AT1, que es responsable de las acciones conocidas de la angiotensina II. El aumento en las concentraciones plasmáticas de Ang II, tras un bloqueo del receptor de AT1 con Valsartán, podría estimular al receptor de AT2 no bloqueado, lo cual parece contrarrestar el efecto del receptor de AT1. Valsartán no exhibe ninguna actividad agonista parcial en el receptor de AT1, y tiene mucho mayor (aproximadamente 20.000 veces) afinidad por el receptor de AT1 que por el receptor de AT2. No se sabe si Valsartán se une o bloquea otros receptores hormonales o canales iónicos con importancia conocida en la regulación cardiovascular. Valsartán no inhibe la ECA (también conocida como cininasa II), que transforma la Ang I en Ang II y degrada la bradiquinina. Como no hay un efecto en la ECA, ni tampoco potenciación de bradiquinina o sustancia P, es poco probable que los antagonistas de la angiotensina II se asocien con tos. En estudios clínicos en los que se comparó Valsartán con un inhibidor de la ECA, la incidencia de tos seca fue significativamente menor (P < 0,05) en los pacientes tratados con Valsartán que en aquellos que recibieron un inhibidor de la ECA (2,6% frente a 7,9%, respectivamente). En un estudio clínico de pacientes con antecedentes de tos seca durante la terapia con algún inhibidor de la ACE, 19,5% de los sujetos del estudio que recibieron Valsartán y 19,0% de aquellos que recibieron algún diurético tiazídico experimentaron tos, en comparación con 68,5% de los sujetos tratados con algún inhibidor de la ECA (P < 0,05). Farmacocinética: Absorción: Tras la administración oral de Valsartán en monoterapia, las concentraciones plasmáticas máximas de Valsartán se alcanzan en un plazo de 2-4 horas con la formulación en comprimidos y de 1-2 horas con la formulación en solución. La biodisponibilidad absoluta media es de 23% y 39% con las formulaciones en tabletas y solución, respectivamente. Los alimentos disminuyen el nivel de exposición (medido por el ABC) a Valsartán en
aproximadamente 40%, y su concentración plasmática máxima (Cmáx) en aproximadamente 50%, aunque a partir de aproximadamente 8 h después de su administración, las concentraciones plasmáticas de Valsartán son similares en los grupos postprandiales y en ayunas. Sin embargo, esta reducción en el ABC no se ve acompañada de una reducción clínicamente significativa en el efecto terapéutico, por lo cual Valsartán puede administrarse con o sin alimentos. Distribución: El volumen de distribución en estado estable de Valsartán tras su administración intravenosa es de aproximadamente 17 litros, lo cual indica que Valsartán no se distribuye ampliamente en los tejidos. Valsartán tiene un alto grado de unión a proteínas séricas (94-97%), principalmente a la albúmina sérica. Metabolismo: Valsartán no experimenta un alto grado de biotransformación, ya que sólo alrededor de 20% de la dosis se recupera en forma de metabolitos. Se ha identificado un metabolito hidroxi en el plasma a concentraciones bajas (menos de 10% del ABC de Valsartán). Este metabolito es farmacológicamente inactivo. Eliminación: Valsartán muestra una cinética de descomposición multiexponencial (t½a < 1 h y t½b aproximadamente 9 h). Valsartán se elimina principalmente mediante excreción biliar en las heces (aproximadamente 83% de la dosis) y por vía renal en la orina (aproximadamente 13% de la dosis), principalmente como fármaco inalterado. Tras su administración intravenosa, la depuración plasmática de Valsartán es de aproximadamente 2 L/h y su depuración renal es de 0,62 L/h (aproximadamente 30% de la depuración total). La vida media de Valsartán es de 6 horas. Poblaciones especiales de pacientes: Niños: En un estudio realizado en 26 pacientes pediátricos hipertensos (de 1 a 16 años de edad) que recibieron una dosis única de una suspensión de Valsartán (media: 0,9 a 2 mg/kg, con una dosis máxima de 80 mg), la depuración (litros/h/kg) de Valsartán fue similar en todo el rango de edad de 1 a 16 años, y a la de los adultos que recibieron la misma formulación. Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 mL/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Personas de edad avanzada: En algunos sujetos de edad avanzada, se observó una exposición sistémica a Valsartán algo mayor que en los sujetos jóvenes; sin embargo, no se ha demostrado que esto tenga alguna significancia clínica. Insuficiencia renal: Como era de esperarse de un compuesto cuya depuración renal representa sólo el 30% de la depuración plasmática total, no se observó correlación alguna entre la función renal y la exposición sistémica a Valsartán. Por lo tanto, no es necesario ajustar la dosis en pacientes con insuficiencia renal (depuración de creatinina > 10 mL/min). Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 mL/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. Valsartán tiene un alto grado de unión a proteínas plasmáticas, por lo cual es poco probable que se elimine a través de diálisis. Insuficiencia hepática: Aproximadamente 70% de la dosis absorbida se elimina en la bilis, fundamentalmente en forma inalterada. Valsartán no experimenta ninguna biotransformación notable. Se observó una duplicación de la exposición (ABC) en pacientes con insuficiencia hepática leve a moderada, en comparación con sujetos sanos. Sin embargo, no se observó correlación alguna entre la concentración plasmática de Valsartán y el grado de disfunción hepática. No se ha estudiado Valsartán en pacientes con disfunción hepática grave. Otras características de los pacientes: Pacientes con insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, el tiempo promedio para alcanzar la concentración máxima y la vida media de eliminación de Valsartán son similares a los observados en voluntarios sanos. Los valores de ABC y Cmáx de Valsartán casi son proporcionales al aumentar la dosis en el rango clínico de dosificación (40 a 160 mg administrados dos veces al día). El factor de acumulación promedio es de aproximadamente 1,7. La depuración aparente de Valsartán tras su administración oral es de aproximadamente 4,5 L/h. La edad no afecta la depuración aparente en pacientes con insuficiencia cardiaca. Información no clínica: Los datos pre-clínicos no revelaron riesgos especiales para los seres humanos, según los estudios convencionales de seguridad farmacológica, toxicidad de dosis repetidas, genotoxicidad y potencial carcinogénico. En ratas, la administración de dosis tóxicas para las madres (600 mg/kg/día) durante los últimos días de la gestación y la lactancia condujo a una menor supervivencia, un menor aumento en el peso y un retraso en el desarrollo (desprendimiento del pabellón auricular y apertura del canal auditivo) en la descendencia. Estas dosis administradas en ratas (600 mg/kg/día) son aproximadamente 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En estudios pre-clínicos de seguridad, las dosis elevadas de Valsartán (200 a 600 mg/kg de peso corporal) administradas en ratas ocasionaron una disminución de los parámetros de glóbulos rojos (eritrocitos, hemoglobina, hematocrito), así como indicios de cambios en la hemodinamia renal (ligero aumento en las concentraciones plasmáticas de urea, e hiperplasia tubular renal y basofilia en machos). Estas dosis administradas en ratas (200 y 600 mg/kg/día) son aproximadamente 6 y 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En monos tití que recibieron dosis similares, los cambios fueron semejantes aunque más graves, sobre todo en los riñones, donde los cambios evolucionaron a una nefropatía con aumentos en las concentraciones de urea y creatinina. En ambas especies, también se observó hipertrofia de las células renales yuxtaglomerulares. Se consideró que todos los cambios fueron ocasionados por la acción farmacológica de Valsartán, la cual produce hipotensión prolongada, especialmente en monos tití. En lo que respecta a las dosis terapéuticas de Valsartán en seres humanos, la hipertrofia de las células renales yuxtaglomerulares no parece tener relevancia alguna. Población pediátrica: La administración oral diaria de Valsartán a ratas recién nacidas/jóvenes (entre los 7 y 70 días de vida), a dosis tan bajas como 1 mg/kg/día (aproximadamente 10-35% de la dosis máxima recomendada para uso pediátrico de 4 mg/kg/día en forma de exposición sistémica) produjo un daño renal irreversible y persistente. Estos efectos previamente mencionados representan un efecto farmacológico exagerado ya esperado de los inhibidores de la enzima convertidora de angiotensina II y de los bloqueadores tipo I de la angiotensina II; esos efectos se observan al tratar a ratas durante los primeros 13 días de vida. Este periodo coincide con las 36 semanas de gestación en los seres humanos, que en ocasiones pueden extenderse hasta 44 semanas después de la concepción en seres humanos. En el estudio con Valsartán administrado a ratas jóvenes, las ratas recibieron dosis hasta el día 70, por lo cual no es posible excluir la existencia de efectos en la maduración renal (4-6 semanas después del parto). La maduración de la función renal es un proceso continuo que se presenta durante el primer año de vida en los seres humanos. Por consiguiente, no es posible excluir que esto tenga relevancia clínica en niños menores de 1 año de edad, mientras que por otro lado, los datos preclínicos no indican la existencia de un problema de seguridad en niños mayores de 1 año de edad.
Indicaciones.
Hipertensión: Tratamiento de la hipertensión. Insuficiencia cardiaca: Tratamiento de la insuficiencia cardiaca clase II-IV de la NYHA (New York Heart Association) en pacientes que estén recibiendo uno de los tratamientos habituales, como diuréticos, digitálicos y o bien, inhibidores de la enzima convertidora de angiotensina IECA o bien betabloqueadores pero no ambos; no es obligatorio que el paciente esté recibiendo todos estos tratamientos habituales. Post-infarto de miocardio (80 mg): ALSARKARE está indicado para mejorar la supervivencia después de un infarto de miocardio en pacientes clínicamente estables con síntomas, signos clínicos o signos radiológicos de insuficiencia ventricular izquierda o con disfunción sistólica del ventrículo izquierdo.
Dosificación.
Alsarkare puede administrarse de manera independiente a una comida, pero debe administrarse con agua. Vía de administración: Para uso oral. Adultos. Hipertensión: La dosis inicial recomendada de Valsartán consiste en 80 mg administrados una vez al día. El efecto antihipertensivo se presenta sustancialmente dentro del plazo de 2 semanas, y los efectos máximos se alcanzan en 4 semanas. En algunos pacientes cuya presión arterial no se encuentre controlada adecuadamente, se puede aumentar la dosis a 160 mg, y a un máximo de 320 mg. Valsartán también puede administrarse junto con otros agentes antihipertensivos. La adición de un diurético, como hidroclorotiazida, disminuirá aún más la presión arterial en estos pacientes. Infarto de miocardio reciente: En pacientes clínicamente estables, se puede iniciar la terapia desde 12 horas después de un infarto de miocardio. Después de administrar una dosis inicial de 20 mg dos veces al día, se debe ajustar la dosis de Valsartán a 40 mg, 80 mg y 160 mg dos veces al día durante las próximas semanas. La dosis inicial se suministra con el comprimido ranurado de 40 mg. La dosis máxima objetivo consiste en 160 mg administrados dos veces al día. En general, se recomienda que los pacientes alcancen un nivel posológico de 80 mg administrados dos veces al día hacia las dos semanas después de haber iniciado el tratamiento, y que la dosis máxima objetivo, de 160 mg administrados dos veces al día, sea alcanzada a los 3 meses según la tolerabilidad del paciente. Si se presenta una hipotensión sintomática o una disfunción renal, se debe contemplar una reducción de la dosis. Valsartán puede utilizarse en pacientes tratados con otras terapias administradas post-infarto de miocardio, como por ejemplo, trombolíticos, ácido acetilsalicílico, betabloqueantes, estatinas y diuréticos. No se recomienda la combinación con inhibidores de la ECA (Enzima convertidora de Angiotensina) (ver Advertencias y precauciones). La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. Insuficiencia cardiaca: La dosis inicial recomendada de Valsartán consiste en 40 mg administrados dos veces al día. El ajuste ascendente hasta 80 mg y 160 mg administrados dos veces al día debe hacerse a intervalos de cuando menos dos semanas a la dosis más alta, según la tolerabilidad del paciente. Se debe contemplar una reducción en la dosis de diuréticos concomitantes. La dosis diaria máxima administrada en estudios clínicos consiste en 320 mg en dosis divididas. Valsartán puede administrarse junto con otras terapias para insuficiencia cardiaca. Sin embargo, no se recomienda la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán (ver Advertencias y precauciones). La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. Niños: Niños y adolescentes de 6 a 18 años de edad: La dosis inicial consiste en 40 mg administrados una vez al día para niños que pesen menos de 35 kg, y de 80 mg administrados una vez al día para los niños que pesen 35 kg o más. Se debe ajustar la dosis según la respuesta de la presión arterial. Para conocer las dosis máximas estudiadas en estudios clínicos, consulte la siguiente tabla. No se han estudiado dosis más altas que las incluidas en el listado adjunto, por lo cual las mismas no se recomiendan.
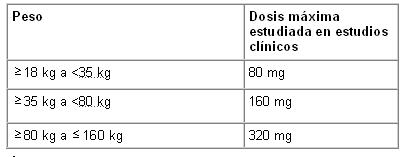
Niños menores de 6 años de edad: No se han establecido los perfiles de seguridad y eficacia de Valsartán en niños de 1 a 6 años de edad. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia renal: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia hepática: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis. Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg. Insuficiencia cardiaca e infarto de miocardio reciente en pacientes pediátricos: No se recomienda el uso de Valsartán en el tratamiento de la insuficiencia cardiaca o del infarto de miocardio reciente en niños y adolescentes menores de 18 años de edad, debido a la falta de datos sobre seguridad y eficacia. Personas de edad avanzada: No es necesario ajustar la dosis en personas de edad avanzada. Insuficiencia renal: No es necesario ajustar la dosis en pacientes con una depuración de creatinina > 10 ml/min (ver Advertencias). Insuficiencia hepática: Valsartán está contraindicado en pacientes con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones y Advertencias). En pacientes con insuficiencia hepática leve a moderada sin colestasis, la dosis de Valsartán no debe exceder 80 mg.
Contraindicaciones.
Valsartán está contraindicado en: Hipersensibilidad a la sustancia activa o a cualquiera de los excipientes. Insuficiencia hepática grave, cirrosis biliar y colestasis. El segundo y el tercer trimestre de embarazo (ver Advertencias; Embarazo y lactancia).
Reacciones adversas.
Datos de estudios clínicos y datos posteriores a la comercialización: En estudios clínicos controlados realizados en pacientes adultos con hipertensión, la incidencia global de reacciones adversas (RA) fue similar con el placebo y es consistente con el perfil farmacológico de Valsartán. La incidencia de RA no pareció relacionarse con la dosis o con la duración del tratamiento, ni tampoco mostró asociación alguna con el sexo, la edad o la raza. Se ha evaluado el efecto antihipertensivo de Valsartán en dos estudios clínicos aleatorizados, y doble ciegos que se realizaron en 561 pacientes pediátricos de 6 a 18 años de edad. Con la excepción de trastornos gastrointestinales aislados (como dolor abdominal, náuseas, vómito) y mareos, no se identificaron diferencias relevantes en cuanto al tipo, la frecuencia y la intensidad de las reacciones adversas entre el perfil de seguridad de los pacientes pediátricos de 6 a 18 años de edad, y las reacciones previamente reportadas en pacientes adultos. La evaluación neurocognitiva y del desarrollo de los pacientes pediátricos de 6 a 16 años de edad no reveló efectos adversos globales clínicamente relevantes después de administrar un tratamiento con Valsartán durante un máximo de un año. En un estudio aleatorizado, doble ciego y realizado en 90 niños de 1 a 6 años de edad, el cual fue seguido por un estudio abierto de extensión de un año de duración, se observaron dos muertes y casos aislados de aumentos manifiestos en las concentraciones de aminotransferasas hepáticas. Estos casos se produjeron en una población que presentaba comorbilidades significativas. No se ha establecido una relación causal con Valsartán. En un segundo estudio en el que se aleatorizó a 75 niños de 1 a 6 años de edad, no se presentaron aumentos significativos en las concentraciones de aminotransferasas hepáticas ni muertes al administrar el tratamiento con Valsartán. Los casos de hiperkalemia se observaron con mayor frecuencia en niños y adolescentes de 6 a 18 años de edad con nefropatía crónica subyacente. El perfil de seguridad observado en estudios clínicos controlados, que se realizaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca, varía del perfil global de seguridad observado en pacientes hipertensos. Esto puede relacionarse con la enfermedad subyacente de los pacientes. A continuación se enumeran las reacciones adversas que se presentaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca: A continuación se listan las reacciones adversas reportadas a partir de estudios clínicos, experiencia posterior a la comercialización y hallazgos de laboratorio, según su clase de sistema orgánico. Para todas las reacciones adversas reportadas a partir de la experiencia posterior a la comercialización y los hallazgos de laboratorio, no es posible aplicar cualquier frecuencia de reacciones adversas, por lo cual se mencionan con una frecuencia "desconocida". Las reacciones adversas se clasifican según su frecuencia utilizando la siguiente convención: Muy comunes ≥1/10. Comunes ≥1/100 a < 1/10. Poco comunes ≥1/1.000 a < 1/100. Raras ≥1/10000 a < 1/1.000. Muy raras < 1/10.000. Frecuencia desconocida (no se pueden estimar a partir de los datos disponibles). Hipertensión: Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: disminución en las concentraciones de hemoglobina, disminución de hematocrito, neutropenia, trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos vasculares: Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco común: dolor abdominal. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática, incluyendo un aumento en las concentraciones séricas de bilirrubina. Trastornos de la piel y el tejido subcutáneo: Frecuencia desconocida: angioedema, exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo: Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Frecuencia desconocida: insuficiencia y deterioro renal, aumento en las concentraciones séricas de creatinina. Trastornos generales y afecciones en el sitio de administración: Poco común: fatiga. Antecedentes recientes de infarto de miocardio y/o insuficiencia cardiaca (estudio realizado en pacientes adultos solamente): Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Poco común: hiperkalemia. Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del sistema nervioso: Comunes: mareos, vértigo postural. Poco comunes: síncope, cefalea. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos cardiacos: Poco común: insuficiencia cardíaca. Trastornos vasculares: Comunes: hipotensión, hipotensión ortostática. Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco comunes: náuseas, diarrea. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática. Trastornos de la piel y el tejido subcutáneo: Poco común: angioedema. Frecuencia desconocida: exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo: Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Comunes: insuficiencia y deterioro renal. Poco comunes: insuficiencia renal aguda, aumento en las concentraciones séricas de creatinina. Frecuencia desconocida: aumento en las concentraciones sanguíneas de nitrógeno ureico. Trastornos generales y afecciones en el sitio de administración: Poco comunes: astenia, fatiga.
Advertencias.
Hiperkalemia: No se recomienda el uso concomitante con complementos de potasio, diuréticos ahorradores de potasio, sustitutos de la sal que contengan potasio u otros agentes que puedan aumentar las concentraciones de potasio (heparina, etc.). Se debe instituir un seguimiento de las concentraciones de potasio, según sea necesario (ver Interacciones). Función renal deteriorada: Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 ml/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. No es necesario ajustar la dosis en pacientes adultos con una depuración de creatinina > 10 ml/min. Insuficiencia hepática: En pacientes con insuficiencia hepática leve a moderada sin colestasis, Valsartán debe utilizarse con precaución. Pacientes con depleción de sodio y/o volumen: En pacientes con una depleción grave de sodio y/o volumen, como aquellos que reciben dosis altas de diuréticos, se pueden presentar casos raros de hipotensión sintomática después de iniciar la terapia con Valsartán. Se debe corregir la depleción de sodio y/o volumen antes de iniciar el tratamiento con Valsartán, reduciendo por ejemplo la dosis de diuréticos. Estenosis de la arteria renal: En pacientes con estenosis bilateral de la arteria renal, o estenosis de un riñón único, no se ha establecido el uso seguro de Valsartán. La administración a corto plazo de Valsartán, a doce pacientes con hipertensión renovascular secundaria a una estenosis unilateral de la arteria renal, no indujo cambios significativos en la hemodinámica renal, la creatinina sérica o el nitrógeno ureico en sangre (BUN). Sin embargo, otros agentes que afectan al sistema de renina-angiotensina podrían aumentar las concentraciones sanguíneas de urea y las concentraciones séricas de creatinina en pacientes con estenosis unilateral de la arteria renal, por lo cual se recomienda instaurar un seguimiento de la función renal en los pacientes tratados con Valsartán. Trasplante renal: Actualmente no se tiene experiencia sobre el uso seguro de Valsartán en pacientes que se han sometido recientemente a un trasplante de riñón. Hiperaldosteronismo primario: Los pacientes con hiperaldosteronismo primario no deben recibir tratamiento con Valsartán, ya que su sistema de renina-angiotensina no se encuentra activado. Estenosis de la válvula aórtica y mitral, miocardiopatía hipertrófica obstructiva: Al igual que con otros vasodilatadores, se recomienda tener precaución especial en los pacientes que padezcan estenosis aórtica o mitral, o miocardiopatía hipertrófica obstructiva (HOCM). Embarazo: No se debe iniciar la administración de antagonistas de los receptores de la angiotensina II (ARAII) durante el embarazo. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alterna (ver Contraindicaciones y Embarazo y lactancia). Infarto de miocardio reciente: La combinación de Captopril y Valsartán no ha demostrado ningún beneficio clínico adicional, sino más bien aumentó el riesgo de desarrollar eventos adversos, en comparación con el tratamiento con sus respectivas monoterapias. Por lo tanto, no se recomienda la combinación de Valsartán con ningún inhibidor de la ECA. Se debe tener precaución al iniciar la terapia en pacientes con antecedentes recientes de infarto de miocardio. La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con antecedentes recientes de infarto de miocardio comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán no ha demostrado beneficio clínico alguno. Esta combinación aparentemente aumenta el riesgo de desarrollar eventos adversos, por lo cual no se recomienda. Se debe tener precaución al iniciar la terapia en pacientes con insuficiencia cardiaca. La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con insuficiencia cardiaca comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Otras afecciones con estimulación del sistema de renina-angiotensina: En aquellos pacientes cuya función renal pueda depender de la actividad del sistema de renina-angiotensina (por ejemplo, pacientes con insuficiencia cardiaca congestiva grave), el tratamiento con inhibidores de la enzima convertidora de angiotensina se ha asociado con el desarrollo de oliguria y/o azotemia progresiva y, en casos raros, con insuficiencia renal aguda y/o la muerte. Como Valsartán es un antagonista de la angiotensina II, no es posible excluir que el uso de Valsartán pueda asociarse con un deterioro de la función renal. Lactosa: El producto contiene lactosa. Los pacientes con problemas hereditarios poco usuales de intolerancia a la galactosa, insuficiencia de lactasa de Lapp o malabsorción de glucosa y galactosa, no deberán tomar este medicamento. Población pediátrica: Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio durante el tratamiento con Valsartán. En especial, esto se aplica cuando Valsartán se administra en presencia de otras afecciones (fiebre, deshidratación) que puedan deteriorar la función renal. Función hepática deteriorada: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones). Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg.
Interacciones.
No se recomienda el uso concomitante: Litio: Se han reportado aumentos reversibles en las concentraciones séricas de litio y toxicidad durante el uso concomitante de inhibidores de la ECA. Debido a la falta de experiencia sobre el uso concomitante de Valsartán y litio, no se recomienda esta combinación. Si fuera necesaria la combinación, se recomienda vigilar rigurosamente las concentraciones séricas de litio. Diuréticos ahorradores de potasio, complementos de potasio, sustitutos de la sal que contienen potasio y otras sustancias que pueden aumentar las concentraciones de potasio: Si se considera necesario administrar en combinación con Valsartán algún medicamento que afecte las concentraciones de potasio, se recomienda vigilar las concentraciones plasmáticas de potasio. Se requiere tener precaución con el uso concomitante de: Medicamentos antiinflamatorios no esteroideos (AINEs), incluyendo inhibidores selectivos de la COX-2, ácido acetilsalicílico > 3 g/día y AINEs no selectivos: Cuando los antagonistas de la angiotensina II se administran simultáneamente con AINEs, se puede presentar una atenuación del efecto antihipertensivo. Además, el uso concomitante de antagonistas de la angiotensina II y AINEs podría conducir a un mayor riesgo de experimentar un agravamiento de la función renal y un aumento en las concentraciones séricas de potasio. Por lo tanto, se recomienda vigilar la función renal al inicio del tratamiento e implementar una hidratación adecuada del paciente. Falta de interacciones: En estudios de interacción farmacológica realizados con Valsartán, no se han encontrado interacciones de significancia clínica con Valsartán o con cualquiera de las siguientes sustancias: cimetidina, warfarina, furosemida, digoxina, atenolol, indometacina, hidroclorotiazida, amlodipino, glibenclamida. Población pediátrica: En el tratamiento de la hipertensión en niños y adolescentes, donde las anormalidades renales subyacentes son comunes, se recomienda tener precaución con el uso concomitante de Valsartán y otras sustancias que inhiben el sistema de renina-angiotensina-aldosterona, ya que podría aumentar las concentraciones séricas de potasio. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Embarazo y lactancia: Fertilidad: Valsartán no produjo efectos adversos en el desempeño reproductivo de las ratas macho o hembra que recibieron dosis orales de hasta 200 mg/kg/día. Esta dosis equivale a 6 veces la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). Embarazo: No se recomienda el uso de antagonistas de los receptores de la angiotensina II (ARAII) durante el primer trimestre de embarazo (ver la sección de Advertencias y precauciones). El uso de ARAII se contraindica durante el segundo y el tercer trimestre de embarazo (ver Contraindicaciones; Advertencias y precauciones). La evidencia epidemiológica sobre el riesgo de teratogenicidad tras la exposición a inhibidores de la ECA durante el primer trimestre de embarazo no han sido concluyentes; sin embargo, no es posible descartar un pequeño aumento en el riesgo. Aunque no se dispone de datos epidemiológicos específicos sobre el riesgo de administrar ARAII, es posible que existan riesgos similares para esta clase de fármacos. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alternativa. Se sabe que la exposición a la terapia con AIIRA durante el segundo y el tercer trimestre induce fetotoxicidad humana (disminución de la función renal, oligohidramnios, retraso en la osificación del cráneo) y toxicidad neonatal (insuficiencia renal, hipotensión, e hiperkalemia). Si se ha producido una exposición a ARAII a partir del segundo trimestre de embarazo, se recomienda practicar un ultrasonido de la función renal y el cráneo. Se debe vigilar estrechamente a los lactantes cuyas madres hayan tomado ARAII (ver las secciones: Contraindicaciones; Advertencias y precauciones). Lactancia: Debido a que no se dispone de información sobre el uso de Valsartán durante la lactancia, no se recomienda administrar Valsartán, y es preferible administrar tratamientos alternativos con perfiles de seguridad mejor establecidos durante la lactancia, especialmente en recién nacidos o prematuros. Capacidad para realizar tareas que requieren discernimiento, habilidades motrices o cognitivas: No se han llevado a cabo estudios sobre los efectos en la capacidad para conducir. Al conducir u operar maquinaria, se debe tener en cuenta que, ocasionalmente, se pueden presentar mareos o cansancio.
Conservación.
Almacenar a temperaturas inferiores a 30°C. Vencimiento: La fecha de caducidad se indica en el envase. Uso y manejo: No hay requisitos especiales para el uso o el manejo de este producto. Incompatibilidades: No se dispone de datos relevantes.
Sobredosificación.
Síntomas y signos: La sobredosis con Valsartán es capaz de ocasionar una hipotensión manifiesta, que podría conducir a bajos niveles de conciencia, un colapso circulatorio y/o choque. Tratamiento: Las medidas terapéuticas dependen del momento de la ingestión y el tipo y la intensidad de los síntomas; la estabilización del estado circulatorio es de primordial importancia. Si se presenta hipotensión, se debe colocar al paciente en posición horizontal y se debe llevar a cabo una corrección del volumen sanguíneo. Es poco probable que Valsartán se elimine a través de hemodiálisis.
Presentación.
Blister de Alu/Alu. Comprimidos recubiertos 80 mg.
ALSARKARE
ETEX
160 mg
Antihipertensivo.
Composición.
ALSARKARE COMPRIMIDOS RECUBIERTOS 160 mg contiene: Valsartán 160 mg. Excipientes: Lactosa monohidratada, celulosa microcristalina, almidón de maíz, crospovidona, povidona, Dióxido de Silicio coloidal anhidro, estearato de magnesio, Instacoat universal (ICE-U-0115 amarillo[Hipromelosa, Macrogol, Dióxido de Titanio, Óxido de Hierro Rojo, Óxido de Hierro Negro, Óxido de Hierro Amarillo]) c.s.
Farmacología.
Farmacodinamia: Grupo farmacoterapéutico: Antagonistas de la angiotensina II, Código ATC: C09CA03. Mecanismo de acción: Efectos farmacodinámicos: Valsartán es un potente antagonista oral, activo y específico de los receptores de la angiotensina II (Ang II). Actúa selectivamente sobre el subtipo de receptor de AT1, que es responsable de las acciones conocidas de la angiotensina II. El aumento en las concentraciones plasmáticas de Ang II, tras un bloqueo del receptor de AT1 con Valsartán, podría estimular al receptor de AT2 no bloqueado, lo cual parece contrarrestar el efecto del receptor de AT1. Valsartán no exhibe ninguna actividad agonista parcial en el receptor de AT1, y tiene mucho mayor (aproximadamente 20.000 veces) afinidad por el receptor de AT1 que por el receptor de AT2. No se sabe si Valsartán se une o bloquea otros receptores hormonales o canales iónicos con importancia conocida en la regulación cardiovascular. Valsartán no inhibe la ECA (también conocida como cininasa II), que transforma la Ang I en Ang II y degrada la bradiquinina. Como no hay un efecto en la ECA, ni tampoco potenciación de bradiquinina o sustancia P, es poco probable que los antagonistas de la angiotensina II se asocien con tos. En estudios clínicos en los que se comparó Valsartán con un inhibidor de la ECA, la incidencia de tos seca fue significativamente menor (P < 0,05) en los pacientes tratados con Valsartán que en aquellos que recibieron un inhibidor de la ECA (2,6% frente a 7,9%, respectivamente). En un estudio clínico de pacientes con antecedentes de tos seca durante la terapia con algún inhibidor de la ECA, 19,5% de los sujetos del estudio que recibieron Valsartán y 19,0% de aquellos que recibieron algún diurético tiazídico experimentaron tos, en comparación con 68,5% de los sujetos tratados con algún inhibidor de la ECA (P < 0,05). Farmacocinética: Absorción: Tras la administración oral de Valsartán en monoterapia, las concentraciones plasmáticas máximas de Valsartán se alcanzan en un plazo de 2-4 horas con la formulación en comprimidos y de 1-2 horas con la formulación en solución. La biodisponibilidad absoluta media es de 23% y 39% con las formulaciones en tabletas y solución, respectivamente. Los alimentos disminuyen el nivel de exposición (medido por el ABC) a Valsartán en aproximadamente 40%, y su concentración plasmática máxima (Cmáx) en aproximadamente 50%, aunque a partir de aproximadamente 8 h después de su administración, las concentraciones plasmáticas de Valsartán son similares en los grupos postprandiales y en ayunas. Sin embargo, esta reducción en el ABC no se ve acompañada de una reducción clínicamente significativa en el efecto terapéutico, por lo cual Valsartán puede administrarse con o sin alimentos. Distribución: El volumen de distribución en estado estable de Valsartán tras su administración intravenosa es de aproximadamente 17 litros, lo cual indica que Valsartán no se distribuye ampliamente en los tejidos. Valsartán tiene un alto grado de unión a proteínas séricas (94-97%), principalmente a la albúmina sérica. Metabolismo: Valsartán no experimenta un alto grado de biotransformación, ya que sólo alrededor de 20% de la dosis se recupera en forma de metabolitos. Se ha identificado un metabolito hidroxi en el plasma a concentraciones bajas (menos de 10% del ABC de Valsartán). Este metabolito es farmacológicamente inactivo. Eliminación: Valsartán muestra una cinética de descomposición multiexponencial (t½a < 1 h y t½b aproximadamente 9 h). Valsartán se elimina principalmente mediante excreción biliar en las heces (aproximadamente 83% de la dosis) y por vía renal en la orina (aproximadamente 13% de la dosis), principalmente como fármaco inalterado. Tras su administración intravenosa, la depuración plasmática de Valsartán es de aproximadamente 2 L/h y su depuración renal es de 0,62 L/h (aproximadamente 30% de la depuración total). La vida media de Valsartán es de 6 horas. Poblaciones especiales de pacientes: Niños: En un estudio realizado en 26 pacientes pediátricos hipertensos (de 1 a 16 años de edad) que recibieron una dosis única de una suspensión de Valsartán (media: 0,9 a 2 mg/kg, con una dosis máxima de 80 mg), la depuración (litros/h/kg) de Valsartán fue similar en todo el rango de edad de 1 a 16 años, y a la de los adultos que recibieron la misma formulación. Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 mL/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Personas de edad avanzada: En algunos sujetos de edad avanzada, se observó una exposición sistémica a Valsartán algo mayor que en los sujetos jóvenes; sin embargo, no se ha demostrado que esto tenga alguna significancia clínica. Insuficiencia renal: Como era d
e esperarse de un compuesto cuya depuración renal representa sólo el 30% de la depuración plasmática total, no se observó correlación alguna entre la función renal y la exposición sistémica a Valsartán. Por lo tanto, no es necesario ajustar la dosis en pacientes con insuficiencia renal (depuración de creatinina > 10 mL/min). Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 mL/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. Valsartán tiene un alto grado de unión a proteínas plasmáticas, por lo cual es poco probable que se elimine a través de diálisis. Insuficiencia hepática: Aproximadamente 70% de la dosis absorbida se elimina en la bilis, fundamentalmente en forma inalterada. Valsartán no experimenta ninguna biotransformación notable. Se observó una duplicación de la exposición (ABC) en pacientes con insuficiencia hepática leve a moderada, en comparación con sujetos sanos. Sin embargo, no se observó correlación alguna entre la concentración plasmática de Valsartán y el grado de disfunción hepática. No se ha estudiado Valsartán en pacientes con disfunción hepática grave. Otras características de los pacientes: Pacientes con insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, el tiempo promedio para alcanzar la concentración máxima y la vida media de eliminación de Valsartán son similares a los observados en voluntarios sanos. Los valores de ABC y Cmáx de Valsartán casi son proporcionales al aumentar la dosis en el rango clínico de dosificación (40 a 160 mg administrados dos veces al día). El factor de acumulación promedio es de aproximadamente 1,7. La depuración aparente de Valsartán tras su administración oral es de aproximadamente 4,5 L/h. La edad no afecta la depuración aparente en pacientes con insuficiencia cardiaca. Información no clínica: Los datos pre-clínicos no revelaron riesgos especiales para los seres humanos, según los estudios convencionales de seguridad farmacológica, toxicidad de dosis repetidas, genotoxicidad y potencial carcinogénico. En ratas, la administración de dosis tóxicas para las madres (600 mg/kg/día) durante los últimos días de la gestación y la lactancia condujo a una menor supervivencia, un menor aumento en el peso y un retraso en el desarrollo (desprendimiento del pabellón auricular y apertura del canal auditivo) en la descendencia. Estas dosis administradas en ratas (600 mg/kg/día) son aproximadamente 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En estudios pre-clínicos de seguridad, las dosis elevadas de Valsartán (200 a 600 mg/kg de peso corporal) administradas en ratas ocasionaron una disminución de los parámetros de glóbulos rojos (eritrocitos, hemoglobina, hematocrito), así como indicios de cambios en la hemodinamia renal (ligero aumento en las concentraciones plasmáticas de urea, e hiperplasia tubular renal y basofilia en machos). Estas dosis administradas en ratas (200 y 600 mg/kg/día) son aproximadamente 6 y 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En monos tití que recibieron dosis similares, los cambios fueron semejantes aunque más graves, sobre todo en los riñones, donde los cambios evolucionaron a una nefropatía con aumentos en las concentraciones de urea y creatinina. En ambas especies, también se observó hipertrofia de las células renales yuxtaglomerulares. Se consideró que todos los cambios fueron ocasionados por la acción farmacológica de Valsartán, la cual produce hipotensión prolongada, especialmente en monos tití. En lo que respecta a las dosis terapéuticas de Valsartán en seres humanos, la hipertrofia de las células renales yuxtaglomerulares no parece tener relevancia alguna. Población pediátrica: La administración oral diaria de Valsartán a ratas recién nacidas/jóvenes (entre los 7 y 70 días de vida), a dosis tan bajas como 1 mg/kg/día (aproximadamente 10-35% de la dosis máxima recomendada para uso pediátrico de 4 mg/kg/día en forma de exposición sistémica) produjo un daño renal irreversible y persistente. Estos efectos previamente mencionados representan un efecto farmacológico exagerado ya esperado de los inhibidores de la enzima convertidora de angiotensina II y de los bloqueadores tipo I de la angiotensina II; esos efectos se observan al tratar a ratas durante los primeros 13 días de vida. Este periodo coincide con las 36 semanas de gestación en los seres humanos, que en ocasiones pueden extenderse hasta 44 semanas después de la concepción en seres humanos. En el estudio con Valsartán administrado a ratas jóvenes, las ratas recibieron dosis hasta el día 70, por lo cual no es posible excluir la existencia de efectos en la maduración renal (4-6 semanas después del parto). La maduración de la función renal es un proceso continuo que se presenta durante el primer año de vida en los seres humanos. Por consiguiente, no es posible excluir que esto tenga relevancia clínica en niños menores de 1 año de edad, mientras que por otro lado, los datos preclínicos no indican la existencia de un problema de seguridad en niños mayores de 1 año de edad.
Indicaciones.
Hipertensión: Tratamiento de la hipertensión. Insuficiencia cardiaca: Tratamiento de la insuficiencia cardiaca clase II-IV de la NYHA (New York Heart Association) en pacientes que estén recibiendo uno de los tratamientos habituales, como diuréticos, digitálicos y o bien, inhibidores de la enzima convertidora de angiotensina IECA o bien betabloqueadores pero no ambos; no es obligatorio que el paciente esté recibiendo todos estos tratamientos habituales. Post-infarto de miocardio (160 mg): ALSARKARE está indicado para mejorar la supervivencia después de un infarto de miocardio en pacientes clínicamente estables con síntomas, signos clínicos o signos radiológicos de insuficiencia ventricular izquierda o con disfunción sistólica del ventrículo izquierdo.
Dosificación.
Alsarkare puede administrarse de manera independiente a una comida, pero debe administrarse con agua. Vía de administración: Para uso oral. Adultos: Hipertensión: La dosis inicial recomendada de Valsartán consiste en 80 mg administrados una vez al día. El efecto antihipertensivo se presenta sustancialmente dentro del plazo de 2 semanas, y los efectos máximos se alcanzan en 4 semanas. En algunos pacientes cuya presión arterial no se encuentre controlada adecuadamente, se puede aumentar la dosis a 160 mg, y a un máximo de 320 mg. Valsartán también puede administrarse junto con otros agentes antihipertensivos. La adición de un diurético, como hidroclorotiazida, disminuirá aún más la presión arterial en estos pacientes. Infarto de miocardio reciente: En pacientes clínicamente estables, se puede iniciar la terapia desde 12 horas después de un infarto de miocardio. Después de administrar una dosis inicial de 20 mg dos veces al día, se debe ajustar la dosis de Valsartán a 40 mg, 80 mg y 160 mg dos veces al día durante las próximas semanas. La dosis inicial se suministra con el comprimido ranurado de 40 mg. La dosis máxima objetivo consiste en 160 mg administrados dos veces al día. En general, se recomienda que los pacientes alcancen un nivel posológico de 80 mg administrados dos veces al día hacia las dos semanas después de haber iniciado el tratamiento, y que la dosis máxima objetivo, de 160 mg administrados dos veces al día, sea alcanzada a los 3 meses según la tolerabilidad del paciente. Si se presenta una hipotensión sintomática o una disfunción renal, se debe contemplar una reducción de la dosis. Valsartán puede utilizarse en pacientes tratados con otras terapias administradas post-infarto de miocardio, como por ejemplo, trombolíticos, ácido acetilsalicílico, betabloqueantes, estatinas y diuréticos. No se recomienda la combinación con inhibidores de la ECA (Enzima convertidora de Angiotensina) (ver Advertencias y precauciones). La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. Insuficiencia cardiaca: La dosis inicial recomendada de Valsartán consiste en 40 mg administrados dos veces al día. El ajuste ascendente hasta 80 mg y 160 mg administrados dos veces al día debe hacerse a intervalos de cuando menos dos semanas a la dosis más alta, según la tolerabilidad del paciente. Se debe contemplar una reducción en la dosis de diuréticos concomitantes. La dosis diaria máxima administrada en estudios clínicos consiste en 320 mg en dosis divididas. Valsartán puede administrarse junto con otras terapias para insuficiencia cardiaca. Sin embargo, no se recomienda la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán (ver Advertencias y precauciones). La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. Niños: Niños y adolescentes de 6 a 18 años de edad: La dosis inicial consiste en 40 mg administrados una vez al día para niños que pesen menos de 35 kg, y de 80 mg administrados una vez al día para los niños que pesen 35 kg o más. Se debe ajustar la dosis según la respuesta de la presión arterial. Para conocer las dosis máximas estudiadas en estudios clínicos, consulte la siguiente tabla. No se han estudiado dosis más altas que las incluidas en el listado adjunto, por lo cual las mismas no se recomiendan.
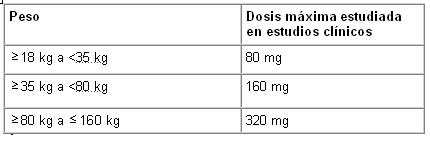
Niños menores de 6 años de edad: No se han establecido los perfiles de seguridad y eficacia de Valsartán en niños de 1 a 6 años de edad. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia renal: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia hepática: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis. Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg. Insuficiencia cardiaca e infarto de miocardio reciente en pacientes pediátricos: No se recomienda el uso de Valsartán en el tratamiento de la insuficiencia cardiaca o del infarto de miocardio reciente en niños y adolescentes menores de 18 años de edad, debido a la falta de datos sobre seguridad y eficacia. Personas de edad avanzada: No es necesario ajustar la dosis en personas de edad avanzada. Insuficiencia renal: No es necesario ajustar la dosis en pacientes con una depuración de creatinina > 10 ml/min (ver Advertencias y precauciones). Insuficiencia hepática: Valsartán está contraindicado en pacientes con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones; Advertencias y precauciones). En pacientes con insuficiencia hepática leve a moderada sin colestasis, la dosis de Valsartán no debe exceder 80 mg.
Contraindicaciones.
Valsartán está contraindicado en: Hipersensibilidad a la sustancia activa o a cualquiera de los excipientes. Insuficiencia hepática grave, cirrosis biliar y colestasis. El segundo y el tercer trimestre de embarazo (ver las secciones: Advertencias y precauciones; Embarazo y lactancia).
Reacciones adversas.
Datos de estudios clínicos y datos posteriores a la comercialización: En estudios clínicos controlados realizados en pacientes adultos con hipertensión, la incidencia global de reacciones adversas (RA) fue similar con el placebo y es consistente con el perfil farmacológico de Valsartán. La incidencia de RA no pareció relacionarse con la dosis o con la duración del tratamiento, ni tampoco mostró asociación alguna con el sexo, la edad o la raza. Se ha evaluado el efecto antihipertensivo de Valsartán en dos estudios clínicos aleatorizados, y doble ciegos que se realizaron en 561 pacientes pediátricos de 6 a 18 años de edad. Con la excepción de trastornos gastrointestinales aislados (como dolor abdominal, náuseas, vómito) y mareos, no se identificaron diferencias relevantes en cuanto al tipo, la frecuencia y la intensidad de las reacciones adversas entre el perfil de seguridad de los pacientes pediátricos de 6 a 18 años de edad, y las reacciones previamente reportadas en pacientes adultos. La evaluación neurocognitiva y del desarrollo de los pacientes pediátricos de 6 a 16 años de edad no reveló efectos adversos globales clínicamente relevantes después de administrar un tratamiento con Valsartán durante un máximo de un año. En un estudio aleatorizado, doble ciego y realizado en 90 niños de 1 a 6 años de edad, el cual fue seguido por un estudio abierto de extensión de un año de duración, se observaron dos muertes y casos aislados de aumentos manifiestos en las concentraciones de aminotransferasas hepáticas. Estos casos se produjeron en una población que presentaba comorbilidades significativas. No se ha establecido una relación causal con Valsartán. En un segundo estudio en el que se aleatorizó a 75 niños de 1 a 6 años de edad, no se presentaron aumentos significativos en las concentraciones de aminotransferasas hepáticas ni muertes al administrar el tratamiento con Valsartán. Los casos de hiperkalemia se observaron con mayor frecuencia en niños y adolescentes de 6 a 18 años de edad con nefropatía crónica subyacente. El perfil de seguridad observado en estudios clínicos controlados, que se realizaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca, varía del perfil global de seguridad observado en pacientes hipertensos. Esto puede relacionarse con la enfermedad subyacente de los pacientes. A continuación se enumeran las reacciones adversas que se presentaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca: A continuación se listan las reacciones adversas reportadas a partir de estudios clínicos, experiencia posterior a la comercialización y hallazgos de laboratorio, según su clase de sistema orgánico. Para todas las reacciones adversas reportadas a partir de la experiencia posterior a la comercialización y los hallazgos de laboratorio, no es posible aplicar cualquier frecuencia de reacciones adversas, por lo cual se mencionan con una frecuencia Desconocida. Las reacciones adversas se clasifican según su frecuencia utilizando la siguiente convención: Muy comunes ≥1/10. Comunes ≥1/100 a < 1/10. Poco comunes ≥1/1.000 a < 1/100. Raras ≥1/10000 a < 1/1.000. Muy raras < 1/10.000. Frecuencia desconocida (no se pueden estimar a partir de los datos disponibles). Hipertensión: Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: disminución en las concentraciones de hemoglobina, disminución de hematocrito, neutropenia, trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos vasculares: Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco común: dolor abdominal. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática, incluyendo un aumento en las concentraciones séricas de bilirrubina. Trastornos de la piel y el tejido subcutáneo: Frecuencia desconocida: angioedema, exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo: Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Frecuencia desconocida: insuficiencia y deterioro renal, aumento en las concentraciones séricas de creatinina. Trastornos generales y afecciones en el sitio de administración: Poco común: fatiga. Antecedentes recientes de infarto de miocardio y/o insuficiencia cardiaca (estudio realizado en pacientes adultos solamente): Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Poco común: hiperkalemia. Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del sistema nervioso: Comunes: mareos, vértigo postural. Poco comunes: síncope, cefalea. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos cardiacos: Poco común: insuficiencia cardíaca. Trastornos vasculares: Comunes: hipotensión, hipotensión ortostática. Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco comunes: náuseas, diarrea. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática. Trastornos de la piel y el tejido subcutáneo: Poco común: angioedema. Frecuencia desconocida: exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo: Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Comunes: insuficiencia y deterioro renal. Poco comunes: insuficiencia renal aguda, aumento en las concentraciones séricas de creatinina. Frecuencia desconocida: aumento en las concentraciones sanguíneas de nitrógeno ureico. Trastornos generales y afecciones en el sitio de administración: Poco comunes: astenia, fatiga.
Advertencias.
Hiperkalemia: No se recomienda el uso concomitante con complementos de potasio, diuréticos ahorradores de potasio, sustitutos de la sal que contengan potasio u otros agentes que puedan aumentar las concentraciones de potasio (heparina, etc.). Se debe instituir un seguimiento de las concentraciones de potasio, según sea necesario (ver Interacciones). Función renal deteriorada: Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 ml/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. No es necesario ajustar la dosis en pacientes adultos con una depuración de creatinina > 10 ml/min. Insuficiencia hepática: En pacientes con insuficiencia hepática leve a moderada sin colestasis, Valsartán debe utilizarse con precaución. Pacientes con depleción de sodio y/o volumen: En pacientes con una depleción grave de sodio y/o volumen, como aquellos que reciben dosis altas de diuréticos, se pueden presentar casos raros de hipotensión sintomática después de iniciar la terapia con Valsartán. Se debe corregir la depleción de sodio y/o volumen antes de iniciar el tratamiento con Valsartán, reduciendo por ejemplo la dosis de diuréticos. Estenosis de la arteria renal: En pacientes con estenosis bilateral de la arteria renal, o estenosis de un riñón único, no se ha establecido el uso seguro de Valsartán. La administración a corto plazo de Valsartán, a doce pacientes con hipertensión renovascular secundaria a una estenosis unilateral de la arteria renal, no indujo cambios significativos en la hemodinámica renal, la creatinina sérica o el nitrógeno ureico en sangre (BUN). Sin embargo, otros agentes que afectan al sistema de renina-angiotensina podrían aumentar las concentraciones sanguíneas de urea y las concentraciones séricas de creatinina en pacientes con estenosis unilateral de la arteria renal, por lo cual se recomienda instaurar un seguimiento de la función renal en los pacientes tratados con Valsartán. Trasplante renal: Actualmente no se tiene experiencia sobre el uso seguro de Valsartán en pacientes que se han sometido recientemente a un trasplante de riñón. Hiperaldosteronismo primario: Los pacientes con hiperaldosteronismo primario no deben recibir tratamiento con Valsartán, ya que su sistema de renina-angiotensina no se encuentra activado. Estenosis de la válvula aórtica y mitral, miocardiopatía hipertrófica obstructiva: Al igual que con otros vasodilatadores, se recomienda tener precaución especial en los pacientes que padezcan estenosis aórtica o mitral, o miocardiopatía hipertrófica obstructiva (HOCM). Embarazo: No se debe iniciar la administración de antagonistas de los receptores de la angiotensina II (ARAII) durante el embarazo. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alterna (ver Contraindicaciones; Embarazo y lactancia). Infarto de miocardio reciente: La combinación de Captopril y Valsartán no ha demostrado ningún beneficio clínico adicional, sino más bien aumentó el riesgo de desarrollar eventos adversos, en comparación con el tratamiento con sus respectivas monoterapias. Por lo tanto, no se recomienda la combinación de Valsartán con ningún inhibidor de la ECA. Se debe tener precaución al iniciar la terapia en pacientes con antecedentes recientes de infarto de miocardio. La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con antecedentes recientes de infarto de miocardio comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán no ha demostrado beneficio clínico alguno. Esta combinación aparentemente aumenta el riesgo de desarrollar eventos adversos, por lo cual no se recomienda. Se debe tener precaución al iniciar la terapia en pacientes con insuficiencia cardiaca. La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con insuficiencia cardiaca comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Otras afecciones con estimulación del sistema de renina-angiotensina: En aquellos pacientes cuya función renal pueda depender de la actividad del sistema de renina-angiotensina (por ejemplo, pacientes con insuficiencia cardiaca congestiva grave), el tratamiento con inhibidores de la enzima convertidora de angiotensina se ha asociado con el desarrollo de oliguria y/o azotemia progresiva y, en casos raros, con insuficiencia renal aguda y/o la muerte. Como Valsartán es un antagonista de la angiotensina II, no es posible excluir que el uso de Valsartán pueda asociarse con un deterioro de la función renal. Lactosa: El producto contiene lactosa. Los pacientes con problemas hereditarios poco usuales de intolerancia a la galactosa, insuficiencia de lactasa de Lapp o malabsorción de glucosa y galactosa, no deberán tomar este medicamento. Población pediátrica: Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio durante el tratamiento con Valsartán. En especial, esto se aplica cuando Valsartán se administra en presencia de otras afecciones (fiebre, deshidratación) que puedan deteriorar la función renal. Función hepática deteriorada: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones). Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg.
Interacciones.
No se recomienda el uso concomitante: Litio: Se han reportado aumentos reversibles en las concentraciones séricas de litio y toxicidad durante el uso concomitante de inhibidores de la ECA. Debido a la falta de experiencia sobre el uso concomitante de Valsartán y litio, no se recomienda esta combinación. Si fuera necesaria la combinación, se recomienda vigilar rigurosamente las concentraciones séricas de litio. Diuréticos ahorradores de potasio, complementos de potasio, sustitutos de la sal que contienen potasio y otras sustancias que pueden aumentar las concentraciones de potasio: Si se considera necesario administrar en combinación con Valsartán algún medicamento que afecte las concentraciones de potasio, se recomienda vigilar las concentraciones plasmáticas de potasio. Se requiere tener precaución con el uso concomitante de: Medicamentos antiinflamatorios no esteroideos (AINEs), incluyendo inhibidores selectivos de la COX-2, ácido acetilsalicílico > 3 g/día y AINEs no selectivos. Cuando los antagonistas de la angiotensina II se administran simultáneamente con AINEs, se puede presentar una atenuación del efecto antihipertensivo. Además, el uso concomitante de antagonistas de la angiotensina II y AINEs podría conducir a un mayor riesgo de experimentar un agravamiento de la función renal y un aumento en las concentraciones séricas de potasio. Por lo tanto, se recomienda vigilar la función renal al inicio del tratamiento e implementar una hidratación adecuada del paciente. Falta de interacciones: En estudios de interacción farmacológica realizados con Valsartán, no se han encontrado interacciones de significancia clínica con Valsartán o con cualquiera de las siguientes sustancias: cimetidina, warfarina, furosemida, digoxina, atenolol, indometacina, hidroclorotiazida, amlodipino, glibenclamida. Población pediátrica: En el tratamiento de la hipertensión en niños y adolescentes, donde las anormalidades renales subyacentes son comunes, se recomienda tener precaución con el uso concomitante de Valsartán y otras sustancias que inhiben el sistema de renina-angiotensina-aldosterona, ya que podría aumentar las concentraciones séricas de potasio. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Embarazo y lactancia: Fertilidad: Valsartán no produjo efectos adversos en el desempeño reproductivo de las ratas macho o hembra que recibieron dosis orales de hasta 200 mg/kg/día. Esta dosis equivale a 6 veces la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). Embarazo: No se recomienda el uso de antagonistas de los receptores de la angiotensina II (ARAII) durante el primer trimestre de embarazo (ver Advertencias y precauciones). El uso de ARAII se contraindica durante el segundo y el tercer trimestre de embarazo (ver Contraindicaciones; Advertencias y precauciones). La evidencia epidemiológica sobre el riesgo de teratogenicidad tras la exposición a inhibidores de la ECA durante el primer trimestre de embarazo no han sido concluyentes; sin embargo, no es posible descartar un pequeño aumento en el riesgo. Aunque no se dispone de datos epidemiológicos específicos sobre el riesgo de administrar ARAII, es posible que existan riesgos similares para esta clase de fármacos. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alternativa. Se sabe que la exposición a la terapia con AIIRA durante el segundo y el tercer trimestre induce fetotoxicidad humana (disminución de la función renal, oligohidramnios, retraso en la osificación del cráneo) y toxicidad neonatal (insuficiencia renal, hipotensión, e hiperkalemia). Si se ha producido una exposición a ARAII a partir del segundo trimestre de embarazo, se recomienda practicar un ultrasonido de la función renal y el cráneo. Se debe vigilar estrechamente a los lactantes cuyas madres hayan tomado ARAII (ver Contraindicaciones; Advertencias y precauciones). Lactancia: Debido a que no se dispone de información sobre el uso de Valsartán durante la lactancia, no se recomienda administrar Valsartán, y es preferible administrar tratamientos alternativos con perfiles de seguridad mejor establecidos durante la lactancia, especialmente en recién nacidos o prematuros. Capacidad para realizar tareas que requieren discernimiento, habilidades motrices o cognitivas. No se han llevado a cabo estudios sobre los efectos en la capacidad para conducir. Al conducir u operar maquinaria, se debe tener en cuenta que, ocasionalmente, se pueden presentar mareos o cansancio.
Conservación.
Almacenar a temperaturas inferiores a 30°C. Vencimiento: La fecha de caducidad se indica en el envase. Uso y manejo: No hay requisitos especiales para el uso o el manejo de este producto. Incompatibilidades: No se dispone de datos relevantes.
Sobredosificación.
Síntomas y signos: La sobredosis con Valsartán es capaz de ocasionar una hipotensión manifiesta, que podría conducir a bajos niveles de conciencia, un colapso circulatorio y/o choque. Tratamiento: Las medidas terapéuticas dependen del momento de la ingestión y el tipo y la intensidad de los síntomas; la estabilización del estado circulatorio es de primordial importancia. Si se presenta hipotensión, se debe colocar al paciente en posición horizontal y se debe llevar a cabo una corrección del volumen sanguíneo. Es poco probable que Valsartán se elimine a través de hemodiálisis.
Presentación.
Blister de Alu/Alu. Comprimidos recubiertos 160 mg.
ALSARKARE
ETEX
320 mg
Antihipertensivo.
Composición.
ALSARKARE COMPRIMIDOS RECUBIERTOS 320 mg contiene: Valsartán 320 mg. Excipientes: Lactosa monohidratada, celulosa microcristalina, almidón de maíz, crospovidona, povidona, Dióxido de Silicio coloidal anhidro, estearato de magnesio, Instacoat universal (ICE-U-0114 café [Hipromelosa, Macrogol, Dióxido de Titanio, Óxido de Hierro Rojo, Óxido de Hierro Negro, Óxido de Hierro Amarillo]) c.s.
Farmacología.
Farmacodinamia: Grupo farmacoterapéutico: Antagonistas de la angiotensina II, Código ATC: C09CA03. Mecanismo de acción: Efectos farmacodinámicos: Valsartán es un potente antagonista oral, activo y específico de los receptores de la angiotensina II (Ang II). Actúa selectivamente sobre el subtipo de receptor de AT1, que es responsable de las acciones conocidas de la angiotensina II. El aumento en las concentraciones plasmáticas de Ang II, tras un bloqueo del receptor de AT1 con Valsartán, podría estimular al receptor de AT2 no bloqueado, lo cual parece contrarrestar el efecto del receptor de AT1. Valsartán no exhibe ninguna actividad agonista parcial en el receptor de AT1, y tiene mucho mayor (aproximadamente 20.000 veces) afinidad por el receptor de AT1 que por el receptor de AT2. No se sabe si Valsartán se une o bloquea otros receptores hormonales o canales iónicos con importancia conocida en la regulación cardiovascular. Valsartán no inhibe la ECA (también conocida como cininasa II), que transforma la Ang I en Ang II y degrada la bradiquinina. Como no hay un efecto en la ECA, ni tampoco potenciación de bradiquinina o sustancia P, es poco probable que los antagonistas de la angiotensina II se asocien con tos. En estudios clínicos en los que se comparó Valsartán con un inhibidor de la ECA, la incidencia de tos seca fue significativamente menor (P < 0,05) en los pacientes tratados con Valsartán que en aquellos que recibieron un inhibidor de la ECA (2,6% frente a 7,9%, respectivamente). En un estudio clínico de pacientes con antecedentes de tos seca durante la terapia con algún inhibidor de la ACE, 19,5% de los sujetos del estudio que recibieron Valsartán y 19,0% de aquellos que recibieron algún diurético tiazídico experimentaron tos, en comparación con 68,5% de los sujetos tratados con algún inhibidor de la ECA (P < 0,05). Farmacocinética: Absorción: Tras la administración oral de Valsartán en monoterapia, las concentraciones plasmáticas máximas de Valsartán se alcanzan en un plazo de 2-4 horas con la formulación en comprimidos y de 1-2 horas con la formulación en solución. La biodisponibilidad absoluta media es de 23% y 39% con las formulaciones en tabletas y solución, respectivamente. Los alimentos disminuyen el nivel de exposición (medido por el ABC) a Valsartán en aproximadamente 40%, y su concentración plasmática máxima (Cmáx) en aproximadamente 50%, aunque a partir de aproximadamente 8 h después de su administración, las concentraciones plasmáticas de Valsartán son similares en los grupos postprandiales y en ayunas. Sin embargo, esta reducción en el ABC no se ve acompañada de una reducción clínicamente significativa en el efecto terapéutico, por lo cual Valsartán puede administrarse con o sin alimentos. Distribución: El volumen de distribución en estado estable de Valsartán tras su administración intravenosa es de aproximadamente 17 litros, lo cual indica que Valsartán no se distribuye ampliamente en los tejidos. Valsartán tiene un alto grado de unión a proteínas séricas (94-97%), principalmente a la albúmina sérica. Metabolismo: Valsartán no experimenta un alto grado de biotransformación, ya que sólo alrededor de 20% de la dosis se recupera en forma de metabolitos. Se ha identificado un metabolito hidroxi en el plasma a concentraciones bajas (menos de 10% del ABC de Valsartán). Este metabolito es farmacológicamente inactivo. Eliminación: Valsartán muestra una cinética de descomposición multiexponencial (t½a < 1 h y t½b aproximadamente 9 h). Valsartán se elimina principalmente mediante excreción biliar en las heces (aproximadamente 83% de la dosis) y por vía renal en la orina (aproximadamente 13% de la dosis), principalmente como fármaco inalterado. Tras su administración intravenosa, la depuración plasmática de Valsartán es de aproximadamente 2 L/h y su depuración renal es de 0,62 L/h (aproximadamente 30% de la depuración total). La vida media de Valsartán es de 6 horas. Poblaciones especiales de pacientes: Niños: En un estudio realizado en 26 pacientes pediátricos hipertensos (de 1 a 16 años de edad) que recibieron una dosis única de una suspensión de Valsartán (media: 0,9 a 2 mg/kg, con una dosis máxima de 80 mg), la depuración (litros/h/kg) de Valsartán fue similar en todo el rango de edad de 1 a 16 años, y a la de los adultos que recibieron la misma formulación. Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 mL/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Personas de edad avanzada: En algunos sujetos de edad avanzada, se observó una exposición sistémica a Valsartán algo mayor que en los sujetos jóvenes; sin embargo, no se ha demostrado que esto tenga alguna significancia clínica. Insuficiencia renal: Como era de esperarse de un compuesto cuya depuración renal representa sólo el 30% de la depuración plasmática total, no se observó correlación alguna entre la función renal y la exposición sistémica a Valsartán. Por lo tanto, no es necesario ajustar la dosis en pacientes con insuficiencia renal (depuración de creatinina > 10 mL/min). Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 mL/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. Valsartán tiene un alto grado de unión a proteínas plasmáticas, por lo cual es poco probable que se elimine a través de diálisis. Insuficiencia hepática: Aproximadamente 70% de la dosis absorbida se elimina en la bilis, fundamentalmente en forma inalterada. Valsartán no experimenta ninguna biotransformación notable. Se observó una duplicación de la exposición (ABC) en pacientes con insuficiencia hepática leve a moderada, en comparación con sujetos sanos. Sin embargo, no se observó correlación alguna entre la concentración plasmática de Valsartán y el grado de disfunción hepática. No se ha estudiado Valsartán en pacientes con disfunción hepática grave. Otras características de los pacientes: Pacientes con insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, el tiempo promedio para alcanzar la concentración máxima y la vida media de eliminación de Valsartán son similares a los observados en voluntarios sanos. Los valores de ABC y Cmáx de Valsartán casi son proporcionales al aumentar la dosis en el rango clínico de dosificación (40 a 160 mg administrados dos veces al día). El factor de acumulación promedio es de aproximadamente 1,7. La depuración aparente de Valsartán tras su administración oral es de aproximadamente 4,5 L/h. La edad no afecta la depuración aparente en pacientes con insuficiencia cardiaca. Información no clínica: Los datos pre-clínicos no revelaron riesgos especiales para los seres humanos, según los estudios convencionales de seguridad farmacológica, toxicidad de dosis repetidas, genotoxicidad y potencial carcinogénico. En ratas, la administración de dosis tóxicas para las madres (600 mg/kg/día) durante los últimos días de la gestación y la lactancia condujo a una menor supervivencia, un menor aumento en el peso y un retraso en el desarrollo (desprendimiento del pabellón auricular y apertura del canal auditivo) en la descendencia. Estas dosis administradas en ratas (600 mg/kg/día) son aproximadamente 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En estudios pre-clínicos de seguridad, las dosis elevadas de Valsartán (200 a 600 mg/kg de peso corp
oral) administradas en ratas ocasionaron una disminución de los parámetros de glóbulos rojos (eritrocitos, hemoglobina, hematocrito), así como indicios de cambios en la hemodinamia renal (ligero aumento en las concentraciones plasmáticas de urea, e hiperplasia tubular renal y basofilia en machos). Estas dosis administradas en ratas (200 y 600 mg/kg/día) son aproximadamente 6 y 18 veces mayores que la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). En monos tití que recibieron dosis similares, los cambios fueron semejantes aunque más graves, sobre todo en los riñones, donde los cambios evolucionaron a una nefropatía con aumentos en las concentraciones de urea y creatinina. En ambas especies, también se observó hipertrofia de las células renales yuxtaglomerulares. Se consideró que todos los cambios fueron ocasionados por la acción farmacológica de Valsartán, la cual produce hipotensión prolongada, especialmente en monos tití. En lo que respecta a las dosis terapéuticas de Valsartán en seres humanos, la hipertrofia de las células renales yuxtaglomerulares no parece tener relevancia alguna. Población pediátrica: La administración oral diaria de Valsartán a ratas recién nacidas/jóvenes (entre los 7 y 70 días de vida), a dosis tan bajas como 1 mg/kg/día (aproximadamente 10-35% de la dosis máxima recomendada para uso pediátrico de 4 mg/kg/día en forma de exposición sistémica) produjo un daño renal irreversible y persistente. Estos efectos previamente mencionados representan un efecto farmacológico exagerado ya esperado de los inhibidores de la enzima convertidora de angiotensina II y de los bloqueadores tipo I de la angiotensina II; esos efectos se observan al tratar a ratas durante los primeros 13 días de vida. Este periodo coincide con las 36 semanas de gestación en los seres humanos, que en ocasiones pueden extenderse hasta 44 semanas después de la concepción en seres humanos. En el estudio con Valsartán administrado a ratas jóvenes, las ratas recibieron dosis hasta el día 70, por lo cual no es posible excluir la existencia de efectos en la maduración renal (4-6 semanas después del parto). La maduración de la función renal es un proceso continuo que se presenta durante el primer año de vida en los seres humanos. Por consiguiente, no es posible excluir que esto tenga relevancia clínica en niños menores de 1 año de edad, mientras que por otro lado, los datos preclínicos no indican la existencia de un problema de seguridad en niños mayores de 1 año de edad.
Indicaciones.
Hipertensión: Tratamiento de la hipertensión. Insuficiencia cardiaca: Tratamiento de la insuficiencia cardiaca clase II-IV de la NYHA (New York Heart Association) en pacientes que estén recibiendo uno de los tratamientos habituales, como diuréticos, digitálicos y o bien, inhibidores de la enzima convertidora de angiotensina IECA o bien betabloqueadores pero no ambos; no es obligatorio que el paciente esté recibiendo todos estos tratamientos habituales. Post-infarto de miocardio (40, 80 y 160 mg): ALSARKARE está indicado para mejorar la supervivencia después de un infarto de miocardio en pacientes clínicamente estables con síntomas, signos clínicos o signos radiológicos de insuficiencia ventricular izquierda o con disfunción sistólica del ventrículo izquierdo.
Dosificación.
Alsarkare puede administrarse de manera independiente a una comida, pero debe administrarse con agua. Vía de administración: Para uso oral. Adultos: Hipertensión: La dosis inicial recomendada de Valsartán consiste en 80 mg administrados una vez al día. El efecto antihipertensivo se presenta sustancialmente dentro del plazo de 2 semanas, y los efectos máximos se alcanzan en 4 semanas. En algunos pacientes cuya presión arterial no se encuentre controlada adecuadamente, se puede aumentar la dosis a 160 mg, y a un máximo de 320 mg. Valsartán también puede administrarse junto con otros agentes antihipertensivos. La adición de un diurético, como hidroclorotiazida, disminuirá aún más la presión arterial en estos pacientes. Infarto de miocardio reciente: En pacientes clínicamente estables, se puede iniciar la terapia desde 12 horas después de un infarto de miocardio. Después de administrar una dosis inicial de 20 mg dos veces al día, se debe ajustar la dosis de Valsartán a 40 mg, 80 mg y 160 mg dos veces al día durante las próximas semanas. La dosis inicial se suministra con el comprimido ranurado de 40 mg. La dosis máxima objetivo consiste en 160 mg administrados dos veces al día. En general, se recomienda que los pacientes alcancen un nivel posológico de 80 mg administrados dos veces al día hacia las dos semanas después de haber iniciado el tratamiento, y que la dosis máxima objetivo, de 160 mg administrados dos veces al día, sea alcanzada a los 3 meses según la tolerabilidad del paciente. Si se presenta una hipotensión sintomática o una disfunción renal, se debe contemplar una reducción de la dosis. Valsartán puede utilizarse en pacientes tratados con otras terapias administradas post-infarto de miocardio, como por ejemplo, trombolíticos, ácido acetilsalicílico, betabloqueantes, estatinas y diuréticos. No se recomienda la combinación con inhibidores de la ECA (Enzima convertidora de Angiotensina) (ver Advertencias y precauciones). La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. Insuficiencia cardiaca: La dosis inicial recomendada de Valsartán consiste en 40 mg administrados dos veces al día. El ajuste ascendente hasta 80 mg y 160 mg administrados dos veces al día debe hacerse a intervalos de cuando menos dos semanas a la dosis más alta, según la tolerabilidad del paciente. Se debe contemplar una reducción en la dosis de diuréticos concomitantes. La dosis diaria máxima administrada en estudios clínicos consiste en 320 mg en dosis divididas. Valsartán puede administrarse junto con otras terapias para insuficiencia cardiaca. Sin embargo, no se recomienda la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán (ver Advertencias y precauciones). La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. Niños: Niños y adolescentes de 6 a 18 años de edad: La dosis inicial consiste en 40 mg administrados una vez al día para niños que pesen menos de 35 kg, y de 80 mg administrados una vez al día para los niños que pesen 35 kg o más. Se debe ajustar la dosis según la respuesta de la presión arterial. Para conocer las dosis máximas estudiadas en estudios clínicos, consulte la siguiente tabla. No se han estudiado dosis más altas que las incluidas en el listado adjunto, por lo cual las mismas no se recomiendan.
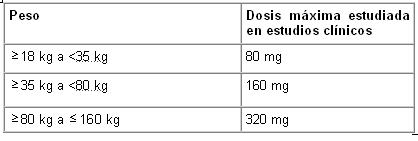
Niños menores de 6 años de edad: No se han establecido los perfiles de seguridad y eficacia de Valsartán en niños de 1 a 6 años de edad. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia renal: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Uso en pacientes pediátricos de 6 a 18 años de edad con insuficiencia hepática: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis. Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg. Insuficiencia cardiaca e infarto de miocardio reciente en pacientes pediátricos: No se recomienda el uso de Valsartán en el tratamiento de la insuficiencia cardiaca o del infarto de miocardio reciente en niños y adolescentes menores de 18 años de edad, debido a la falta de datos sobre seguridad y eficacia. Personas de edad avanzada: No es necesario ajustar la dosis en personas de edad avanzada. Insuficiencia renal: No es necesario ajustar la dosis en pacientes con una depuración de creatinina > 10 ml/min (ver Advertencias y precauciones). Insuficiencia hepática: Valsartán está contraindicado en pacientes con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones; Advertencias y precauciones). En pacientes con insuficiencia hepática leve a moderada sin colestasis, la dosis de Valsartán no debe exceder 80 mg.
Contraindicaciones.
Valsartán está contraindicado en: Hipersensibilidad a la sustancia activa o a cualquiera de los excipientes. Insuficiencia hepática grave, cirrosis biliar y colestasis. El segundo y el tercer trimestre de embarazo (ver las secciones: Advertencias y precauciones; Embarazo y lactancia).
Reacciones adversas.
Datos de estudios clínicos y datos posteriores a la comercialización: En estudios clínicos controlados realizados en pacientes adultos con hipertensión, la incidencia global de reacciones adversas (RA) fue similar con el placebo y es consistente con el perfil farmacológico de Valsartán. La incidencia de RA no pareció relacionarse con la dosis o con la duración del tratamiento, ni tampoco mostró asociación alguna con el sexo, la edad o la raza. Se ha evaluado el efecto antihipertensivo de Valsartán en dos estudios clínicos aleatorizados, y doble ciegos que se realizaron en 561 pacientes pediátricos de 6 a 18 años de edad. Con la excepción de trastornos gastrointestinales aislados (como dolor abdominal, náuseas, vómito) y mareos, no se identificaron diferencias relevantes en cuanto al tipo, la frecuencia y la intensidad de las reacciones adversas entre el perfil de seguridad de los pacientes pediátricos de 6 a 18 años de edad, y las reacciones previamente reportadas en pacientes adultos. La evaluación neurocognitiva y del desarrollo de los pacientes pediátricos de 6 a 16 años de edad no reveló efectos adversos globales clínicamente relevantes después de administrar un tratamiento con Valsartán durante un máximo de un año. En un estudio aleatorizado, doble ciego y realizado en 90 niños de 1 a 6 años de edad, el cual fue seguido por un estudio abierto de extensión de un año de duración, se observaron dos muertes y casos aislados de aumentos manifiestos en las concentraciones de aminotransferasas hepáticas. Estos casos se produjeron en una población que presentaba comorbilidades significativas. No se ha establecido una relación causal con Valsartán. En un segundo estudio en el que se aleatorizó a 75 niños de 1 a 6 años de edad, no se presentaron aumentos significativos en las concentraciones de aminotransferasas hepáticas ni muertes al administrar el tratamiento con Valsartán. Los casos de hiperkalemia se observaron con mayor frecuencia en niños y adolescentes de 6 a 18 años de edad con nefropatía crónica subyacente. El perfil de seguridad observado en estudios clínicos controlados, que se realizaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca, varía del perfil global de seguridad observado en pacientes hipertensos. Esto puede relacionarse con la enfermedad subyacente de los pacientes. A continuación se enumeran las reacciones adversas que se presentaron en pacientes con antecedentes recientes de infarto de miocardio y/o con insuficiencia cardiaca: A continuación se listan las reacciones adversas reportadas a partir de estudios clínicos, experiencia posterior a la comercialización y hallazgos de laboratorio, según su clase de sistema orgánico. Para todas las reacciones adversas reportadas a partir de la experiencia posterior a la comercialización y los hallazgos de laboratorio, no es posible aplicar cualquier frecuencia de reacciones adversas, por lo cual se mencionan con una frecuencia "desconocida". Las reacciones adversas se clasifican según su frecuencia utilizando la siguiente convención: Muy comunes ≥1/10. Comunes ≥1/100 a < 1/10. Poco comunes ≥1/1.000 a < 1/100. Raras ≥1/10000 a < 1/1.000. Muy raras < 1/10.000. Frecuencia desconocida (no se pueden estimar a partir de los datos disponibles). Hipertensión: Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: disminución en las concentraciones de hemoglobina, disminución de hematocrito, neutropenia, trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos vasculares: Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco común: dolor abdominal. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática, incluyendo un aumento en las concentraciones séricas de bilirrubina. Trastornos de la piel y el tejido subcutáneo: Frecuencia desconocida: angioedema, exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo: Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Frecuencia desconocida: insuficiencia y deterioro renal, aumento en las concentraciones séricas de creatinina. Trastornos generales y afecciones en el sitio de administración: Poco común: fatiga. Antecedentes recientes de infarto de miocardio y/o insuficiencia cardiaca (estudio realizado en pacientes adultos solamente): Trastornos sanguíneos y del sistema linfático: Frecuencia desconocida: trombocitopenia. Trastornos del sistema inmune: Frecuencia desconocida: hipersensibilidad, incluyendo enfermedad del suero. Trastornos metabólicos y nutricionales: Poco común: hiperkalemia. Frecuencia desconocida: aumento en las concentraciones séricas de potasio, hiponatremia. Trastornos del sistema nervioso: Comunes: mareos, vértigo postural. Poco comunes: síncope, cefalea. Trastornos del oído y el laberinto: Poco común: vértigo. Trastornos cardiacos: Poco común: insuficiencia cardíaca. Trastornos vasculares: Comunes: hipotensión, hipotensión ortostática. Frecuencia desconocida: vasculitis. Trastornos respiratorios, torácicos y mediastínicos: Poco común: tos. Trastornos gastrointestinales: Poco comunes: náuseas, diarrea. Trastornos hepatobiliares: Frecuencia desconocida: aumento en los valores de la función hepática. Trastornos de la piel y el tejido subcutáneo: Poco común: angioedema. Frecuencia desconocida: exantema, prurito. Trastornos musculoesqueléticos y del tejido conjuntivo: Frecuencia desconocida: mialgia. Trastornos renales y urinarios: Comunes: insuficiencia y deterioro renal. Poco comunes: insuficiencia renal aguda, aumento en las concentraciones séricas de creatinina. Frecuencia desconocida: aumento en las concentraciones sanguíneas de nitrógeno ureico. Trastornos generales y afecciones en el sitio de administración: Poco comunes: astenia, fatiga.
Advertencias.
Hiperkalemia: No se recomienda el uso concomitante con complementos de potasio, diuréticos ahorradores de potasio, sustitutos de la sal que contengan potasio u otros agentes que puedan aumentar las concentraciones de potasio (heparina, etc.). Se debe instituir un seguimiento de las concentraciones de potasio, según sea necesario (ver lInteracciones). Función renal deteriorada: Actualmente no se tiene experiencia sobre su uso seguro en pacientes con una depuración de creatinina < 10 ml/min, ni en pacientes sometidos a diálisis, por lo cual Valsartán debe utilizarse con precaución en estos pacientes. No es necesario ajustar la dosis en pacientes adultos con una depuración de creatinina > 10 ml/min. Insuficiencia hepática: En pacientes con insuficiencia hepática leve a moderada sin colestasis, Valsartán debe utilizarse con precaución. Pacientes con depleción de sodio y/o volumen: En pacientes con una depleción grave de sodio y/o volumen, como aquellos que reciben dosis altas de diuréticos, se pueden presentar casos raros de hipotensión sintomática después de iniciar la terapia con Valsartán. Se debe corregir la depleción de sodio y/o volumen antes de iniciar el tratamiento con Valsartán, reduciendo por ejemplo la dosis de diuréticos. Estenosis de la arteria renal: En pacientes con estenosis bilateral de la arteria renal, o estenosis de un riñón único, no se ha establecido el uso seguro de Valsartán. La administración a corto plazo de Valsartán, a doce pacientes con hipertensión renovascular secundaria a una estenosis unilateral de la arteria renal, no indujo cambios significativos en la hemodinámica renal, la creatinina sérica o el nitrógeno ureico en sangre (BUN). Sin embargo, otros agentes que afectan al sistema de renina-angiotensina podrían aumentar las concentraciones sanguíneas de urea y las concentraciones séricas de creatinina en pacientes con estenosis unilateral de la arteria renal, por lo cual se recomienda instaurar un seguimiento de la función renal en los pacientes tratados con Valsartán. Trasplante renal: Actualmente no se tiene experiencia sobre el uso seguro de Valsartán en pacientes que se han sometido recientemente a un trasplante de riñón. Hiperaldosteronismo primario: Los pacientes con hiperaldosteronismo primario no deben recibir tratamiento con Valsartán, ya que su sistema de renina-angiotensina no se encuentra activado. Estenosis de la válvula aórtica y mitral, miocardiopatía hipertrófica obstructiva: Al igual que con otros vasodilatadores, se recomienda tener precaución especial en los pacientes que padezcan estenosis aórtica o mitral, o miocardiopatía hipertrófica obstructiva (HOCM). Embarazo: No se debe iniciar la administración de antagonistas de los receptores de la angiotensina II (ARAII) durante el embarazo. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alterna (ver Contraindicaciones; Embarazo y lactancia). Infarto de miocardio reciente: La combinación de Captopril y Valsartán no ha demostrado ningún beneficio clínico adicional, sino más bien aumentó el riesgo de desarrollar eventos adversos, en comparación con el tratamiento con sus respectivas monoterapias. Por lo tanto, no se recomienda la combinación de Valsartán con ningún inhibidor de la ECA. Se debe tener precaución al iniciar la terapia en pacientes con antecedentes recientes de infarto de miocardio. La evaluación de pacientes con antecedentes recientes de infarto de miocardio siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con antecedentes recientes de infarto de miocardio comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Insuficiencia cardiaca: En pacientes con insuficiencia cardiaca, la combinación triple de un inhibidor de la ECA, un betabloqueante y Valsartán no ha demostrado beneficio clínico alguno. Esta combinación aparentemente aumenta el riesgo de desarrollar eventos adversos, por lo cual no se recomienda. Se debe tener precaución al iniciar la terapia en pacientes con insuficiencia cardiaca. La evaluación de pacientes con insuficiencia cardiaca siempre debe incluir una evaluación de la función renal. El uso de Valsartán en pacientes con insuficiencia cardiaca comúnmente ocasiona una reducción de la presión arterial, pero por lo general no es necesario suspender la terapia a causa de la hipotensión sintomática continua, siempre y cuando se sigan las instrucciones de dosificación. Otras afecciones con estimulación del sistema de renina-angiotensina: En aquellos pacientes cuya función renal pueda depender de la actividad del sistema de renina-angiotensina (por ejemplo, pacientes con insuficiencia cardiaca congestiva grave), el tratamiento con inhibidores de la enzima convertidora de angiotensina se ha asociado con el desarrollo de oliguria y/o azotemia progresiva y, en casos raros, con insuficiencia renal aguda y/o la muerte. Como Valsartán es un antagonista de la angiotensina II, no es posible excluir que el uso de Valsartán pueda asociarse con un deterioro de la función renal. Lactosa: El producto contiene lactosa. Los pacientes con problemas hereditarios poco usuales de intolerancia a la galactosa, insuficiencia de lactasa de Lapp o malabsorción de glucosa y galactosa, no deberán tomar este medicamento. Población pediátrica: Función renal deteriorada: No se ha estudiado su uso en pacientes pediátricos con una depuración de creatinina < 30 mL/min, ni en pacientes pediátricos sometidos a diálisis, por lo cual no se recomienda administrar Valsartán en estos pacientes. No es necesario ajustar la dosis en pacientes pediátricos con una depuración de creatinina > 30 ml/min. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio durante el tratamiento con Valsartán. En especial, esto se aplica cuando Valsartán se administra en presencia de otras afecciones (fiebre, deshidratación) que puedan deteriorar la función renal. Función hepática deteriorada: Al igual que en los adultos, Valsartán se contraindica en pacientes pediátricos con insuficiencia hepática grave, cirrosis biliar y en pacientes con colestasis (ver Contraindicaciones). Existe una experiencia clínica limitada con Valsartán en pacientes pediátricos con insuficiencia hepática leve a moderada. En estos pacientes, la dosis de Valsartán no debe exceder 80 mg.
Interacciones.
No se recomienda el uso concomitante: Litio: Se han reportado aumentos reversibles en las concentraciones séricas de litio y toxicidad durante el uso concomitante de inhibidores de la ECA. Debido a la falta de experiencia sobre el uso concomitante de Valsartán y litio, no se recomienda esta combinación. Si fuera necesaria la combinación, se recomienda vigilar rigurosamente las concentraciones séricas de litio. Diuréticos ahorradores de potasio, complementos de potasio, sustitutos de la sal que contienen potasio y otras sustancias que pueden aumentar las concentraciones de potasio: Si se considera necesario administrar en combinación con Valsartán algún medicamento que afecte las concentraciones de potasio, se recomienda vigilar las concentraciones plasmáticas de potasio. Se requiere tener precaución con el uso concomitante de: Medicamentos antiinflamatorios no esteroideos (AINEs), incluyendo inhibidores selectivos de la COX-2, ácido acetilsalicílico > 3 g/día y AINEs no selectivos: Cuando los antagonistas de la angiotensina II se administran simultáneamente con AINEs, se puede presentar una atenuación del efecto antihipertensivo. Además, el uso concomitante de antagonistas de la angiotensina II y AINEs podría conducir a un mayor riesgo de experimentar un agravamiento de la función renal y un aumento en las concentraciones séricas de potasio. Por lo tanto, se recomienda vigilar la función renal al inicio del tratamiento e implementar una hidratación adecuada del paciente. Falta de interacciones: En estudios de interacción farmacológica realizados con Valsartán, no se han encontrado interacciones de significancia clínica con Valsartán o con cualquiera de las siguientes sustancias: cimetidina, warfarina, furosemida, digoxina, atenolol, indometacina, hidroclorotiazida, amlodipino, glibenclamida. Población pediátrica: En el tratamiento de la hipertensión en niños y adolescentes, donde las anormalidades renales subyacentes son comunes, se recomienda tener precaución con el uso concomitante de Valsartán y otras sustancias que inhiben el sistema de renina-angiotensina-aldosterona, ya que podría aumentar las concentraciones séricas de potasio. Se debe vigilar estrechamente la función renal y las concentraciones séricas de potasio. Embarazo y lactancia: Fertilidad: Valsartán no produjo efectos adversos en el desempeño reproductivo de las ratas macho o hembra que recibieron dosis orales de hasta 200 mg/kg/día. Esta dosis equivale a 6 veces la dosis máxima recomendada en seres humanos en mg/m2 (los cálculos suponen una dosis oral de 320 mg/día y un paciente de 60 kg). Embarazo: No se recomienda el uso de antagonistas de los receptores de la angiotensina II (ARAII) durante el primer trimestre de embarazo (ver Advertencias y precauciones). El uso de ARAII se contraindica durante el segundo y el tercer trimestre de embarazo (ver Contraindicaciones; Advertencias y precauciones). La evidencia epidemiológica sobre el riesgo de teratogenicidad tras la exposición a inhibidores de la ECA durante el primer trimestre de embarazo no han sido concluyentes; sin embargo, no es posible descartar un pequeño aumento en el riesgo. Aunque no se dispone de datos epidemiológicos específicos sobre el riesgo de administrar ARAII, es posible que existan riesgos similares para esta clase de fármacos. A menos que se considere esencial la continuación de la terapia con ARAII, las pacientes que planeen embarazarse deben cambiarse a tratamientos antihipertensivos alternos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostique un embarazo, se deberá suspender inmediatamente el tratamiento con ARAII y, si es adecuado, iniciar una terapia alternativa. Se sabe que la exposición a la terapia con AIIRA durante el segundo y el tercer trimestre induce fetotoxicidad humana (disminución de la función renal, oligohidramnios, retraso en la osificación del cráneo) y toxicidad neonatal (insuficiencia renal, hipotensión, e hiperkalemia). Si se ha producido una exposición a ARAII a partir del segundo trimestre de embarazo, se recomienda practicar un ultrasonido de la función renal y el cráneo. Se debe vigilar estrechamente a los lactantes cuyas madres hayan tomado ARAII (ver Contraindicaciones; Advertencias y precauciones). Lactancia: Debido a que no se dispone de información sobre el uso de Valsartán durante la lactancia, no se recomienda administrar Valsartán, y es preferible administrar tratamientos alternativos con perfiles de seguridad mejor establecidos durante la lactancia, especialmente en recién nacidos o prematuros. Capacidad para realizar tareas que requieren discernimiento, habilidades motrices o cognitivas: No se han llevado a cabo estudios sobre los efectos en la capacidad para conducir. Al conducir u operar maquinaria, se debe tener en cuenta que, ocasionalmente, se pueden presentar mareos o cansancio.
Conservación.
Almacenar a temperaturas inferiores a 30°C. Vencimiento: La fecha de caducidad se indica en el envase. Uso y manejo: No hay requisitos especiales para el uso o el manejo de este producto. Incompatibilidades: No se dispone de datos relevantes.
Sobredosificación.
Síntomas y signos: La sobredosis con Valsartán es capaz de ocasionar una hipotensión manifiesta, que podría conducir a bajos niveles de conciencia, un colapso circulatorio y/o choque. Tratamiento: Las medidas terapéuticas dependen del momento de la ingestión y el tipo y la intensidad de los síntomas; la estabilización del estado circulatorio es de primordial importancia. Si se presenta hipotensión, se debe colocar al paciente en posición horizontal y se debe llevar a cabo una corrección del volumen sanguíneo. Es poco probable que Valsartán se elimine a través de hemodiálisis.
Presentación.
Blister de Alu/Alu. Comprimidos recubiertos 320 mg.
Laboratorio que comercializa Alsarkare
ETEX →

