KLARICID
ABBOTT
Comprimidos recubiertos Filmtab 250mg
Antibiótico.
Descripción.
Claritromicina es un antibiótico macrólido semi-sintético obtenido por substitución de un grupo CH3O para el grupo hidroxilo (OH) en posición 6 del anillo lactónico de la eritromicina. Específicamente la claritromicina es 6-O-metil eritromicina A. El antibiótico es un polvo blanco a blanquecino, prácticamente inodoro, esencialmente insoluble en agua y ligeramente soluble en etanol, metanol y acetonitrilo. Su peso molecular es 747,96.
Composición.
Cada comprimido recubierto contiene: Claritromicina 250 mg. Excipientes: Núcleo: Croscarmelosa sódica, almidón pregelatinizado, colorante amarillo D y C N°10, laca alumínica (quinolina), dióxido de silicio coloidal (silicagel), polividona, ácido esteárico, estearato de magnesio, talco, celulosa microcristalina (avicel PH-102), celulosa microcristalina (avicel PH-101). Recubrimiento: Hidroxipropilmetilcelulosa 15 cps, propilenglicol, monooleato de sorbitan, hidroxipropilcelulosa, dióxido de titanio, colorante amarillo quinilina laca, vainillina, ácido sórbico, Hidroxipropilmetilcelulosa 6 cps.
Farmacología.
Propiedades Farmacodinámicas: Microbiología: La claritromicina ejerce su acción antibacteriana ligándose a las sub-unidades ribosomales 50S de las bacterias susceptibles y suprimiendo la síntesis proteica. La claritromicina ha demostrado una excelente actividad in vitro, tanto contra las cepas estándar de bacterias como de aislados clínicos. Es altamente potente contra una amplia variedad de organismos aerobios y anaerobios Gram-positivos y Gram-negativos. Las concentraciones inhibitorias mínimas (CIMs) de claritromicina generalmente son una dilución log2 más potentes que las CIMs de eritromicina. Los datos in vitro también indican que la claritromicina tiene excelente actividad contra la Legionella pneumophila y Mycoplasma pneumoniae. Es bactericida para Helicobacter pylori; esta actividad de claritromicina es mayor en pH neutro que en pH ácido. Los datos in vitro e in vivo muestran que este antibiótico tiene actividad clínicamente significativa contra mycobacterias especies. Los datos in vitro indican que Enterobacteriaceae, pseudomonas especies y otros bacilos Gram-negativos no fermentadores de lactosa no son susceptibles a claritromicina. La claritromicina ha mostrado ser activa contra la mayoría de las cepas de los siguientes microorganismos tanto in vitro como en infecciones clínicas como se describe en la sección Indicaciones: Microorganismos Aerobios Gram-positivos: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes. Microorganismos Aerobios Gram-negativos: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis. Otros microorganismos: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR). Mycobacterias: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) que consisten en: Mycobacterium avium, Mycobacterium intracellulare. La producción de Beta-Lactamasa no debe tener efecto en la actividad de la claritromicina. Nota: La mayoría de las cepas de estafilococos resistentes a meticilina y oxacilina son resistentes a claritromicina. Helicobacter: Helicobacter pylori. En cultivos realizados previo a la terapia, se aisló H. pylori y se determinaron los CIMs de claritromicina pre-tratamiento en 104 pacientes. De estos, cuatro pacientes tenían cepas resistentes, dos pacientes tenían cepas con susceptibilidad intermedia y 98 pacientes tenían cepas susceptibles. Los siguientes datos in vitro están disponibles, pero su importancia clínica se desconoce. La claritromicina exhibe in vitro actividad contra la mayoría de las cepas de los siguientes microorganismos; sin embargo, la seguridad y efectividad de la claritromicina en el tratamiento de infecciones clínicas debido a estos microorganismos no se ha establecido en estudios clínicos adecuados y bien controlados. Microorganismos aerobios Gram-positivo: Streptococcus agalactiae, Streptococci (Grupo C, F, G), Streptococci grupo viridans. Microorganismos aerobios Gram-negativo: Bordetella pertussis, Pasteurella multocida. Microorganismo anaerobios Gram-positivo: Clostridium perfringens, Peptococcus niger, Propionibacterium acnes. Microorganismos anaerobios Gram-negativo: Bacteroides melaninogenicus. Spirochetes: Borrelia burgdorferi. Campylobacter: Campylobacter jejuni. El principal metabolito de claritromicina en el hombre y otros primates es un metabolito microbiológicamente activo, 14-OH-claritromicina. Este metabolito es tan activo o 1 a 2 veces menos activo que el compuesto padre para la mayoría de los organismos, excepto para H. Influenzae contra el cual es dos veces más activo. El compuesto padre y el 14-OH metabolito ejercen un efecto aditivo o sinergístico sobre H influenzae in vitro e in vivo, dependiendo de las cepas bacterianas. Se encontró que la claritromicma es dos a diez veces más activa que la eritromicina en varios modelos experimentales de infección animal. Se mostró, por ejemplo, ser más efectiva que la eritromicina en infección sistémica en ratón, absceso subcutáneo en ratón e infecciones del tracto respiratorio en ratón causadas por S. pneumoniae, S. aureus, S. pyogenes y H. influenzae. En cerdos de guinea con infección por Legionella, este efecto fue más pronunciado, una dosis intraperitoneal de 1,6 mg/kg/día de claritromicina fue más efectiva que 50 mg/kg/día de eritromicina. Pruebas de Susceptibilidad: Los métodos cuantitativos que requieren medición de los diámetros de zona dan los estimados más precisos de susceptibilidad de las bacterias a los agentes antimicrobianos. Un procedimiento recomendado utiliza discos impregnados con 15 mcg de claritromicina para la prueba de susceptibilidad (prueba de difusión Kirby-Bauer); las interpretaciones correlacionan los diámetros de la zona de inhibición de esta prueba de disco con los valores CIM para claritromicina. Las CIMs se determinan por método de dilución agar o caldo. Con estos procedimientos, un informe de laboratorio de "susceptible" indica que el organismo infectante probablemente responda a la terapia. Un informe de "resistente" indica que el organismo infectante probablemente no responda a la terapia. Un informe de "Susceptibilidad Intermedia" sugiere que el efecto terapéutico de la droga puede ser equívoco o que el organismo sería susceptible si se usan dosis más altas (susceptibilidad intermedia también se refiere a moderadamente susceptible). Propiedades Farmacocinéticas: La cinética de la claritromicina administrada oralmente se ha estudiado extensamente en muchas especies animales y humanos adultos. Estos estudios han mostrado que la claritromicina es inmediata y rápidamente absorbida con una biodisponibilidad absoluta de aproximadamente 50%. Se encontró una acumulación pequeña o no pronosticada y la disposición metabólica no cambió en ninguna de las especies que siguieron con dosificación múltiple. La ingesta de alimentos inmediatamente antes de la dosis aumenta la biodisponibilidad de la claritromicina en una media de 25%. En general, este aumento es menor y debe ser de poca importancia clínica con los regímenes de dosis recomendados. La claritromicina puede así ser administrada con o sin alimento. In vitro: Los estudios in vitro mostraron que la unión de la claritromicina a proteínas en el plasma humano promedió alrededor de 70% en concentraciones de 0,45 a 4,5 mcg/mL. Una disminución de la unión a 41 % en 45,0 mcg/mL sugirió que los sitios de unión pueden llegar a ser saturados, pero esto ocurrió solamente en concentraciones lejos en exceso de los niveles terapéuticos de la droga. In vivo: Resultados de estudios en animales mostraron que los niveles de claritromicina en todos los tejidos, excepto el sistema nervioso central, fueron varias veces más altos que los niveles de droga circulante. Las concentraciones más altas fueron usualmente encontradas en el hígado y pulmón donde las proporciones tejido a plasma (T/P) alcanzaron 10 a 20. Sujetos normales: Con dosis de 250 mg dos veces al día, el peak de la concentración plasmática estado estable se alcanzó en dos a tres días y promedió alrededor de 1 mcg/mL para claritromicina y 0,6 mcg/mL para 14-OH-claritromicina, mientras las vidas medias de eliminación de la droga padre y el metabolito fueron tres a cuatro horas y cinco a seis horas, respectivamente. Con dosis de 500 mg dos veces al día, el Cmáx estado estable para claritromicina y su metabolito hidroxilado se alcanzó con la quinta dosis. Después de la quinta y séptima dosis, el Cmáx estado estable para claritromicina promedió 2,7 y 2,9 mcg/mL; su metabolito hidroxilado promedió 0,88 y 0,83 mcg/mL, respectivamente. Con un nivel de dosis de 500 mg, la vida media de la droga padre fue 4,5 a 4,8 horas, mientras que la de 14-OH-claritromicina fue 6,9 a 8,7 horas. En estado estable, los niveles de la 14-OH-claritromicina no aumentaron proporcionalmente con la dosis de claritromicina y las vidas medias aparentes tanto de la claritromicina como de su metabolito hidroxilado tendieron a ser más largas con dosis más altas. Este comportamiento farmacocinético no lineal de la claritromicina, unido con la disminución general en la formación de productos 14-hidroxilados y N-demetilados en dosis más altas, indica que el metabolismo no lineal de la claritromicina llega a ser más pronunciado en dosis altas. En humanos adultos a quienes se da una dosis oral única de 250 mg o 1200 mg de claritromicina, la excreción urinaria se encargó del 37,9% de la dosis más baja y 46,0% de la dosis más alta. La eliminación fecal se encargó del 40,2% y 29,1 % (esto incluyó un sujeto con sólo una muestra de deposición que contenía 14,1 %) de estas respectivas dosis. Pacientes: La claritromicina y su 14-OH-metabolito se distribuyen rápidamente en los tejidos y fluidos del cuerpo. Datos limitados de un pequeño número de pacientes sugieren que la claritromicina no alcanza niveles significativos en el fluido cerebroespinal (CSF) después de dosis orales (por ej. sólo 1 a 2% de los niveles séricos en CSF en pacientes con barreras CSF-sangre normales). Las concentraciones en los tejidos son usualmente varias veces más altas que las concentraciones séricas. Ejemplos de concentraciones de tejido y suero se presentan a continuación.

Deterioro Hepático: En un estudio que comparó un grupo de sujetos humanos sanos con un grupo de sujetos con deterioro del hígado a quienes se les dio 250 mg de claritromicina dos veces al día, por dos días y una dosis única de 250 mg al tercer día, los niveles plasmáticos estado estable y el clearing sistémico de claritromicina no fueron significativamente diferentes entre los dos grupos. En contraste, las concentraciones estado estable del 14-OH-metabolito fueron marcadamente más bajas en el grupo de sujetos con deterioro hepático. Este clearance metabólico disminuido del compuesto padre por 14-hidroxilación estuvo parcialmente alterado por un aumento en el clearance renal de la droga padre, provocando niveles estado estable de la droga padre comparables en sujetos sanos y con deterioro hepático. Estos resultados indican que no es necesario un ajuste de dosis en sujetos con deterioro hepático moderado o severo con función renal normal. Deterioro Renal: Se condujo un estudio para evaluar y comparar el perfil farmacocinético de múltiples dosis orales de 500 mg de claritromicina en sujetos con función renal normal y disminuida. Los niveles plasmáticos, vida media, Cmáx y Cmín tanto para claritromicina como para su 14-OH-metabolito fueron más altos y el ABC fue más amplio en sujetos con deterioro renal. Excreción urinaria y Kelim fueron más bajas. El alcance con el cual estos parámetros difirieron se correlacionó con el grado de deterioro renal; mientras más severo el deterioro renal, más significativa la diferencia (ver Dosificación). Sujetos mayores: También se condujo un estudio para evaluar y comparar la seguridad y perfiles farmacocinéticos de múltiples dosis orales de 500 mg de claritromicina en hombres y mujeres mayores sanos con aquellos sujetos hombres adultos jóvenes sanos. En el grupo de mayores, los niveles plasmáticos circulantes fueron más altos y la eliminación más lenta que en el grupo más joven tanto para la droga padre como para el 14-OH-metabolito. Sin embargo, no hubo diferencia entre los dos grupos cuando el clearance renal se correlacionó con el clearance de creatinina. De aquellos resultados se concluyó que ningún efecto en el manejo de claritromicina se relaciona con la función renal ni con la edad per se. Infecciones por Mycobacterium avium: Las concentraciones estado estable de claritromicina y 14-OH-claritromicina observadas después de la administración de dosis de 500 mg de claritromicina cada 12 horas a pacientes adultos con infección por VIH fueron similares a aquellas observadas en sujetos normales. Sin embargo, en dosis más altas que se pueden requerir para tratar infecciones por Mycobacterium avium, las concentraciones de claritromicina fueron mucho más altas que aquellas observadas en las dosis usuales. En pacientes adultos infectados con VIH que toman 1000 y 2000 mg/día en dosis divididas en dos, los valores estado estable de Cmáx de claritromicina variaron desde 2 a 4 mcg/mL y 5 a 10 mcg/mL, respectivamente. Las vidas medias de eliminación parecieron ser más largas con estas dosis más altas en comparación con aquellas observadas con dosis usuales en sujetos normales. Las concentraciones plasmáticas más altas y las vidas medias de eliminación observadas con estas dosis son consistentes con la conocida no linealidad de la farmacocinética de claritromicina. Administración Concomitante de Omeprazol: Se condujo un estudio farmacocinético con claritromicina 500 mg tres veces al día y omeprazol 40 mg una vez al día. Cuando la claritromicina se administró sola en dosis de 500 mg cada ocho horas, el valor medio estado estable de Cmáx fue aproximadamente 3,8 mcg/mL y el valor medio estado estable de Cmín fue aproximadamente 1,8 mcg/mL. La media de ABC0-8 para claritromicina fue 22,9 mcg/hr/mL. La Tmáx y la vida media fueron 2,1 hr y 5,3 hr, respectivamente, cuando la claritromicina se dosificó en 500 mg tres veces al día. En el mismo estudio cuando se administró claritromicina 500 mg tres veces al día con omeprazol 40 mg una vez al día, se observaron aumentos en la vida media y el ABC0-24 de omeprazol. Para todos los sujetos combinados, la media AUC0-24 de omeprazol fue 89% mayor y la media armónica para el T½ de omeprazol fue 34% mayor cuando el omeprazol se administró con claritromicina que cuando se administró solo. Cuando la claritromicina se administró con omeprazol, el estado estable de Cmáx, Cmín y AUC0-8 de claritromicina se aumentaron en 10%, 27% y 15%, respectivamente, sobre los valores alcanzados cuando la claritromicina se administró con placebo. En estado estable, las concentraciones en la mucosa gástrica de claritromicina seis horas después de la dosis fueron aproximadamente 25 veces más altas en el grupo claritromicina/omeprazol comparado con el grupo claritromicina sola. Seis horas después de la dosis, la media de las concentraciones en el tejido gástrico de claritromicina fueron aproximadamente 2 veces más altas cuando la claritromicina se administró con omeprazol que cuando la claritromicina se administró con placebo. Datos de seguridad pre-clínica: Toxicidad Aguda, Subcrónica y Crónica: Se realizaron estudios en ratones, ratas, perros y/o monos con claritromicina administrada oralmente. La duración de la administración variaron de una dosis oral única a administración oral repetida diariamente por seis meses consecutivos. En estudios agudos en ratones y ratas, una rata, pero no ratón, murió después de un gavage único de 5 g/kg de peso corporal. La dosis letal media, por lo tanto, fue mayor de 5 g/kg, la dosis de administración más alta aceptable. No se atribuyeron efectos adversos a claritromicina en primates expuestos a 100 mg/kg/día durante 14 días consecutivos o a 35 mg/kg/día durante un mes. Igualmente, no se observaron efectos adversos en ratas expuestas a 75 mg/kg/día durante un mes, a 35 mg/kg/día durante tres meses, o a 8 mg/kg/día por seis meses. Los perros fueron más sensibles a la claritromicina, tolerando 50 mg/kg/día durante 14 días, 10 mg/kg/día por uno y tres meses y 4 mg/kg/día por seis meses sin efectos adversos. Los principales signos clínicos en dosis tóxicas en estos estudios descritos anteriormente, incluyeron emesis, debilidad, reducido consumo alimenticio y reducida ganancia de peso, salivación, deshidratación e hiperactividad. Dos de diez monos que recibieron 400 mg/kg/día murieron en el día 8 de tratamiento; heces amarillas decoloradas se observaron en pocas ocasiones aisladas en algunos monos sobrevivientes a quienes se administró una dosis de 400 mg/kg/día durante 28 días. El primer órgano objetivo en dosis tóxicas en todas las especies fue el hígado. El desarrollo de hepatoxicidad en todas las especies fue detectable por elevación temprana de las concentraciones séricas de fosfatasa alcalina, alanina y aspartato aminotransferasa, gama-glutamil transferasa, y/o dehidrogenasa láctica. La discontinuación de la droga, generalmente produjo un retorno o acercamiento a las concentraciones normales de estos parámetros específicos. Tejidos adicionales comúnmente menos afectados en los diversos estudios incluyeron el estómago, timo y otros tejidos linfáticos, y los riñones. El lagrimeo e inyección conjuntival después de dosis cercanas a las terapéuticas, ocurrieron sólo en perros. Con una dosis masiva de 400 mg/kg/día, algunos perros y monos desarrollaron opacidad corneal y/o edema. Fertilidad, Reproducción y Teratogenicidad: Los estudios sobre fertilidad y reproducción han mostrado que dosis diarias de 150 a 160 mg/kg/día en ratas hembras y machos no causaron efectos adversos en el ciclo menstrual, fertilidad, parto y número y viabilidad de la descendencia. Dos estudios de teratogenicidad en ratas Wistar (p.o) y Sprague-Dawley (p.o. e i.v.), un estudio con conejos blancos en Nueva Zelanda y un estudio con monos cinomolgus fallaron para demostrar alguna teratogenicidad de claritromicina. Sólo en un estudio adicional con ratas Sprague-Dawley en dosis similares y esencialmente en condiciones similares ocurrió una incidencia muy baja, estadísticamente insignificante (aproximadamente 6%) de anomalías cardiovasculares. Estas anomalías parecieron ser debidas a expresión espontánea de cambios genéticos dentro de la colonia. Dos estudios en ratones también revelaron una incidencia variable de fisura palatina (3 a 30%) después de dosis 70 veces el rango superior de la dosis usual diaria clínica humana (500 mg dos veces al día), pero no en 35 veces la dosis máxima diaria clínica humana, sugiriendo toxicidad maternal y fetal pero no teratogenicidad. Se ha mostrado que la claritromicina produce pérdida embriónica en monos cuando se administra en aproximadamente diez veces el rango superior de la dosis humana diaria usual (500 mg dos veces al día), comenzando en el día 20 de gestación. Este efecto se ha atribuido a la toxicidad maternal de la droga en dosis muy altas. Un estudio adicional en monos hembras preñadas con dosis de aproximadamente 2,5 a 5 veces la dosis diaria máxima entregada no produjo ningún riesgo a la cría. Un test letal dominante en ratones con dosis de 1000 mg/kg/día (aproximadamente 70 veces la dosis clínica máxima diaria humana) fue claramente negativo para cualquier actividad mutagénica y en un estudio de ratas Segmento 1 tratadas con hasta 500 mg/kg/día (aproximadamente 35 veces la dosis clínica máxima diaria humana) durante 80 días, no se mostró evidencia de deterioro funcional de la fertilidad masculina debido al largo período de exposición a estas dosis muy altas de claritromicina. Mutagenicidad: Los estudios para evaluar el potencial mutagénico de claritromicina se realizaron usando tanto sistemas de prueba con microsomas de hígado de rata no activados como no activados (Test de Ames). Los resultados de estos estudios no proporcionaron evidencia de potencial mutagénico en las concentraciones de droga de 25 mcg/placa de Petri o menos. En una concentración de 50 mcg, la droga fue tóxica para todas las cepas testeadas. Estudios clínicos: El Helicobacter pylori se asocia fuertemente con la enfermedad de úlcera péptica. Noventa (90) a 100% de los pacientes con úlceras duodenales está infectado con este patógeno. La erradicación del H. pylori se ha mostrado que reduce la tasa de recurrencia de úlcera duodenal, por consiguiente reduciendo la necesidad de terapia de mantención anti-secretoria. Triple Terapia en Ulcera Duodenal: En un estudio doble ciego bien controlado, pacientes con úlcera duodenal infectados con H. pylori recibieron triple terapia con 500 mg de claritromicina dos veces al día, amoxicilina 1000 mg dos veces al día y omeprazol 20 mg al día, durante diez días. El H. pylori fue erradicado en 90% de los pacientes que recibieron claritromicina triple terapia y en 60% de los pacientes que recibieron terapia dual. En un estudio independiente en pacientes infectados con H. pylori que recibieron terapia de erradicación con claritromicina 500 mg dos veces al día en conjunto con amoxicilina 1000 mg dos veces al día y omeprazol 20 mg al día (Grupo A) u omeprazol 20 mg dos veces al día (Grupo B) por siete días. En aquellos pacientes no tratados previamente con terapia anti-H. pylori, el H. pylori fue erradicado en 88% de los pacientes en el Grupo A y 86% de los pacientes en el grupo B. En un estudio abierto en pacientes infectados con H. pylori con úlcera duodenal o dispepsia no ulcerosa (NUD) recibieron terapia de erradicación con claritromicina 500 mg dos veces al día, lansoprazol 30 mg dos veces al día, más amoxicilina 1000 mg dos veces al día, durante diez días. En un análisis de todos los pacientes tratados, el H. pylori fue erradicado en 91 % de los pacientes. Terapia Dual en Ulcera Duodenal: En estudios doble ciego, bien controlados, pacientes con úlcera duodenal infectados con H. pylori recibieron terapia de erradicación con claritromicina 500 mg tres veces al día y omeprazol 40 mg diariamente, durante 14 días, seguido por omeprazol 40 mg (estudio A) u omeprazol 20 mg (estudios B, C y D) diariamente por un adicional de 14 días; los pacientes en cada grupo control recibieron omeprazol solo por 28 días. En el estudio A, el H. pylori se erradicó por sobre el 80% de los pacientes que recibieron claritromicina y omeprazol y en sólo 1 % de los pacientes que recibieron omeprazol solo. En los estudios B, C, y D, la tasa de erradicación combinada fue sobre el 70% de los pacientes que recibieron claritromicina y omeprazol y menos del 1 % en pacientes que recibieron omeprazol solo. En cada estudio, la tasa de recurrencia de úlcera a los seis meses fue estadísticamente más baja en pacientes tratados con claritromicina y omeprazol comparado con pacientes que recibieron omeprazol solo. En un estudio investigador-ciego, los pacientes infectados con H. pylori recibieron terapia de erradicación con claritromicina 500 mg tres veces al día, en conjunto con lansoprazol 60 mg/día en dosis única o dividida, durante 14 días. La tasa de erradicación combinada fue sobre 60%.
Indicaciones.
La claritromicina está indicada para el tratamiento de infecciones debidas a organismos susceptibles. Tales infecciones incluyen: Infecciones del tracto respiratorio inferior (ej. bronquitis, pneumonía; Infecciones del tracto respiratorio superior (ej. faringitis, sinusitis); Infecciones de la piel y tejidos blandos (ej. foliculitis, celulitis, erisipelas; Infecciones micobacterianas localizadas o diseminadas debido a Mycobacterium avium o Mycobacterium intracellulare. Infecciones localizadas debido a Mycobacterium chelonae, Mycobacterium fortuitum o Mycobacterium kansasii; La claritromicina está indicada para la prevención de infección diseminada por Mycobacterium avium complex en pacientes infectados con VIH con conteo de linfocito CD4 menor o igual a 100/mm3; Claritromicina en presencia de supresión ácida también está indicada para la erradicación de H. pylori produciendo una disminución de la recurrencia de úlcera duodenal (ver Estudios clínicos).
Dosificación.
La dosis usual recomendada de claritromicina en adultos es de un comprimido de 250 mg dos veces al día. En infecciones más severas, la dosis puede ser aumentada a 500 mg dos veces al día. La duración usual de la terapia es de 6 a 14 días. En pacientes con deterioro renal con clearance de creatinina menos de 30 mL/min, la dosis de claritromicina se debe reducir a la mitad, por ej., 250 mg una vez al día, o 250 mg dos veces al día en las infecciones más severas. El tratamiento no se debe prolongar más allá de 14 días en estos pacientes. Dosis en pacientes con infecciones mycobacterianas: La dosis recomendada para adultos con infecciones mycobacterianas es 500 mg dos veces al día. El tratamiento de infecciones diseminadas MAC en pacientes con SIDA se debe continuar tanto tiempo hasta se demuestre beneficio clínico y microbiológico. La claritromicina se debe usar en conjunto con otros agentes antimycobacterianos. El tratamiento de otras infecciones mycobacterianas no-tuberculosas se debe continuar según el criterio del médico. Dosis para profilaxis MAC: La dosis recomendada de claritromicina en adultos es 500 mg dos veces al día. Para la erradicación de H. pylori, los regímenes de dosis recomendada son: Régimen Triple Terapia: Claritromicina 500 mg dos veces al día en conjunto con lansoprazol 30 mg dos veces al día, más amoxicilina 1000 mg dos veces al día, por diez días. Claritromicina 500 mg dos veces al día en conjunto con amoxicilina 1000 mg dos veces al día y omeprazol 20 mg dos veces al día, por siete a diez días. Regímenes Terapia Dual: Claritromicina 500 mg tres veces al día en conjunto con omeprazol 40 mg diarios por 14 días, seguido por omeprazol 20 mg o 40 mg diarios por un adicional de 14 días. Claritromicina 500 mg tres veces al día en conjunto con lansoprazol 60 mg diarios por 14 días. Más allá se puede requerir supresión ácida para completar la cicatrización de la úlcera.
Contraindicaciones.
La claritromicina está contraindicada en pacientes con conocida hipersensibilidad a los antibióticos macrólidos. La administración concomitante de claritromicina y cualquiera de las siguientes drogas está contraindicada: astemizol, cisaprida, pimozida, terfenadina y ergotamina o dihidroergotamina (ver Interacciones).
Reacciones adversas.
El perfil de seguridad de la formulación pediátrica es similar a la del comprimido de 250 mg en pacientes adultos. La Tabla 1 muestra los eventos adversos reportados en pacientes que tomaron claritromicina en estudios clínicos. Los eventos adversos de muestran por sistema corporal y frecuencia (común ≥1/100, < 1/10).
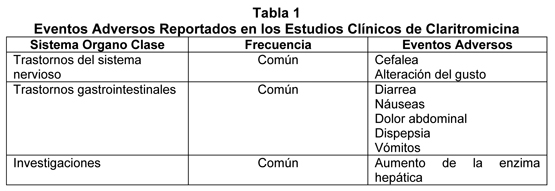
Experiencia Post-Comercialización: La claritromicina se comercializa en varias formulaciones diferentes. La Tabla 2 es una compilación de reacciones adversas para todas las formulaciones incluyendo claritromicina suspensión pediátrica. Debido a que estas reacciones se reportan voluntariamente desde una población de tamaño incierto, no siempre es posible estimar realmente su frecuencia o establecer una relación causal a la exposición a la droga. La exposición de paciente se estima ser mayor a 1 billón de días de tratamiento paciente para claritromicina.
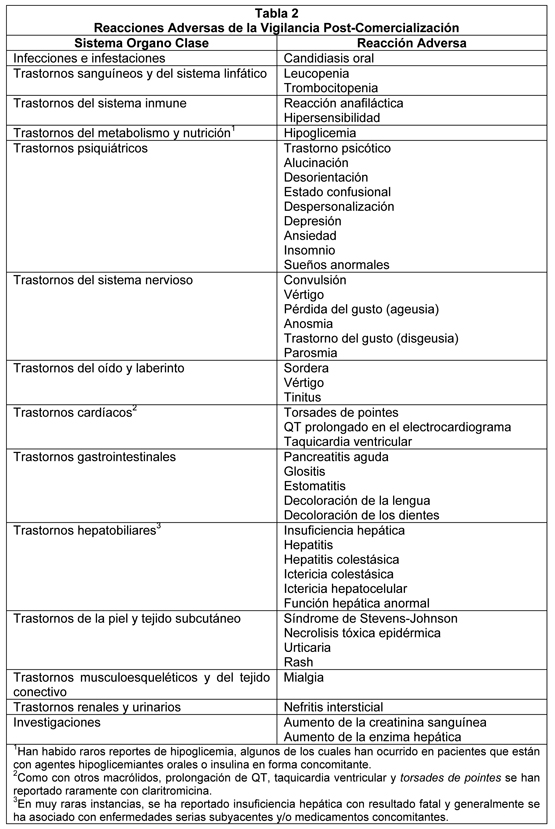
Han habido informes post-comercialización de toxicidad de la colchicina con uso concomitante de claritromicina y colchicina, especialmente en los ancianos, algunos de los cuales ocurrieron en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones: Colchicina y Advertencias). Pacientes Inmunocomprometidos: En pacientes con SIDA y otros inmunocomprometidos tratados con la más alta dosis de claritromicina por largos períodos de tiempo por infecciones micobacterianas, a menudo fue difícil distinguir eventos adversos posiblemente asociados con la administración de claritromicina de signos subyacentes a la enfermedad por VIH o enfermedad intercurrente. En pacientes adultos, los eventos adversos más frecuentemente informados por pacientes tratados con dosis diarias totales de 1000 mg de claritromicina fueron: náuseas, vómitos, alteración del gusto, dolor abdominal, diarrea, rash, flatulencia, cefalea, constipación, trastornos de audición, elevaciones de SGOT y SGPT. Eventos adicionales de baja frecuencia incluyeron disnea, insomnio y boca seca. En estos pacientes inmuno comprometidos las evaluaciones de los valores de laboratorio se realizaron analizando aquellos valores fuera del nivel seriamente anormal (por ej. el extremo alto o el límite bajo) para el test específico. Sobre las bases de este criterio, alrededor de 2% a 3% de estos pacientes que recibieron 1000 mg de claritromicina diariamente tuvieron niveles elevados de SGOT y SGTP seriamente anormales y glóbulos blancos y recuento de plaquetas anormalmente bajos. Un menor porcentaje de pacientes también tenía niveles elevados del BUN.
Advertencias.
El médico no debe prescribir claritromicina a mujeres embarazadas sin evaluar cuidadosamente los beneficios frente al riesgo, especialmente durante los tres primeros meses de embarazo. Claritromicina no debería ser usada en mujeres embarazadas excepto en cuadros clínicos en los que no exista terapia alternativa apropiada. Si el embarazo ocurre durante el tratamiento, el paciente debería ser informado del potencial daño al feto. Claritromicina ha demostrado efectos adversos en el embarazo y/o desarrollo embriofetal en monos, ratas, ratones y conejos a dosis que producen niveles plasmáticos 2 a 17 veces los niveles plasmáticos alcanzados en humanos tratados con las dosis máximas recomendadas. El uso a largo plazo, como con otros antibióticos, produce colonización con números aumentados de bacterias y hongos no susceptibles. Si ocurren superinfecciones, se debe instituir una terapia apropiada. Se ha reportado colitis pseudomembranosa con prácticamente todos los agentes antibacterianos, incluyendo macrólidos y puede variar desde leve hasta con riesgo vital. Se ha reportado diarrea asociada a Clostridium difficile (CDAD) con el uso de prácticamente todos los agentes antimicrobianos incluyendo claritromicina, y puede variar en severidad desde diarrea leve a colitis fatal. El tratamiento con agentes antibacterianos alteran la flora normal del colon, el cual puede llevar a un sobrecrecimiento de C. difficile. El CDAD se debe considerar en todos los pacientes que presentan diarrea después del uso de antibióticos. Es necesario una historia médica cuidadosa ya que CDAD se ha reportado que ocurre sobre dos meses después de la administración de agentes antibacterianos. Se ha reportado exacerbación de síntomas de miastenia gravis en pacientes que reciben terapia con claritromicina. La claritromicina se excreta principalmente por el hígado. Por lo tanto, se debe tener precaución en la administración del antibiótico a pacientes con función hepática alterada. También se debe tener cuidado cuando se administra claritromicina a pacientes con insuficiencia renal moderada a severa. Colchicina: Han habido informes post-comercialización de toxicidad de la colchicina con el uso concomitante de claritromicina y colchicina, especialmente en los ancianos, algunos de los cuales ocurrieron en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones: Colchicina). También se debe prestar atención a la posibilidad de resistencia cruzada entre claritromicina y otros macrólidos, como también con lincomicina y clindamicina.
Interacciones.
El uso de las siguientes drogas está estrictamente contraindicado debido al potencial para efectos severos por interacción de droga: Se han reportado niveles elevados de cisaprida en pacientes que reciben claritromicina y cisaprida concomitantemente. Esto puede producir prolongación de QT y arritmias cardíacas incluyendo taquicardia ventricular, fibrilación ventricular y torsades de pointes. Efectos similares se han observado en pacientes que toman claritromicina y pimozida concomitantemente (ver Contraindicaciones). Se ha informado de macrólidos que alteran el metabolismo de la terfenadina causando un aumento en los niveles de terfenadina que ocasionalmente se ha asociado con arritmias cardíacas tales como prolongación QT, taquicardia ventricular, fibrilación ventricular y torsades de pointes (ver Contraindicaciones). En un estudio en 14 voluntarios sanos, la administración concomitante de comprimidos de claritromicina y terfenadina produjo un aumento de dos a tres veces en los niveles séricos del metabolito ácido de la terfenadina y en la prolongación del intervalo QT que no llevó a ningún efecto clínicamente detectable. Ergotamina/dihidroergotamina: Los informes Post-comercialización indican que la co-administración de claritromicina con ergotamina o dihidroergotamina se ha asociado a toxicidad aguda por ergot caracterizada por vasoespasmo, e isquemia de las extremidades y de otros tejidos incluyendo sistema nervioso central. La administración concomitante de claritromicina y estos productos medicinales está contraindicada (ver Contraindicaciones). Efectos de Otros Productos Medicinales sobre Claritromicina: Las siguientes drogas son conocidas o sospechosas que afectan las concentraciones circulantes de claritromicina; se puede requerir ajustes de dosis de claritromicina o consideración de tratamientos alternativos. Efavirenz, nevirapina, rifampicina, rifabutina y rifapentina: Fuertes inductores del sistema del metabolismo de citocromo P450 tales como efavirenz, nevirapina, rifampicina, rifabutina y rifapentina pueden acelerar el metabolismo de claritromicina y por ende disminuir los niveles plasmáticos de claritromicina, mientras aumentan aquellos de 14(R)-hidroxi-claritromicina (14-OH-claritromicina), un metabolito que también es activo microbiológicamente, Dado que las actividades microbiológicas de claritromicina y 14-OH-claritromicina son diferentes para diferentes bacterias, el efecto terapéutico intentado podría estar impedido durante la administración concomitante de claritromicina e inductores de enzima. Fluconazol: La administración concomitante de fluconazol 200 mg diarios y claritromicina 500 mg dos veces al día a 21 voluntarios sanos llevó a incrementos en la concentración mínima media estado estable de claritromicina (Cmín) y área bajo la curva (ABC) de 33% y 18% respectivamente. Las concentraciones estado estable del metabolito activo 14-OH-claritromicina no se afectaron significativamente por la administración concomitante de fluconazol. No es necesario hacer ajuste de dosis de claritromicina. Ritonavir: Un estudio farmacocinético demostró que la administración concomitante de ritonavir 200 mg cada ocho horas y claritromicina 500 mg cada 12 horas produjo una inhibición marcada del metabolismo de claritromicina. La Cmáx de claritromicina aumentó en 31 %, Cmín aumentó 182% y ABC aumentó 77% con la administración concomitante de ritonavir. Se observó una inhibición esencialmente completa de la formación de 14-[R]-hidroxi-claritromicina. Debido a la gran ventana terapéutica para claritromicina, no debe ser necesaria una reducción en la dosificación en pacientes con función renal normal. Sin embargo, para pacientes con deterioro renal, se deben considerar los siguientes ajustes de dosificación: para pacientes con Clcr 30 a 60 mL/min, la dosis de claritromicina se debe reducir en 50%. Para pacientes con Clcr < 30 mL/min la dosis de claritromicina se debe reducir en 75%. Las dosis de claritromicina mayores a 1 g/día no se deben coadministrar con ritonavir. Efectos de Claritromicina sobre Otros Productos Medicinales: Antiarrítmicos: Existen reportes post-comercialización de torsades de pointes que ocurrieron con el uso concurrente de claritromicina y quinidina o disopiramida. Los electrocardiogramas se deben monitorear para prolongación de QTc durante la co-administración de claritromicina con estas drogas. Los niveles séricos de estos medicamentos se deben monitorear durante la terapia con claritromicina. Interacciones basadas en CYP3A4: La co-administración de claritromicina, conocido inhibidor de CYP3A y una droga principalmente metabolizada por CYP3A se puede asociar con elevaciones en las concentraciones de droga que pudieran incrementar o prolongar tanto los efectos terapéuticos como los adversos de la droga concomitante. La claritromicina se debe usar con precaución en pacientes que reciben tratamiento con otras drogas conocidas como sustratos de la enzima CYP3A, especialmente si el sustrato CYP3A tiene un margen de seguridad estrecho (ej. carbamazepina) y/o el sustrato es extensamente metabolizado por esta enzima. Se pueden considerar ajustes de dosis, y cuando sea posible, se deben monitorear de cerca las concentraciones séricas de drogas principalmente metabolizadas por CYP3A en pacientes que reciben claritromicina concurrentemente. Las siguientes drogas o clases de drogas son conocidas o se sospecha que se metabolizan por la misma isoenzima CYP3A: alprazolam, astemizol, carbamazepina, cilostazol, cisaprida, ciclosporina, disopiramida, alcaloides ergot, lovastatina, metilprednisolona, midazolam, omeprazol, anticoagulantes orales (ej. warfarina), pimozida, quinidina, rifabutina, sildenafil, simvastatina, tacrolimus, terfenadina, triazolam y vinblastina. Las drogas que interactúan por mecanismos similares a través de otras isoenzimas dentro del sistema citocromo P450 incluyen fenitoína, teofilina y valproato. Inhibidores de la HMG-CoA Reductasa: Como con otros macrólidos, se ha reportado que la claritromicina aumenta las concentraciones de inhibidores de la HMG-CoA reductasa (ej. lovastatina y simvastatina). Se han informado raros reportes de rabdomiólisis en pacientes que toman estas drogas concomitantemente. Omeprazol: Claritromicina (500 mg cada 8 horas) se administró en combinación con omeprazol (40 mg diarios) a sujetos adultos sanos. Las concentraciones plasmáticas estado estables de omeprazol se aumentaron (Cmáx, ABC0-24, y t½ aumentaron en 30%, 89% y 34%, respectivamente), por la administración concomitante de claritromicina. El valor medio del pH gástrico de 24 horas fue 5.2 cuando el omeprazol se administró solo y 5.7 cuando el omeprazol se co-administró con claritromicina. Anticoagulantes orales: Reportes espontáneos en el período post-comercialización sugieren que la administración concomitante de claritromicina y anticoagulantes orales puede potenciar los efectos de los anticoagulantes orales. Se deben monitorear cuidadosamente los tiempos de protrombina mi
entras los pacientes estén recibiendo claritromicina y anticoagulantes orales simultáneamente. Sildenafil, tadalafil y vardenafil: Cada uno de estos inhibidores de fosfodiesterasa se metaboliza, al menos en parte, por CYP3A, y CYP3A puede ser inhibido por la claritromicina administrada concomitantemente. La co-administración de claritromicina con sildenafil, tadalafil o vardenafil produciría probablemente un aumento de la exposición al inhibidor de fosfodiesterasa. Se debe considerar una reducción de las dosis de sildenafil, tadalafil y vardenafil cuando estas drogas se co-administran con claritromicina. Teofilina, carbamazepina: Los resultados de los estudios clínicos indican que hubo un modesto pero estadísticamente significativo (p≤0.05) aumento de los niveles circulantes de teofilina o carbamazepina cuando cualquiera de estas drogas se administraron concomitantemente con claritromicina. Tolterodina: La principal ruta del metabolismo de tolterodina es vía la isoforma 2D6 del citocromo P450 (CYP2D6). Sin embargo, en un subgrupo de la población dedicada de CYP2D6, la ruta identificada del metabolismo es vía CYP3A. En este subgrupo de la población, la inhibición de CYP3A produce concentraciones séricas significativamente mayores de tolterodina. Puede ser necesaria una reducción de la dosis de tolterodina en la presencia de inhibidores de CYP3A, tal como claritromicina en la población de metabolizadores pobres de CYP2D6. Triazolobenzodiazepinas (ej. alprazolam, midazolam, triazolam): Cuando se co-administra midazolam con claritromicina comprimidos (500 mg dos veces al día), el ABC de midazolam se incrementó 2.7 veces después de la administración intravenosa de midazolam y 7 veces después de la administración oral. La administración concomitante de midazolam oral y claritromicina se debe evitar. Si se co-administra midazolam intravenoso con claritromicina se debe monitorear cercanamente al paciente para permitir un ajuste de dosis. Las mismas precauciones se deben aplicar también a otras benzodiazepinas que se metabolizan por CYP3A, incluyendo triazolam y alprazolam. Para las benzodiazepinas que no son dependientes de CYP3A para su eliminación (temazepam, nitrazepam, lorazepam), no es probable una interacción clínicamente importante con claritromicina. Han existido reportes post-comercialización de interacciones de droga y efectos sobre el sistema nervioso central (SNC) (ej. somnolencia y confusión) con el uso concomitante de claritromicina y triazolam. Se sugiere monitoreo del paciente por aumento de los efectos farmacológicos sobre el SNC. Interacciones de Otras Drogas: Colchicina: La colchicina es un sustrato tanto para CYP3A como para el transportador del eflujo, P-glicoproteína (Pgp). Se sabe que la claritromicina y otros macrólidos inhiben CYP3A y Pgp. Cuando la claritromicina y la colchicina se administran juntas, la inhibición de Pgp y/o CYP3A por claritromicina puede llevar a aumento de la exposición a colchicina. Los pacientes se deben monitorear por síntomas clínicos de toxicidad a colchicina (ver Advertencias). Digoxina: Se piensa que la digoxina es un sustrato para el transportador del eflujo, P-glicoproteína (Pgp). Se conoce que la claritromicina inhibe Pgp. Cuando claritromicina y digoxina se administran juntas, la inhibición de Pgp por claritromicina puede llevar a aumento de la exposición a digoxina. En vigilancia post-comercialización se han reportado concentraciones séricas elevadas de digoxina en pacientes que reciben claritromicina y digoxina concomitantemente. Algunos pacientes han mostrado signos clínicos consistentes con toxicidad a digoxina, incluyendo arritmias potencialmente fatales. Las concentraciones séricas de digoxina se deben monitorear cuidadosamente si los pacientes reciben digoxina y claritromicina simultáneamente. Zidovudina: La administración oral simultánea de claritromicina comprimidos y zidovudina en pacientes adultos infectados con VIH puede producir una disminución en las concentraciones estado estables de zidovudina. Hoy en día, esta interacción no parece ocurrir en pacientes pediátricos infectados con VIH que toman Claritromicina Suspensión Pediátrica con zidovudina o dideoxinosina. Interacciones Bi-Direccionales de Droga: Atazanavir: Tanto claritromicina como atazanavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bi-direccional de droga. La co-administración de claritromicina (500 mg dos veces al día) con atazanavir (400 mg una vez al día) produjo 2 veces de aumento en la exposición a claritromicina y un 70% de disminución en la exposición a 14-OH-claritromicina, con un 28% de aumento en el ABC de atazanavir. Debido a la gran ventana terapéutica para claritromicina, no es necesaria una reducción de dosis en pacientes con función renal normal. Para pacientes con función renal moderada (clearance de creatinina 30 a 60 mL/min), la dosis de claritromicina se debe disminuir en 75% usando una formulación apropiada de claritromicina. No se deben co-administrar dosis de claritromicina mayores de 1000 mg por día con inhibidores de proteasa. Itraconazol: Tanto claritromicina como itraconazol son sustratos e inhibidores de CYP3A, llevando a una interacción bi-direccional de droga. Claritromicina puede aumentar los niveles plasmáticos de itraconazol, mientras itraconazol puede aumentar los niveles plasmáticos de claritromicina. Se debe monitorear cercanamente a los pacientes que toman itraconazol y claritromicina concomitantemente, por signos o síntomas de efecto farmacológico aumentado o prolongado. Saquinavir: Tanto claritromicina como saquinavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bi-direccional de droga. La administración concomitante de claritromicina (500 mg dos veces al día) y saquinavir (cápsulas de gelatina blanda, 1200 mg tres veces al día) a 12 voluntarios sanos produjo valores estado estable de ABC y Cmáx de saquinavir que eran 177% y 187% mayores que aquellos observados con saquinavir solo. Los valores ABC y Cmáx de claritromicina fueron aproximadamente 40% mayores que aquellos observados con claritromicina sola. No se requiere ajuste de dosis cuando las dos drogas se co-administran por un tiempo limitado en las dosis/formulaciones estudiadas. Observaciones de estudios de interacción de droga usando la formulación cápsula de gelatina blanda no puede ser representativa de los efectos observados usando la cápsula de gelatina dura de saquinavir. Observaciones de estudios de interacción de droga realizada con saquinavir solo no pueden ser representativas de los efectos observados con la terapia con saquinavir/ritonavir. Cuando saquinavir se co-administra con ritonavir, se deben considerar los efectos potenciales de ritonavir sobre claritromicina (ver Precauciones, Interacciones). Verapamil: Se han observado hipotensión, bradiarritmias y acidosis láctica en pacientes que toman claritromicina y verapamil concomitantemente. En este momento no se han llevado a cabo estudios clínicamente relevantes dirigidos a la compatibilidad física de la claritromicina con otras mezclas intravenosas. Embarazo: No se ha establecido la seguridad de claritromicina para uso durante el embarazo y durante la lactancia en lactantes. La claritromicina es excretada en la leche humana.
Conservación.
Mantener los comprimidos recubiertos a temperatura ambiente a menos de 25°C en un envase bien cerrado. Mantener alejado de la luz.
Sobredosificación.
Informes indican que la ingestión de grandes cantidades de claritromicina se puede esperar que produzca síntomas gastrointestinales. Un paciente que tenía una historia de trastorno bipolar ingirió 8 gramos de claritromicina y mostró estado mental alterado, conducta paranoide, hipokalemia e hipoxemia. Las reacciones adversas que acompañan una sobredosis se deben tratar con la pronta eliminación de la droga no absorbida y medidas de apoyo. Como con otros macrólidos, no se espera que los niveles séricos de claritromicina se afecten apreciablemente por hemodiálisis o diálisis peritoneal.
Presentación.
Comprimidos recubiertos Filmtab de 250 mg.
KLARICID
ABBOTT
Comprimidos recubiertos Filmtab 500mg
Antibiótico.
Descripción.
Claritromicina es un antibiótico macrólido semi-sintético obtenido por substitución de un grupo CH3O para el grupo hidroxilo (OH) en posición 6 del anillo lactónico de la eritromicina. Específicamente la claritromicina es 6-O-metil eritromicina A. El antibiótico es un polvo blanco a blanquecino, prácticamente inodoro, esencialmente insoluble en agua y ligeramente soluble en etanol, metanol y acetonitrilo. Su peso molecular es 747,96.
Composición.
Cada comprimido recubierto contiene: Claritromicina 500 mg. Excipientes: Núcleo: Croscarmelosa sódica, talco, dióxido de silicio, povidona, ácido esteárico, estearato de magnesio, celulosa microcristalina. Recubrimiento: Hipromelosa 15 cps, propilenglicol, hidroxipropilcelulosa, monooleato de sorbitan, dióxido de titanio, vainillina, colorante D&C amarillo N°10, laca alumínica (amarillo quinolina), ácido sórbico, Hipromelosa 6 cps.
Farmacología.
Propiedades Farmacodinámicas: Microbiología: La claritromicina ejerce su acción antibacteriana ligándose a las sub-unidades ribosomales 50S de las bacterias susceptibles y suprimiendo la síntesis proteica. La claritromicina ha demostrado una excelente actividad in vitro, tanto contra las cepas estándar de bacterias como de aislados clínicos. Es altamente potente contra una amplia variedad de organismos aerobios y anaerobios Gram-positivos y Gram-negativos. Las concentraciones inhibitorias mínimas (CIMs) de claritromicina generalmente son una dilución log2 más potentes que las CIMs de eritromicina. Los datos in vitro también indican que la claritromicina tiene excelente actividad contra la Legionella pneumophila y Mycoplasma pneumoniae. Es bactericida para Helicobacter pylori; esta actividad de claritromicina es mayor en pH neutro que en pH ácido. Los datos in vitro e in vivo muestran que este antibiótico tiene actividad clínicamente significativa contra mycobacterias especies. Los datos in vitro indican que Enterobacteriaceae, pseudomonas especies y otros bacilos Gram-negativos no fermentadores de lactosa no son susceptibles a claritromicina. La claritromicina ha mostrado ser activa contra la mayoría de las cepas de los siguientes microorganismos tanto in vitro como en infecciones clínicas como se describe en la sección Indicaciones: Microorganismos Aerobios Gram-positivos: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes. Microorganismos Aerobios Gram-negativos: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis. Otros microorganismos: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR). Mycobacterias: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) que consisten en: Mycobacterium avium, Mycobacterium intracellulare. La producción de Beta-Lactamasa no debe tener efecto en la actividad de la claritromicina. Nota: La mayoría de las cepas de estafilococos resistentes a meticilina y oxacilina son resistentes a claritromicina. Helicobacter: Helicobacter pylori. En cultivos realizados previo a la terapia, se aisló H. pylori y se determinaron los CIMs de claritromicina pre-tratamiento en 104 pacientes. De estos, cuatro pacientes tenían cepas resistentes, dos pacientes tenían cepas con susceptibilidad intermedia y 98 pacientes tenían cepas susceptibles. Los siguientes datos in vitro están disponibles, pero su importancia clínica se desconoce. La claritromicina exhibe in vitro actividad contra la mayoría de las cepas de los siguientes microorganismos; sin embargo, la seguridad y efectividad de la claritromicina en el tratamiento de infecciones clínicas debido a estos microorganismos no se ha establecido en estudios clínicos adecuados y bien controlados. Microorganismos aerobios Gram-positivo: Streptococcus agalactiae, Streptococci (Grupo C, F, G), Streptococci grupo viridans. Microorganismos aerobios Gram-negativo: Bordetella pertussis, Pasteurella multocida. Microorganismo anaerobios Gram-positivo: Clostridium perfringens, Peptococcus niger, Propionibacterium acnes. Microorganismos anaerobios Gram-negativo: Bacteroides melaninogenicus. Spirochetes: Borrelia burgdorferi. Campylobacter: Campylobacter jejuni. El principal metabolito de claritromicina en el hombre y otros primates es un metabolito microbiológicamente activo, 14-OH-claritromicina. Este metabolito es tan activo o 1 a 2 veces menos activo que el compuesto padre para la mayoría de los organismos, excepto para H. Influenzae contra el cual es dos veces más activo. El compuesto padre y el 14-OH metabolito ejercen un efecto aditivo o sinergístico sobre H influenzae in vitro e in vivo, dependiendo de las cepas bacterianas. Se encontró que la claritromicma es dos a diez veces más activa que la eritromicina en varios modelos experimentales de infección animal. Se mostró, por ejemplo, ser más efectiva que la eritromicina en infección sistémica en ratón, absceso subcutáneo en ratón e infecciones del tracto respiratorio en ratón causadas por S. pneumoniae, S. aureus, S. pyogenes y H. influenzae. En cerdos de guinea con infección por Legionella, este efecto fue más pronunciado, una dosis intraperitoneal de 1,6 mg/kg/día de claritromicina fue más efectiva que 50 mg/kg/día de eritromicina. Pruebas de Susceptibilidad: Los métodos cuantitativos que requieren medición de los diámetros de zona dan los estimados más precisos de susceptibilidad de las bacterias a los agentes antimicrobianos. Un procedimiento recomendado utiliza discos impregnados con 15 mcg de claritromicina para la prueba de susceptibilidad (prueba de difusión Kirby-Bauer); las interpretaciones correlacionan los diámetros de la zona de inhibición de esta prueba de disco con los valores CIM para claritromicina. Las CIMs se determinan por método de dilución agar o caldo. Con estos procedimientos, un informe de laboratorio de "susceptible" indica que el organismo infectante probablemente responda a la terapia. Un informe de "resistente" indica que el organismo infectante probablemente no responda a la terapia. Un informe de "Susceptibilidad Intermedia" sugiere que el efecto terapéutico de la droga puede ser equívoco o que el organismo sería susceptible si se usan dosis más altas (susceptibilidad intermedia también se refiere a moderadamente susceptible). Propiedades Farmacocinéticas: La cinética de la claritromicina administrada oralmente se ha estudiado extensamente en muchas especies animales y humanos adultos. Estos estudios han mostrado que la claritromicina es inmediata y rápidamente absorbida con una biodisponibilidad absoluta de aproximadamente 50%. Se encontró una acumulación pequeña o no pronosticada y la disposición metabólica no cambió en ninguna de las especies que siguieron con dosificación múltiple. La ingesta de alimentos inmediatamente antes de la dosis aumenta la biodisponibilidad de la claritromicina en una media de 25%. En general, este aumento es menor y debe ser de poca importancia clínica con los regímenes de dosis recomendados. La claritromicina puede así ser administrada con o sin alimento. In vitro: Los estudios in vitro mostraron que la unión de la claritromicina a proteínas en el plasma humano promedió alrededor de 70% en concentraciones de 0,45 a 4,5 mcg/mL. Una disminución de la unión a 41 % en 45,0 mcg/mL sugirió que los sitios de unión pueden llegar a ser saturados, pero esto ocurrió solamente en concentraciones lejos en exceso de los niveles terapéuticos de la droga. In vivo: Resultados de estudios en animales mostraron que los niveles de claritromicina en todos los tejidos, excepto el sistema nervioso central, fueron varias veces más altos que los niveles de droga circulante. Las concentraciones más altas fueron usualmente encontradas en el hígado y pulmón donde las proporciones tejido a plasma (T/P) alcanzaron 10 a 20. Sujetos normales: Con dosis de 250 mg dos veces al día, el peak de la concentración plasmática estado estable se alcanzó en dos a tres días y promedió alrededor de 1 mcg/mL para claritromicina y 0,6 mcg/mL para 14-OH-claritromicina, mientras las vidas medias de eliminación de la droga padre y el metabolito fueron tres a cuatro horas y cinco a seis horas, respectivamente. Con dosis de 500 mg dos veces al día, el Cmáx estado estable para claritromicina y su metabolito hidroxilado se alcanzó con la quinta dosis. Después de la quinta y séptima dosis, el Cmáx estado estable para claritromicina promedió 2,7 y 2,9 mcg/mL; su metabolito hidroxilado promedió 0,88 y 0,83 mcg/mL, respectivamente. Con un nivel de dosis de 500 mg, la vida media de la droga padre fue 4,5 a 4,8 horas, mientras que la de 14-OH-claritromicina fue 6,9 a 8,7 horas. En estado estable, los niveles de la 14-OH-claritromicina no aumentaron proporcionalmente con la dosis de claritromicina y las vidas medias aparentes tanto de la claritromicina como de su metabolito hidroxilado tendieron a ser más largas con dosis más altas. Este comportamiento farmacocinético no lineal de la claritromicina, unido con la disminución general en la formación de productos 14-hidroxilados y N-demetilados en dosis más altas, indica que el metabolismo no lineal de la claritromicina llega a ser más pronunciado en dosis altas. En humanos adultos a quienes se da una dosis oral única de 250 mg o 1200 mg de claritromicina, la excreción urinaria se encargó del 37,9% de la dosis más baja y 46,0% de la dosis más alta. La eliminación fecal se encargó del 40,2% y 29,1 % (esto incluyó un sujeto con sólo una muestra de deposición que contenía 14,1 %) de estas respectivas dosis. Pacientes: La claritromicina y su 14-OH-metabolito se distribuyen rápidamente en los tejidos y fluidos del cuerpo. Datos limitados de un pequeño número de pacientes sugieren que la claritromicina no alcanza niveles significativos en el fluido cerebroespinal (CSF) después de dosis orales (por ej. sólo 1 a 2% de los niveles séricos en CSF en pacientes con barreras CSF-sangre normales). Las concentraciones en los tejidos son usualmente varias veces más altas que las concentraciones séricas. Ejemplos de concentraciones de tejido y suero se presentan a continuación.

Deterioro Hepático: En un estudio que comparó un grupo de sujetos humanos sanos con un grupo de sujetos con deterioro del hígado a quienes se les dio 250 mg de claritromicina dos veces al día, por dos días y una dosis única de 250 mg al tercer día, los niveles plasmáticos estado estable y el clearing sistémico de claritromicina no fueron significativamente diferentes entre los dos grupos. En contraste, las concentraciones estado estable del 14-OH-metabolito fueron marcadamente más bajas en el grupo de sujetos con deterioro hepático. Este clearance metabólico disminuido del compuesto padre por 14-hidroxilación estuvo parcialmente alterado por un aumento en el clearance renal de la droga padre, provocando niveles estado estable de la droga padre comparables en sujetos sanos y con deterioro hepático. Estos resultados indican que no es necesario un ajuste de dosis en sujetos con deterioro hepático moderado o severo con función renal normal. Deterioro Renal: Se condujo un estudio para evaluar y comparar el perfil farmacocinético de múltiples dosis orales de 500 mg de claritromicina en sujetos con función renal normal y disminuida. Los niveles plasmáticos, vida media, Cmáx y Cmín tanto para claritromicina como para su 14-OH-metabolito fueron más altos y el ABC fue más amplio en sujetos con deterioro renal. Excreción urinaria y Kelim fueron más bajas. El alcance con el cual estos parámetros difirieron se correlacionó con el grado de deterioro renal; mientras más severo el deterioro renal, más significativa la diferencia (ver Dosificación). Sujetos mayores: También se condujo un estudio para evaluar y comparar la seguridad y perfiles farmacocinéticos de múltiples dosis orales de 500 mg de claritromicina en hombres y mujeres mayores sanos con aquellos sujetos hombres adultos jóvenes sanos. En el grupo de mayores, los niveles plasmáticos circulantes fueron más altos y la eliminación más lenta que en el grupo más joven tanto para la droga padre como para el 14-OH-metabolito. Sin embargo, no hubo diferencia entre los dos grupos cuando el clearance renal se correlacionó con el clearance de creatinina. De aquellos resultados se concluyó que ningún efecto en el manejo de claritromicina se relaciona con la función renal ni con la edad per se. Infecciones por Mycobacterium avium: Las concentraciones estado estable de claritromicina y 14-OH-claritromicina observadas después de la administración de dosis de 500 mg de claritromicina cada 12 horas a pacientes adultos con infección por VIH fueron similares a aquellas observadas en sujetos normales. Sin embargo, en dosis más altas que se pueden requerir para tratar infecciones por Mycobacterium avium, las concentraciones de claritromicina fueron mucho más altas que aquellas observadas en las dosis usuales. En pacientes adultos infectados con VIH que toman 1000 y 2000 mg/día en dosis divididas en dos, los valores estado estable de Cmáx de claritromicina variaron desde 2 a 4 mcg/mL y 5 a 10 mcg/mL, respectivamente. Las vidas medias de eliminación parecieron ser más largas con estas dosis más altas en comparación con aquellas observadas con dosis usuales en sujetos normales. Las concentraciones plasmáticas más altas y las vidas medias de eliminación observadas con estas dosis son consistentes con la conocida no linealidad de la farmacocinética de claritromicina. Administración Concomitante de Omeprazol: Se condujo un estudio farmacocinético con claritromicina 500 mg tres veces al día y omeprazol 40 mg una vez al día. Cuando la claritromicina se administró sola en dosis de 500 mg cada ocho horas, el valor medio estado estable de Cmáx fue aproximadamente 3,8 mcg/mL y el valor medio estado estable de Cmín fue aproximadamente 1,8 mcg/mL. La media de ABC0-8 para claritromicina fue 22,9 mcg/hr/mL. La Tmáx y la vida media fueron 2,1 hr y 5,3 hr, respectivamente, cuando la claritromicina se dosificó en 500 mg tres veces al día. En el mismo estudio cuando se administró claritromicina 500 mg tres veces al día con omeprazol 40 mg una vez al día, se observaron aumentos en la vida media y el ABC0-24 de omeprazol. Para todos los sujetos combinados, la media AUC0-24 de omeprazol fue 89% mayor y la media armónica para el T½ de omeprazol fue 34% mayor cuando el omeprazol se administró con claritromicina que cuando se administró solo. Cuando la claritromicina se administró con omeprazol, el estado estable de Cmáx, Cmín y AUC0-8 de claritromicina se aumentaron en 10%, 27% y 15%, respectivamente, sobre los valores alcanzados cuando la claritromicina se administró con placebo. En estado estable, las concentraciones en la mucosa gástrica de claritromicina seis horas después de la dosis fueron aproximadamente 25 veces más altas en el grupo claritromicina/omeprazol comparado con el grupo claritromicina sola. Seis horas después de la dosis, la media de las concentraciones en el tejido gástrico de claritromicina fueron aproximadamente 2 veces más altas cuando la claritromicina se administró con omeprazol que cuando la claritromicina se administró con placebo. Datos de seguridad pre-clínica: Toxicidad Aguda, Subcrónica y Crónica: Se realizaron estudios en ratones, ratas, perros y/o monos con claritromicina administrada oralmente. La duración de la administración variaron de una dosis oral única a administración oral repetida diariamente por seis meses consecutivos. En estudios agudos en ratones y ratas, una rata, pero no ratón, murió después de un gavage único de 5 g/kg de peso corporal. La dosis letal media, por lo tanto, fue mayor de 5 g/kg, la dosis de administración más alta aceptable. No se atribuyeron efectos adversos a claritromicina en primates expuestos a 100 mg/kg/día durante 14 días consecutivos o a 35 mg/kg/día durante un mes. Igualmente, no se observaron efectos adversos en ratas expuestas a 75 mg/kg/día durante un mes, a 35 mg/kg/día durante tres meses, o a 8 mg/kg/día por seis meses. Los perros fueron más sensibles a la claritromicina, tolerando 50 mg/kg/día durante 14 días, 10 mg/kg/día por uno y tres meses y 4 mg/kg/día por seis meses sin efectos adversos. Los principales signos clínicos en dosis tóxicas en estos estudios descritos anteriormente, incluyeron emesis, debilidad, reducido consumo alimenticio y reducida ganancia de peso, salivación, deshidratación e hiperactividad. Dos de diez monos que recibieron 400 mg/kg/día murieron en el día 8 de tratamiento; heces amarillas decoloradas se observaron en pocas ocasiones aisladas en algunos monos sobrevivientes a quienes se administró una dosis de 400 mg/kg/día durante 28 días. El primer órgano objetivo en dosis tóxicas en todas las especies fue el hígado. El desarrollo de hepatoxicidad en todas las especies fue detectable por elevación temprana de las concentraciones séricas de fosfatasa alcalina, alanina y aspartato aminotransferasa, gama-glutamil transferasa, y/o dehidrogenasa láctica. La discontinuación de la droga, generalmente produjo un retorno o acercamiento a las concentraciones normales de estos parámetros específicos. Tejidos adicionales comúnmente menos afectados en los diversos estudios incluyeron el estómago, timo y otros tejidos linfáticos, y los riñones. El lagrimeo e inyección conjuntival después de dosis cercanas a las terapéuticas, ocurrieron sólo en perros. Con una dosis masiva de 400 mg/kg/día, algunos perros y monos desarrollaron opacidad corneal y/o edema. Fertilidad, Reproducción y Teratogenicidad: Los estudios sobre fertilidad y reproducción han mostrado que dosis diarias de 150 a 160 mg/kg/día en ratas hembras y machos no causaron efectos adversos en el ciclo menstrual, fertilidad, parto y número y viabilidad de la descendencia. Dos estudios de teratogenicidad en ratas Wistar (p.o) y Sprague-Dawley (p.o. e i.v.), un estudio con conejos blancos en Nueva Zelanda y un estudio con monos cinomolgus fallaron para demostrar alguna teratogenicidad de claritromicina. Sólo en un estudio adicional con ratas Sprague-Dawley en dosis similares y esencialmente en condiciones similares ocurrió una incidencia muy baja, estadísticamente insignificante (aproximadamente 6%) de anomalías cardiovasculares. Estas anomalías parecieron ser debidas a expresión espontánea de cambios genéticos dentro de la colonia. Dos estudios en ratones también revelaron una incidencia variable de fisura palatina (3 a 30%) después de dosis 70 veces el rango superior de la dosis usual diaria clínica humana (500 mg dos veces al día), pero no en 35 veces la dosis máxima diaria clínica humana, sugiriendo toxicidad maternal y fetal pero no teratogenicidad. Se ha mostrado que la claritromicina produce pérdida embriónica en monos cuando se administra en aproximadamente diez veces el rango superior de la dosis humana diaria usual (500 mg dos veces al día), comenzando en el día 20 de gestación. Este efecto se ha atribuido a la toxicidad maternal de la droga en dosis muy altas. Un estudio adicional en monos hembras preñadas con dosis de aproximadamente 2,5 a 5 veces la dosis diaria máxima entregada no produjo ningún riesgo a la cría. Un test letal dominante en ratones con dosis de 1000 mg/kg/día (aproximadamente 70 veces la dosis clínica máxima diaria humana) fue claramente negativo para cualquier actividad mutagénica y en un estudio de ratas Segmento 1 tratadas con hasta 500 mg/kg/día (aproximadamente 35 veces la dosis clínica máxima diaria humana) durante 80 días, no se mostró evidencia de deterioro funcional de la fertilidad masculina debido al largo período de exposición a estas dosis muy altas de claritromicina. Mutagenicidad: Los estudios para evaluar el potencial mutagénico de claritromicina se realizaron usando tanto sistemas de prueba con microsomas de hígado de rata no activados como no activados (Test de Ames). Los resultados de estos estudios no proporcionaron evidencia de potencial mutagénico en las concentraciones de droga de 25 mcg/placa de Petri o menos. En una concentración de 50 mcg, la droga fue tóxica para todas las cepas testeadas. Estudios clínicos: El Helicobacter pylori se asocia fuertemente con la enfermedad de úlcera péptica. Noventa (90) a 100% de los pacientes con úlceras duodenales está infectado con este patógeno. La erradicación del H. pylori se ha mostrado que reduce la tasa de recurrencia de úlcera duodenal, por consiguiente reduciendo la necesidad de terapia de mantención anti-secretoria. Triple Terapia en Ulcera Duodenal: En un estudio doble ciego bien controlado, pacientes con úlcera duodenal infectados con H. pylori recibieron triple terapia con 500 mg de claritromicina dos veces al día, amoxicilina 1000 mg dos veces al día y omeprazol 20 mg al día, durante diez días. El H. pylori fue erradicado en 90% de los pacientes que recibieron claritromicina triple terapia y en 60% de los pacientes que recibieron terapia dual. En un estudio independiente en pacientes infectados con H. pylori que recibieron terapia de erradicación con claritromicina 500 mg dos veces al día en conjunto con amoxicilina 1000 mg dos veces al día y omeprazol 20 mg al día (Grupo A) u omeprazol 20 mg dos veces al día (Grupo B) por siete días. En aquellos pacientes no tratados previamente con terapia anti-H. pylori, el H. pylori fue erradicado en 88% de los pacientes en el Grupo A y 86% de los pacientes en el grupo B. En un estudio abierto en pacientes infectados con H. pylori con úlcera duodenal o dispepsia no ulcerosa (NUD) recibieron terapia de erradicación con claritromicina 500 mg dos veces al día, lansoprazol 30 mg dos veces al día, más amoxicilina 1000 mg dos veces al día, durante diez días. En un análisis de todos los pacientes tratados, el H. pylori fue erradicado en 91 % de los pacientes. Terapia Dual en Ulcera Duodenal: En estudios doble ciego, bien controlados, pacientes con úlcera duodenal infectados con H. pylori recibieron terapia de erradicación con claritromicina 500 mg tres veces al día y omeprazol 40 mg diariamente, durante 14 días, seguido por omeprazol 40 mg (estudio A) u omeprazol 20 mg (estudios B, C y D) diariamente por un adicional de 14 días; los pacientes en cada grupo control recibieron omeprazol solo por 28 días. En el estudio A, el H. pylori se erradicó por sobre el 80% de los pacientes que recibieron claritromicina y omeprazol y en sólo 1 % de los pacientes que recibieron omeprazol solo. En los estudios B, C, y D, la tasa de erradicación combinada fue sobre el 70% de los pacientes que recibieron claritromicina y omeprazol y menos del 1 % en pacientes que recibieron omeprazol solo. En cada estudio, la tasa de recurrencia de úlcera a los seis meses fue estadísticamente más baja en pacientes tratados con claritromicina y omeprazol comparado con pacientes que recibieron omeprazol solo. En un estudio investigador-ciego, los pacientes infectados con H. pylori recibieron terapia de erradicación con claritromicina 500 mg tres veces al día, en conjunto con lansoprazol 60 mg/día en dosis única o dividida, durante 14 días. La tasa de erradicación combinada fue sobre 60%.
Indicaciones.
La claritromicina está indicada para el tratamiento de infecciones debidas a organismos susceptibles. Tales infecciones incluyen: Infecciones del tracto respiratorio inferior (ej. bronquitis, pneumonia; Infecciones del tracto respiratorio superior (ej. faringitis, sinusitis); Infecciones de la piel y tejidos blandos (ej. foliculitis, celulitis, erisipelas; Infecciones mycobacterianas localizadas o diseminadas debido a Mycobacterium avium o Mycobacterium intracellulare. Infecciones localizadas debido a Mycobacterium chelonae, Mycobacterium fortuitum o Mycobacterium kansasii; La claritromicina está indicada para la prevención de infección diseminada porMycobacterium avium complex en pacientes infectados con VIH con conteo de linfocito CD4 menor o igual a 100/mm3; Claritromicina en presencia de supresión ácida también está indicada para la erradicación de H. pylori produciendo una disminución de la recurrencia de úlcera duodenal (ver Estudios clínicos).
Dosificación.
La dosis usual recomendada de claritromicina en adultos es de un comprimido de 250 mg dos veces al día. En infecciones más severas, la dosis puede ser aumentada a 500 mg dos veces al día. La duración usual de la terapia es de 6 a 14 días. En pacientes con deterioro renal con clearance de creatinina menos de 30 mL/min, la dosis de claritromicina se debe reducir a la mitad, por ej., 250 mg una vez al día, o 250 mg dos veces al día en las infecciones más severas. El tratamiento no se debe prolongar más allá de 14 días en estos pacientes. Dosis en pacientes con infecciones mycobacterianas: La dosis recomendada para adultos con infecciones mycobacterianas es 500 mg dos veces al día. El tratamiento de infecciones diseminadas MAC en pacientes con SIDA se debe continuar tanto tiempo hasta se demuestre beneficio clínico y microbiológico. La claritromicina se debe usar en conjunto con otros agentes antimycobacterianos. El tratamiento de otras infecciones mycobacterianas no-tuberculosas se debe continuar según el criterio del médico. Dosis para profilaxis MAC: La dosis recomendada de claritromicina en adultos es 500 mg dos veces al día. Para la erradicación de H. pylori, los regímenes de dosis recomendada son: Régimen Triple Terapia: Claritromicina 500 mg dos veces al día en conjunto con lansoprazol 30 mg dos veces al día, más amoxicilina 1000 mg dos veces al día, por diez días. Claritromicina 500 mg dos veces al día en conjunto con amoxicilina 1000 mg dos veces al día y omeprazol 20 mg dos veces al día, por siete a diez días. Regímenes Terapia Dual: Claritromicina 500 mg tres veces al día en conjunto con omeprazol 40 mg diarios por 14 días, seguido por omeprazol 20 mg o 40 mg diarios por un adicional de 14 días. Claritromicina 500 mg tres veces al día en conjunto con lansoprazol 60 mg diarios por 14 días. Más allá se puede requerir supresión ácida para completar la cicatrización de la úlcera.
Contraindicaciones.
La claritromicina está contraindicada en pacientes con conocida hipersensibilidad a los antibióticos macrólidos. La administración concomitante de claritromicina y cualquiera de las siguientes drogas está contraindicada: astemizol, cisaprida, pimozida, terfenadina y ergotamina o dihidroergotamina (ver Interacciones).
Reacciones adversas.
El perfil de seguridad de la formulación pediátrica es similar a la del comprimido de 250 mg en pacientes adultos. La Tabla 1 muestra los eventos adversos reportados en pacientes que tomaron claritromicina en estudios clínicos. Los eventos adversos de muestran por sistema corporal y frecuencia (común ≥1/100, < 1/10).
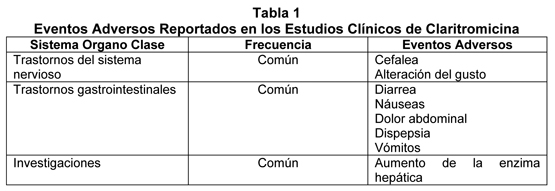
Experiencia Post-Comercialización: La claritromicina se comercializa en varias formulaciones diferentes. La Tabla 2 es una compilación de reacciones adversas para todas las formulaciones incluyendo claritromicina suspensión pediátrica. Debido a que estas reacciones se reportan voluntariamente desde una población de tamaño incierto, no siempre es posible estimar realmente su frecuencia o establecer una relación causal a la exposición a la droga. La exposición de paciente se estima ser mayor a 1 billón de días de tratamiento paciente para claritromicina.
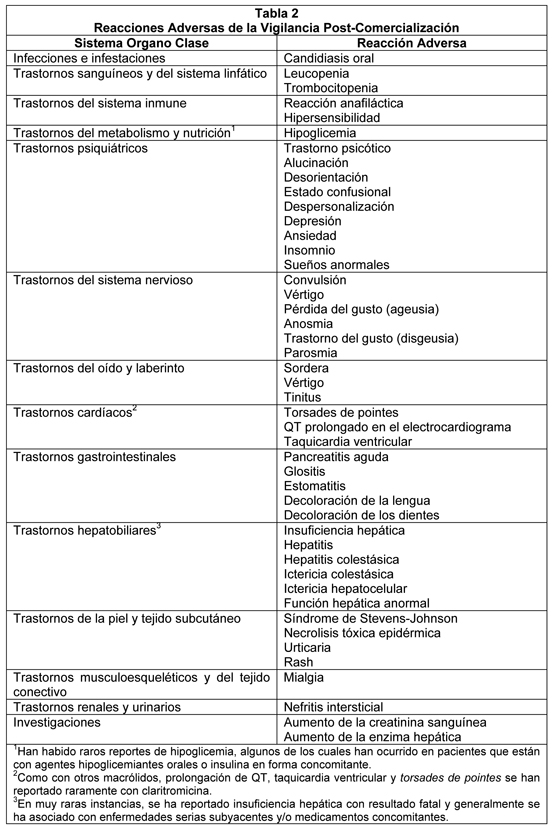
Han habido informes post-comercialización de toxicidad de la colchicina con uso concomitante de claritromicina y colchicina, especialmente en los ancianos, algunos de los cuales ocurrieron en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones: Colchicina y Advertencias). Pacientes Inmunocomprometidos: En pacientes con SIDA y otros inmunocomprometidos tratados con la más alta dosis de claritromicina por largos períodos de tiempo por infecciones micobacterianas, a menudo fue difícil distinguir eventos adversos posiblemente asociados con la administración de claritromicina de signos subyacentes a la enfermedad por VIH o enfermedad intercurrente. En pacientes adultos, los eventos adversos más frecuentemente informados por pacientes tratados con dosis diarias totales de 1000 mg de claritromicina fueron: náuseas, vómitos, alteración del gusto, dolor abdominal, diarrea, rash, flatulencia, cefalea, constipación, trastornos de audición, elevaciones de SGOT y SGPT. Eventos adicionales de baja frecuencia incluyeron disnea, insomnio y boca seca. En estos pacientes inmuno comprometidos las evaluaciones de los valores de laboratorio se realizaron analizando aquellos valores fuera del nivel seriamente anormal (por ej. el extremo alto o el límite bajo) para el test específico. Sobre las bases de este criterio, alrededor de 2% a 3% de estos pacientes que recibieron 1000 mg de claritromicina diariamente tuvieron niveles elevados de SGOT y SGTP seriamente anormales y glóbulos blancos y recuento de plaquetas anormalmente bajos. Un menor porcentaje de pacientes también tenía niveles elevados del BUN.
Advertencias.
El médico no debe prescribir claritromicina a mujeres embarazadas sin evaluar cuidadosamente los beneficios frente al riesgo, especialmente durante los tres primeros meses de embarazo. Claritromicina no debería ser usada en mujeres embarazadas excepto en cuadros clínicos en los que no exista terapia alternativa apropiada. Si el embarazo ocurre durante el tratamiento, el paciente debería ser informado del potencial daño al feto. Claritromicina ha demostrado efectos adversos en el embarazo y/o desarrollo embriofetal en monos, ratas, ratones y conejos a dosis que producen niveles plasmáticos 2 a 17 veces los niveles plasmáticos alcanzados en humanos tratados con las dosis máximas recomendadas. El uso a largo plazo, como con otros antibióticos, produce colonización con números aumentados de bacterias y hongos no susceptibles. Si ocurren superinfecciones, se debe instituir una terapia apropiada. Se ha reportado colitis pseudomembranosa con prácticamente todos los agentes antibacterianos, incluyendo macrólidos y puede variar desde leve hasta con riesgo vital. Se ha reportado diarrea asociada a Clostridium difficile (CDAD) con el uso de prácticamente todos los agentes antimicrobianos incluyendo claritromicina, y puede variar en severidad desde diarrea leve a colitis fatal. El tratamiento con agentes antibacterianos alteran la flora normal del colon, el cual puede llevar a un sobrecrecimiento de C. difficile. El CDAD se debe considerar en todos los pacientes que presentan diarrea después del uso de antibióticos. Es necesario una historia médica cuidadosa ya que CDAD se ha reportado que ocurre sobre dos meses después de la administración de agentes antibac
terianos. Se ha reportado exacerbación de síntomas de miastenia gravis en pacientes que reciben terapia con claritromicina. La claritromicina se excreta principalmente por el hígado. Por lo tanto, se debe tener precaución en la administración del antibiótico a pacientes con función hepática alterada. También se debe tener cuidado cuando se administra claritromicina a pacientes con insuficiencia renal moderada a severa. Colchicina: Han habido informes post-comercialización de toxicidad de la colchicina con el uso concomitante de claritromicina y colchicina, especialmente en los ancianos, algunos de los cuales ocurrieron en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones: Colchicina). También se debe prestar atención a la posibilidad de resistencia cruzada entre claritromicina y otros macrólidos, como también con lincomicina y clindamicina.
Interacciones.
El uso de las siguientes drogas está estrictamente contraindicado debido al potencial para efectos severos por interacción de droga: Se han reportado niveles elevados de cisaprida en pacientes que reciben claritromicina y cisaprida concomitantemente. Esto puede producir prolongación de QT y arritmias cardíacas incluyendo taquicardia ventricular, fibrilación ventricular y torsades de pointes. Efectos similares se han observado en pacientes que toman claritromicina y pimozida concomitantemente (ver Contraindicaciones). Se ha informado de macrólidos que alteran el metabolismo de la terfenadina causando un aumento en los niveles de terfenadina que ocasionalmente se ha asociado con arritmias cardíacas tales como prolongación QT, taquicardia ventricular, fibrilación ventricular y torsades de pointes (ver Contraindicaciones). En un estudio en 14 voluntarios sanos, la administración concomitante de comprimidos de claritromicina y terfenadina produjo un aumento de dos a tres veces en los niveles séricos del metabolito ácido de la terfenadina y en la prolongación del intervalo QT que no llevó a ningún efecto clínicamente detectable. Ergotamina/dihidroergotamina: Los informes Post-comercialización indican que la co-administración de claritromicina con ergotamina o dihidroergotamina se ha asociado a toxicidad aguda por ergot caracterizada por vasoespasmo, e isquemia de las extremidades y de otros tejidos incluyendo sistema nervioso central. La administración concomitante de claritromicina y estos productos medicinales está contraindicada (ver Contraindicaciones). Efectos de Otros Productos Medicinales sobre Claritromicina: Las siguientes drogas son conocidas o sospechosas que afectan las concentraciones circulantes de claritromicina; se puede requerir ajustes de dosis de claritromicina o consideración de tratamientos alternativos. Efavirenz, nevirapina, rifampicina, rifabutina y rifapentina: Fuertes inductores del sistema del metabolismo de citocromo P450 tales como efavirenz, nevirapina, rifampicina, rifabutina y rifapentina pueden acelerar el metabolismo de claritromicina y por ende disminuir los niveles plasmáticos de claritromicina, mientras aumentan aquellos de 14(R)-hidroxi-claritromicina (14-OH-claritromicina), un metabolito que también es activo microbiológicamente, Dado que las actividades microbiológicas de claritromicina y 14-OH-claritromicina son diferentes para diferentes bacterias, el efecto terapéutico intentado podría estar impedido durante la administración concomitante de claritromicina e inductores de enzima. Fluconazol: La administración concomitante de fluconazol 200 mg diarios y claritromicina 500 mg dos veces al día a 21 voluntarios sanos llevó a incrementos en la concentración mínima media estado estable de claritromicina (Cmín) y área bajo la curva (ABC) de 33% y 18% respectivamente. Las concentraciones estado estable del metabolito activo 14-OH-claritromicina no se afectaron significativamente por la administración concomitante de fluconazol. No es necesario hacer ajuste de dosis de claritromicina. Ritonavir: Un estudio farmacocinético demostró que la administración concomitante de ritonavir 200 mg cada ocho horas y claritromicina 500 mg cada 12 horas produjo una inhibición marcada del metabolismo de claritromicina. La Cmáx de claritromicina aumentó en 31 %, Cmín aumentó 182% y ABC aumentó 77% con la administración concomitante de ritonavir. Se observó una inhibición esencialmente completa de la formación de 14-[R]-hidroxi-claritromicina. Debido a la gran ventana terapéutica para claritromicina, no debe ser necesaria una reducción en la dosificación en pacientes con función renal normal. Sin embargo, para pacientes con deterioro renal, se deben considerar los siguientes ajustes de dosificación: para pacientes con Clcr 30 a 60 mL/min, la dosis de claritromicina se debe reducir en 50%. Para pacientes con Clcr < 30 mL/min la dosis de claritromicina se debe reducir en 75%. Las dosis de claritromicina mayores a 1 g/día no se deben coadministrar con ritonavir. Efectos de Claritromicina sobre Otros Productos Medicinales: Antiarrítmicos: Existen reportes post-comercialización de torsades de pointes que ocurrieron con el uso concurrente de claritromicina y quinidina o disopiramida. Los electrocardiogramas se deben monitorear para prolongación de QTc durante la co-administración de claritromicina con estas drogas. Los niveles séricos de estos medicamentos se deben monitorear durante la terapia con claritromicina. Interacciones basadas en CYP3A4: La co-administración de claritromicina, conocido inhibidor de CYP3A y una droga principalmente metabolizada por CYP3A se puede asociar con elevaciones en las concentraciones de droga que pudieran incrementar o prolongar tanto los efectos terapéuticos como los adversos de la droga concomitante. La claritromicina se debe usar con precaución en pacientes que reciben tratamiento con otras drogas conocidas como sustratos de la enzima CYP3A, especialmente si el sustrato CYP3A tiene un margen de seguridad estrecho (ej. carbamazepina) y/o el sustrato es extensamente metabolizado por esta enzima. Se pueden considerar ajustes de dosis, y cuando sea posible, se deben monitorear de cerca las concentraciones séricas de drogas principalmente metabolizadas por CYP3A en pacientes que reciben claritromicina concurrentemente. Las siguientes drogas o clases de drogas son conocidas o se sospecha que se metabolizan por la misma isoenzima CYP3A: alprazolam, astemizol, carbamazepina, cilostazol, cisaprida, ciclosporina, disopiramida, alcaloides ergot, lovastatina, metilprednisolona, midazolam, omeprazol, anticoagulantes orales (ej. warfarina), pimozida, quinidina, rifabutina, sildenafil, simvastatina, tacrolimus, terfenadina, triazolam y vinblastina. Las drogas que interactúan por mecanismos similares a través de otras isoenzimas dentro del sistema citocromo P450 incluyen fenitoína, teofilina y valproato. Inhibidores de la HMG-CoA Reductasa: Como con otros macrólidos, se ha reportado que la claritromicina aumenta las concentraciones de inhibidores de la HMG-CoA reductasa (ej. lovastatina y simvastatina). Se han informado raros reportes de rabdomiólisis en pacientes que toman estas drogas concomitantemente. Omeprazol: Claritromicina (500 mg cada 8 horas) se administró en combinación con omeprazol (40 mg diarios) a sujetos adultos sanos. Las concentraciones plasmáticas estado estables de omeprazol se aumentaron (Cmáx, ABC0-24, y t½ aumentaron en 30%, 89% y 34%, respectivamente), por la administración concomitante de claritromicina. El valor medio del pH gástrico de 24 horas fue 5.2 cuando el omeprazol se administró solo y 5.7 cuando el omeprazol se co-administró con claritromicina. Anticoagulantes orales: Reportes espontáneos en el período post-comercialización sugieren que la administración concomitante de claritromicina y anticoagulantes orales puede potenciar los efectos de los anticoagulantes orales. Se deben monitorear cuidadosamente los tiempos de protrombina mientras los pacientes estén recibiendo claritromicina y anticoagulantes orales simultáneamente. Sildenafil, tadalafil y vardenafil: Cada uno de estos inhibidores de fosfodiesterasa se metaboliza, al menos en parte, por CYP3A, y CYP3A puede ser inhibido por la claritromicina administrada concomitantemente. La co-administración de claritromicina con sildenafil, tadalafil o vardenafil produciría probablemente un aumento de la exposición al inhibidor de fosfodiesterasa. Se debe considerar una reducción de las dosis de sildenafil, tadalafil y vardenafil cuando estas drogas se co-administran con claritromicina. Teofilina, carbamazepina: Los resultados de los estudios clínicos indican que hubo un modesto pero estadísticamente significativo (p≤0.05) aumento de los niveles circulantes de teofilina o carbamazepina cuando cualquiera de estas drogas se administraron concomitantemente con claritromicina. Tolterodina: La principal ruta del metabolismo de tolterodina es vía la isoforma 2D6 del citocromo P450 (CYP2D6). Sin embargo, en un subgrupo de la población dedicada de CYP2D6, la ruta identificada del metabolismo es vía CYP3A. En este subgrupo de la población, la inhibición de CYP3A produce concentraciones séricas significativamente mayores de tolterodina. Puede ser necesaria una reducción de la dosis de tolterodina en la presencia de inhibidores de CYP3A, tal como claritromicina en la población de metabolizadores pobres de CYP2D6. Triazolobenzodiazepinas (ej. alprazolam, midazolam, triazolam): Cuando se co-administra midazolam con claritromicina comprimidos (500 mg dos veces al día), el ABC de midazolam se incrementó 2.7 veces después de la administración intravenosa de midazolam y 7 veces después de la administración oral. La administración concomitante de midazolam oral y claritromicina se debe evitar. Si se co-administra midazolam intravenoso con claritromicina se debe monitorear cercanamente al paciente para permitir un ajuste de dosis. Las mismas precauciones se deben aplicar también a otras benzodiazepinas que se metabolizan por CYP3A, incluyendo triazolam y alprazolam. Para las benzodiazepinas que no son dependientes de CYP3A para su eliminación (temazepam, nitrazepam, lorazepam), no es probable una interacción clínicamente importante con claritromicina. Han existido reportes post-comercialización de interacciones de droga y efectos sobre el sistema nervioso central (SNC) (ej. somnolencia y confusión) con el uso concomitante de claritromicina y triazolam. Se sugiere monitoreo del paciente por aumento de los efectos farmacológicos sobre el SNC. Interacciones de Otras Drogas: Colchicina: La colchicina es un sustrato tanto para CYP3A como para el transportador del eflujo, P-glicoproteína (Pgp). Se sabe que la claritromicina y otros macrólidos inhiben CYP3A y Pgp. Cuando la claritromicina y la colchicina se administran juntas, la inhibición de Pgp y/o CYP3A por claritromicina puede llevar a aumento de la exposición a colchicina. Los pacientes se deben monitorear por síntomas clínicos de toxicidad a colchicina (ver Advertencias). Digoxina: Se piensa que la digoxina es un sustrato para el transportador del eflujo, P-glicoproteína (Pgp). Se conoce que la claritromicina inhibe Pgp. Cuando claritromicina y digoxina se administran juntas, la inhibición de Pgp por claritromicina puede llevar a aumento de la exposición a digoxina. En vigilancia post-comercialización se han reportado concentraciones séricas elevadas de digoxina en pacientes que reciben claritromicina y digoxina concomitantemente. Algunos pacientes han mostrado signos clínicos consistentes con toxicidad a digoxina, incluyendo arritmias potencialmente fatales. Las concentraciones séricas de digoxina se deben monitorear cuidadosamente si los pacientes reciben digoxina y claritromicina simultáneamente. Zidovudina: La administración oral simultánea de claritromicina comprimidos y zidovudina en pacientes adultos infectados con VIH puede producir una disminución en las concentraciones estado estables de zidovudina. Hoy en día, esta interacción no parece ocurrir en pacientes pediátricos infectados con VIH que toman Claritromicina Suspensión Pediátrica con zidovudina o dideoxinosina. Interacciones Bi-Direccionales de Droga: Atazanavir: Tanto claritromicina como atazanavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bi-direccional de droga. La co-administración de claritromicina (500 mg dos veces al día) con atazanavir (400 mg una vez al día) produjo 2 veces de aumento en la exposición a claritromicina y un 70% de disminución en la exposición a 14-OH-claritromicina, con un 28% de aumento en el ABC de atazanavir. Debido a la gran ventana terapéutica para claritromicina, no es necesaria una reducción de dosis en pacientes con función renal normal. Para pacientes con función renal moderada (clearance de creatinina 30 a 60 mL/min), la dosis de claritromicina se debe disminuir en 75% usando una formulación apropiada de claritromicina. No se deben co-administrar dosis de claritromicina mayores de 1000 mg por día con inhibidores de proteasa. Itraconazol: Tanto claritromicina como itraconazol son sustratos e inhibidores de CYP3A, llevando a una interacción bi-direccional de droga. Claritromicina puede aumentar los niveles plasmáticos de itraconazol, mientras itraconazol puede aumentar los niveles plasmáticos de claritromicina. Se debe monitorear cercanamente a los pacientes que toman itraconazol y claritromicina concomitantemente, por signos o síntomas de efecto farmacológico aumentado o prolongado. Saquinavir: Tanto claritromicina como saquinavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bi-direccional de droga. La administración concomitante de claritromicina (500 mg dos veces al día) y saquinavir (cápsulas de gelatina blanda, 1200 mg tres veces al día) a 12 voluntarios sanos produjo valores estado estable de ABC y Cmáx de saquinavir que eran 177% y 187% mayores que aquellos observados con saquinavir solo. Los valores ABC y Cmáx de claritromicina fueron aproximadamente 40% mayores que aquellos observados con claritromicina sola. No se requiere ajuste de dosis cuando las dos drogas se co-administran por un tiempo limitado en las dosis/formulaciones estudiadas. Observaciones de estudios de interacción de droga usando la formulación cápsula de gelatina blanda no puede ser representativa de los efectos observados usando la cápsula de gelatina dura de saquinavir. Observaciones de estudios de interacción de droga realizada con saquinavir solo no pueden ser representativas de los efectos observados con la terapia con saquinavir/ritonavir. Cuando saquinavir se co-administra con ritonavir, se deben considerar los efectos potenciales de ritonavir sobre claritromicina (ver Precauciones, Interacciones). Verapamil: Se han observado hipotensión, bradiarritmias y acidosis láctica en pacientes que toman claritromicina y verapamil concomitantemente. En este momento no se han llevado a cabo estudios clínicamente relevantes dirigidos a la compatibilidad física de la claritromicina con otras mezclas intravenosas. Embarazo: No se ha establecido la seguridad de claritromicina para uso durante el embarazo y durante la lactancia en lactantes. La claritromicina es excretada en la leche humana.
Conservación.
Mantener los comprimidos recubiertos a temperatura ambiente a menos de 25°C en un envase bien cerrado. Mantener alejado de la luz.
Sobredosificación.
Informes indican que la ingestión de grandes cantidades de claritromicina se puede esperar que produzca síntomas gastrointestinales. Un paciente que tenía una historia de trastorno bipolar ingirió 8 gramos de claritromicina y mostró estado mental alterado, conducta paranoide, hipokalemia e hipoxemia. Las reacciones adversas que acompañan una sobredosis se deben tratar con la pronta eliminación de la droga no absorbida y medidas de apoyo. Como con otros macrólidos, no se espera que los niveles séricos de claritromicina se afecten apreciablemente por hemodiálisis o diálisis peritoneal.
Presentación.
Comprimidos recubiertos Filmtab de 500 mg.
KLARICID
ABBOTT
Liofilizado para solución inyectable
Antibiótico.
Descripción.
Claritromicina es un antibiótico macrólido semisintético obtenido por sustitución de un grupo CH3O por el grupo hidroxilo en posición 6 en el anillo lactónico de la eritromicina. Específicamente la claritromicina es 6-O-metil eritromicina A. El antibiótico es un polvo blanco a blanquecino, prácticamente inodoro, esencialmente insoluble en agua y ligeramente soluble en etanol, metanol y acetonitrilo. Su peso molecular es 747,96. La forma farmacéutica inyectable, claritromicina I.V. es un polvo liofilizado que contiene claritromicina 500 mg por ampolla y ácido lactobionato como agente soluble. El polvo es reconstituido con agua para inyectar previo a su uso.
Farmacología.
Propiedades Farmacodinámicas: Microbiología: La Claritromicina ejerce su acción antibacteriana ligándose a las subunidades ribosomales 50S de las bacterias susceptibles con la supresión subsecuente de la síntesis proteica. La Claritromicina ha demostrado una excelente actividad in vitro, tanto contra las cepas bacterianas estándar como contra aislados clínicos. Es altamente potente contra una amplia variedad de organismos aerobios y anaerobios Grampositivos y Gramnegativos. Las concentraciones inhibitorias mínimas (CIMs) de la claritromicina son comúnmente una dilución log2 más potentes que las CIMs de la eritromicina. Los datos in vitro también indican que la Claritromicina tiene excelente actividad contra la Legionella pneumophila, Mycoplasma pneumoniae y Helicobacter (Campylobacter) pylori. Los datos in vitro e in vivo muestran que este antibiótico tiene una actividad clínicamente significativa contra las especies micobacterianas. Los datos in vitro indican que Enterobacteriaceae, especies de Pseudomonas y otros bacilos gramnegativos que no fermentan en lactosa no son susceptibles a la claritromicina. La Claritromicina ha mostrado ser activa contra la mayoría de las cepas de los siguientes microorganismos tanto in vitro como en infecciones clínicas como está descrito en la sección Indicaciones. Microbiologia: Microorganismos Aerobios Grampositivos: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes. Microorganismos Aerobios Gramnegativos: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis. Otros microorganismos: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR). Mycobacterias: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) que consisten en: Mycobacterium avium, Mycobacterium intracellulare. La producción de Beta-Lactamasa no debe tener efecto en la actividad de la claritromicina. Nota: La mayoría de las cepas de estafilococos resistentes a la meticilina y resistentes a la oxacilina son resistentes a la claritromicina. Helicobacter: Helicobacter pylori. En cultivos realizados antes de la terapia, H. pylori fue aislado y las CIMs de la claritromicina se determinaron pretratamiento en 104 pacientes. De estos, cuatro pacientes tuvieron cepas resistentes, dos pacientes tenían cepas con susceptibilidad intermedia y 98 pacientes tenían cepas susceptibles. Los siguientes datos in vitro se encuentran disponibles, pero su importancia clínica es desconocida. La claritromicina exhibe in vitro actividad contra la mayoría de las cepas de los siguientes microorganismos; sin embargo, la seguridad y efectividad de la claritromicina en el tratamiento de infecciones clínicas debido a estos microorganismos no se han establecido en estudios clínicos adecuados y bien controlados. Microorganismos aerobios Grampositivos: Streptococcus agalactiae, Estreptococci (Grupo C, F, G), Estreptococci grupo Viridans. Microorganismos aerobios Gramnegativos: Bordetella pertussis. Pasteurella multocida. Microorganismos anaerobios Grampositivos: Clostridium perfringens, Peptococcus niger, Propionibacteruim acnes. Microorganismos anaerobios Gramnegativos: Bacteroides melaninogenicus. Spirochetes: Borrelia burgdorferi, Treponema pallidum. Campylobacter: Campylobacter jejuni. Un metabolito encontrado en el hombre, 14-OH-claritromicina, tiene significativa actividad antibacteriana. Este metabolito es tan activo o 1 a 2 veces menos activo que el compuesto de origen para la mayoría de los organismos, excepto para H. Influenzae contra el cual es dos veces más activo. El compuesto de origen y el metabolito 14-OH ejercen un efecto aditivo o sinérgico sobre H. influenzae in vitro e in vivo, dependiendo de las cepas bacterianas. Se encontró que la Claritromicina es dos a diez veces más activa que la eritromicina en varios modelos animales experimentales de infección. Se mostró, por ejemplo, ser más efectiva que la eritromicina en infección sistémica del ratón, abscesos subcutáneos del ratón e infecciones de las vías respiratorias del ratón causadas por S. pneumoniae, S. aureus, S. pyogenes y H. influenzae. En cuyes con infección por legionella, este efecto fue más pronunciado; en una dosis intraperitoneal de 1,6 mg/kg/día de claritromicina fue más efectivo que 50 mg/kg/día de eritromicina. Pruebas de Susceptibilidad: Los métodos cuantitativos que requieren medición de diámetros de zona dan los estimados más precisos de susceptibilidad de las bacterias a los agentes antimicrobianos. Un procedimiento recomendado utiliza discos impregnados con 15 mcg de claritromicina para la prueba de susceptibilidad (prueba de difusión Kirby-Bauer); las interpretaciones correlacionan los diámetros de la zona de inhibición de este disco de prueba con los valores CIM para claritromicina. Las CIMs se determinan por método de dilución agar o caldo. Con estos procedimientos, un informe del laboratorio de "susceptible" indica que el microorganismo infectante es probable que responda a la terapia. Un informe de "resistente" indica que el microorganismo infectante no es probable que responda a la terapia. Un informe de "Susceptibilidad Intermedia" sugiere que el efecto terapéutico de la droga puede ser equívoco o que el microorganismo sería susceptible si se usan dosis más altas (lo último también se refiere a moderadamente susceptible). Propiedades Farmacocinéticas: Sujetos normales: En un estudio clínico de dosis única en voluntarios, claritromicina IV se administró en dosis de 75, 125, 250 o 500 mg en un volumen de 100 mL infundido sobre 30 minutos y en dosis de 500, 750 o 1000 mg en un volumen de 250 mL infundidos sobre un período de 60 minutos. La concentración máxima (peak) media (Cmáx) de la droga de origen varió desde 5.16 mcg/ml después de la dosis de 500 mg a 9.40 mcg/ml después de la dosis de 1000 mg (infusión de 60 minutos). La concentración máxima (peak) media (Cmáx) del 14-hidroximetabolito varió desde 0.66 mcg/mL después de la dosis de 500 mg hasta a 1.06 mcg/mL después de la dosis de 1000 mg (infusión de 60 minutos). La media de la vida media plasmática de fase terminal de la droga de origen fue dosis dependiente y varió desde 3.8 horas después de la dosis de 500 mg a 4.5 horas después de la dosis de 1000 mg (infusión de 60 minutos). La media estimada de la vida media plasmática para el 14-hidroximetabolito mostró algunos aumentos dosis dependientes en dosis más altas y varió desde 7.3 horas después de la dosis de 500 mg a 9.3 horas después de la dosis de 1000 mg (infusión de 60 minutos). La media del área bajo la concentración vs. la curva de tiempo (AUC) mostró un aumento no lineal dosis dependiente para la droga de origen de 22.29 h.mcg/mL después de la dosis de 500 mg a 53.26 h.mcg/mL después de la dosis de 1000 mg. La media del área bajo la concentración vs. la curva de tiempo (AUC) para el 14-hidroximetabolito varió desde 8.16 h.mcg/mL después de la dosis de 500 mg a 14.76 h.mcg/mL después de la dosis de 1000 mg (infusión de 60 minutos). En un estudio clínico de siete días de dosis múltiples, los sujetos fueron infundidos con 125 y 250 mg de claritromicina IV en un volumen final de 100 mL sobre un período de 30 minutos o 500 y 750 mg de la formulación en volúmenes finales de 250 mL sobre un período de 60 minutos; la dosis se dio en intervalos de 12 horas. En este estudio, la media observada del estado estable de la concentración máxima (peak) (Cmáx) de claritromicina aumentó de 5.5 mcg/mL con la dosis de 500 mg a 8.6 mcg/mL con la dosis de 750 mg. La media de la vida media terminal aparente fue de 5.3 horas después de la infusión de la dosis de 500 mg sobre un período de 60 minutos y 4.8 horas después de una infusión de 750 mg. La media observada del estado estable de Cmáx para el 14-hidroximetabolito aumentó de 1.02 mcg/mL con la dosis de 500 mg a 1.37 mcg/mL con la dosis de 750 mg. La media de las vidas medias de la fase terminal para este metabolito fue de 7.9 y 5.4 horas para los grupos de dosis de 500 mg y 750 mg, respectivamente. La tendencia no relacionada con la dosis fue evidente. Con la dosificación oral dos veces al día de 250 mg, el estado estable de las concentraciones plasmáticas máximas se lograron en dos a tres días y promediaron cerca de 1 mcg/mL para claritromicina y 0.6 mcg/mL para 14-OH-claritromicina, mientras que las vidas medias de eliminación de la droga de origen y el metabolito fueron de tres a cuatro horas y de cinco a seis horas, respectivamente. Con la dosificación oral dos veces al día de 500 mg, el estado estable de la Cmáx para la claritromicina y su metabolito hidroxilado se logró con la quinta dosis. Después de la quinta y séptima dosis, el estado estable de la Cmáx para la claritromicina promedió 2.7 y 2.9 mcg/mL; su metabolito hidroxilado promedió 0.88 y 0.83 mcg/mL, respectivamente. La vida media de la droga de origen a un nivel de dosis de 500 mg fue de 4.5 a 4.8 horas, mientras que la de la 14-OH-claritromicina fue de 6.9 a 8.7 horas. En estado estable los niveles de 14-OH-claritromicina no aumentaron proporcionalmente con la dosis de claritromicina, y las vidas medias aparentes de tanto la claritromicina como su metabolito hidroxilado tendieron a ser más largas en las dosis más altas. Este comportamiento farmacocinético no lineal de la claritromicina, junto con la disminución general en la formación de productos de 14-hidroxilación y N-demetilación en dosis más altas, indica que el metabolismo de claritromicina se aproxima a la saturación en dosis altas. El principal metabolito en plasma humano fue 14-OH-claritromicina, con niveles máximos de 0.5 mcg/mL y 1.2 mcg/mL después de dosis orales de 250 mg y 1200 mg, respectivamente. En los humanos a los que se les da una dosis oral única de 250 mg o 1200 mg de claritromicina, la excreción urinaria da cuenta del 37.9% de la dosis más baja y 46.0% de la dosis más alta. La eliminación fecal da cuenta del 40.2% y 29.1% (esto incluyó a un sujeto con una sola muestra de deposición que contenía 14.1%) de estas respectivas dosis. Pacientes: La claritromicina y su metabolito 14-OH se distribuyen rápidamente en los tejidos y fluidos del cuerpo. A continuación se presentan ejemplos de concentraciones séricas y de tejidos:

Pacientes con Infecciones Mycobacterianas: Aunque actualmente no existen datos disponibles sobre el uso de claritromicina IV en infecciones mycobacterianas, existen datos farmacocinéticos del uso de los comprimidos de claritromicina en estas infecciones. Las concentraciones estado estable de claritromicina y 14-OH-claritromicina observadas luego de la administración de dosis usuales de claritromicina en pacientes adultos con infección VIH fueron similares a aquellas observadas en sujetos normales. Sin embargo, en las dosis más altas que se pueden requerir para tratar infecciones mycobacterianas, las concentraciones de claritromicina fueron mucho más altas que aquellas observadas en las dosis usuales. Las vidas medias de eliminación parecieron extenderse en estas dosis más altas, en comparación con aquellas observadas con dosis usuales en sujetos normales. Las concentraciones de claritromicina más altas y las vidas medias de eliminación más largas observadas en estas dosis son compatibles con la no linearidad conocida en la farmacocinética de la claritromicina. Datos de seguridad preclínica: Toxicidad Aguda: La DL50 intravenosa de claritromicina IV en ratones se encontró que es de 184 mg/kg y 227 mg/kg en dos estudios separados. Esta fue varias veces más alta que la DL50 en ratas (64 mg base/kg). Estos valores fueron más bajos que aquellos obtenidos a continuación de la administración a ratones por otras vías. Los signos de toxicidad en ambas especies fueron de actividad disminuida, ataxia, espasmos musculares, temblores, disnea y convulsiones. La autopsia y los exámenes histopatológicos de sobrevivientes de un estudio de ratones, en los cuales se obtuvo la DL50 de 184 mg/kg, no mostró cambios asociados con la administración de claritromicina IV. Sin embargo, en otros estudios en ratones y ratas hubo hallazgos gruesos sugerentes de edema pulmonar junto con irregularidades a decoloración difusa rojo oscuro de los lóbulos pulmonares en algunos animales que murieron en forma aguda. Aunque la administración de la droga produjo efectos similares en ambos, ratones y ratas, fue mucho más tóxica para las ratas que para los ratones. No se pudo determinar el modo exacto de toxicidad. Aunque los signos de toxicidad aguda sugirieron efecto en el sistema nervioso central, las necropsias gruesas revelaron cambios pulmonares en algunos ratones y ratas. Las toxicidades intravenosas agudas de varios metabolitos se evaluaron en ratones y se resumen a continuación:

Los signos de toxicidad incluyeron inhibición del movimiento, distréss respiratorio y convulsiones clónicas. Es aparente que las toxicidades de estos metabolitos son comparables a las de la claritromicina tanto en calidad como en grado. Irritación Venosa Aguda: Las soluciones de claritromicina IV se evaluaron para el potencial de causar irritación venosa en la vena marginal de la oreja de conejos. Este estudio demostró que la administración de dosis únicas en muy altas concentraciones (7.5 a 30 mg/base/mL) eran levemente irritantes. Toxicidad SubAguda: Se realizaron estudios de toxicidad subaguda intravenosa durante más de un mes en niveles de dosis de 15, 50 y 160 mg/kg/día en ratas y de 5, 15 y 40 mg base/kg/día en monos. Las dosis máximas utilizadas en los estudios de hallazgo del rango en ratas (rango de 20 a 640 mg/kg/día) y en monos (rango de 5 a 80 mg/kg/día) se encontró que eran sistemáticamente tóxicas para el hígado, sistema biliar y riñones. Estos son los mismos órganos blanco encontrados con estudios en los cuales la claritromicina se administró por vía oral. La ocurrencia de irritación venosa severa en los estudios de un mes en la rata y en el mono con 160 mg/kg y 40 mg/kg, respectivamente, excluyeron el uso de dosis altas suficientes para demostrar claramente la toxicidad del órgano blanco. Esto ocurrió a pesar de los esfuerzos para maximizar la dosis aumentando el volumen de infusión y disminuyendo la tasa de infusión. Las dosis sin efecto en ratas y en monos determinadas por estudios subagudos de un mes fueron de 50 y 15 mg/kg/día, respectivamente, y esto se debió a la irritación venosa a dosis más altas. Embriotoxicidad en Ratas: A ratas se administraron 15, 50 y 160 mg base/kg/día de claritromicina IV vía vena caudal. Se obtuvieron signos significativos de toxicidad materna con 160 mg/kg/día (ganancia de peso disminuida y consumo alimenticio reducido) y con 50 mg/kg/día (consumo alimenticio reducido). Efectos locales del agente de prueba incluyeron hinchazón, moretones, necrosis y pérdida final de una porción de la cola entre los animales con dosis alta. No se observaron efectos sobre las incidencias medias de los sitios de implantación o reabsorciones. No se observaron anormalidades viscerales o esqueléticas debidas a la administración de la droga, excepto para los de tendencia dosis-relacionada en la proporción de fetos machos con un testículo no descendido. De este modo, a pesar de la significativa toxicidad materna, manifestada como irritación venosa y consumo alimenticio reducido y ganancia de peso reducida, no hubo evidencia de embriotoxicidad, embrioletalidad o teratogenicidad en cualquiera de las dosis. Embriotoxicidad en Conejos: A grupos de conejos apareados se les dio claritromicina IV en dosis de 3, 10 y 30 mg base/kg/día. Una madre tratada con 3 mg/kg/día murió al día 29 de la gestación. Se observó irritación venosa en los grupos control y en todos los grupos de tratamiento. La incidencia y severidad de la irritación estuvieron directamente relacionadas con la concentración de la droga en la formulación. Se obtuvieron sígnos de toxicidad materna a los 30 mg/kg/día (reducida ganancia de peso y consumo alimenticio reducido). La incidencia de aborto en los 30 mg/kg/día del grupo en tratamiento fue significativamente más alta que la del grupo control, pero todos los fetos abortados se encontró que eran muy normales. Los niveles inefectivos para la toxicidad materna y fetal fueron de 10 y 30 mg/kg/día, respectivamente. Embriotoxicidad en Monos: La claritromicina ha mostrado producir pérdida embriónica en monos cuando se administra en aproximadamente diez veces el rango superior usual (500 mg dos veces al día) de la dosis oral humana diaria, comenzando el día 20 de gestación. Este efecto se ha atribuido a la toxicidad materna de la droga en dosis muy altas. Un estudio adicional en monas embarazadas con dosificaciones de aproximadamente 2.5 a 5 veces la máxima dosis usual prevista diaria (500 mg dos veces al día) no produjo ningún peligro al conceptus. Mutagenicidad: Se realizaron estudios para evaluar el potencial mutagénico de la claritromicina usando tanto sistemas de prueba con microsomas de hígado de rata activados como no activados (Test de Ames). Los resultados de estos estudios no proporcionaron evidencia de potencial mutagénico en concentraciones de droga de 25 mcg/Placa de Petri o menos. En una concentración de 50 mcg la droga fue tóxica para todas las cepas probadas.
Indicaciones.
La Claritromicina IV se indica cuando se requiere una terapia parenteral para el tratamiento de microorganismos sensibles, en las siguientes condiciones: 1. Infecciones del tracto respiratorio superior. 2. Infecciones del tracto respiratorio inferior. 3. Infecciones de la piel y tejidos blandos. 4. Infecciones mycobacterianas localizadas o diseminadas debido a Mycobacterium avium o Mycobacterium intracellulare. Infecciones localizadas debido a Mycobacterium chelonae, Mycobacterium fortuitum o Mycobacterium kansasii. Nota: Está indicado en pacientes inmunodeprimidos que no responden o no toleran la vía oral.
Dosificación.
La dosificación recomendada de claritromicina IV es de 1.0 g diario, dividido en dos dosis iguales, en cada infusión, después de ulterior dilución con un apropiado diluyente IV, sobre un período de tiempo de 60 minutos. Actualmente no existen datos que apoyen el uso intravenoso de claritromicina en niños. La claritromicina no debe ser dada como un bolo o como una inyección intramuscular. Dosificación en Pacientes con Infecciones Micobacterianas: Aunque actualmente no existen datos referentes al uso de claritromicina IV en pacientes inmunocomprometidos, los datos disponibles se relacionan al uso de claritromicina oral en pacientes infectados con VIH. En infecciones localizadas o diseminadas (M. avium, M. intracellulare, M. chelonae, M. fortuitum, M. kansasii), el tratamiento recomendado en adultos es de 1000 mg/día divididos en dos dosis. La terapia intravenosa se puede limitar por hasta 2 a 5 días en el paciente muy enfermo y se debe cambiar a terapia oral cuando sea posible determinado por el médico. En pacientes con disfunción renal que tienen clearance de creatinina de menos de 30 mL/min, la dosis de claritromicina se debe reducir a una mitad de la dosis normal recomendada. La solución final para infusión se prepara como sigue: Preparar la solución inicial de claritromicina IV agregando 10 mL de Agua Estéril para Inyectables al frasco-ampolla de 500 mg. Usar solamente Agua Estéril para Inyectables, ya que otros diluyentes pueden causar precipitación durante la reconstitución. No usar diluyentes que contengan preservantes o sales inorgánicas. Nota: Cuando el producto se reconstituye como se ha indicado, la solución resultante contiene un efectivo preservante antimicrobiano; cada mL contiene 50 mg de claritromicina IV. La estabilidad en uso física y química se ha demostrado por 48 horas a 5°C y por 24 horas a 25°C. Desde un punto de vista microbiológico, el producto reconstituido se debe usar inmediatamente. Si no es usado inmediatamente, los tiempos y las condiciones de almacenamiento en uso previo a su uso son de responsabilidad del usuario y normalmente no serían más de 24 horas de 2 a 8°C, a menos que la reconstitución/dilución haya tomado lugar en condiciones asépticas validadas y controladas. El producto reconstituido (500 mg en 10 mL de Agua para Inyectables) se debe agregar a un mínimo de 250 mL de uno de los siguientes diluyentes antes de la administración: Dextrosa 5% en Solución Ringer Lactato, Dextrosa 5%, Solución Ringer Lactato, Dextrosa 5% en cloruro de sodio 0.3%, Normosol-M en Dextrosa 5%, Normosol-R en Dextrosa 5%, Dextrosa 5% en cloruro de sodio 0.45% y cloruro de sodio 0.9%. La estabilidad en uso física y química se ha demostrado por 48 horas a 5°C y por 6 horas a 25°C. Desde un punto de vista microbiológico, el producto final diluido se debe usar inmediatamente. Si no es usado inmediatamente, los tiempos y las condiciones de almacenamiento en uso previo a su uso son de responsabilidad del usuario y normalmente no serían más de 24 horas de 2 a 8°C, a menos que la reconstitución/dilución haya tomado lugar en condiciones asépticas validadas y controladas. No se debe agregar droga o agente químico a la claritromicina IV mezcla fluida, a menos que se haya determinado primero su efecto sobre la estabilidad química y física de la solución.
Contraindicaciones.
Claritromicina IV está contraindicada en pacientes con hipersensibilidad conocida a los antibióticos macrólidos. Las reacciones alérgicas o hipersensitivas se deben manejar mediante rápidas medidas de apoyo. La administración concomitante de claritromicina y cualquiera de las siguientes drogas está contraindicada: astemizol, cisaprida, pimozida, terfenadina y ergotamina o dihidroergotamina (ver Interacciones).
Reacciones adversas.
La Tabla 1 muestra los eventos adversos reportados en pacientes a quienes se administró claritromicina IV durante estudios clínicos así como los eventos observados con la formulación oral. Los eventos adversos se muestran por sistema corporal y frecuencia (común ≥1/100, < 1/10).
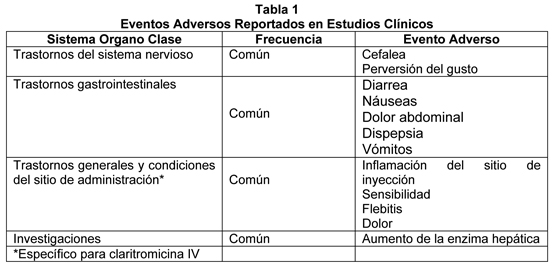
Experiencia Poscomercialización: La claritromicina se comercializa en varias formulaciones diferentes. La Tabla 2 es una recopilación de
reacciones adversas para todas las formulaciones incluyendo claritromicina IV. Debido a que estas reacciones se reportan voluntariamente desde una población de tamaño incierto, no siempre es posible estimar de buena fuente su frecuencia o establecer una relación causal con la exposición a la droga. La exposición del paciente se estima ser mayor que 1 billón de días de tratamiento-paciente para claritromicina.
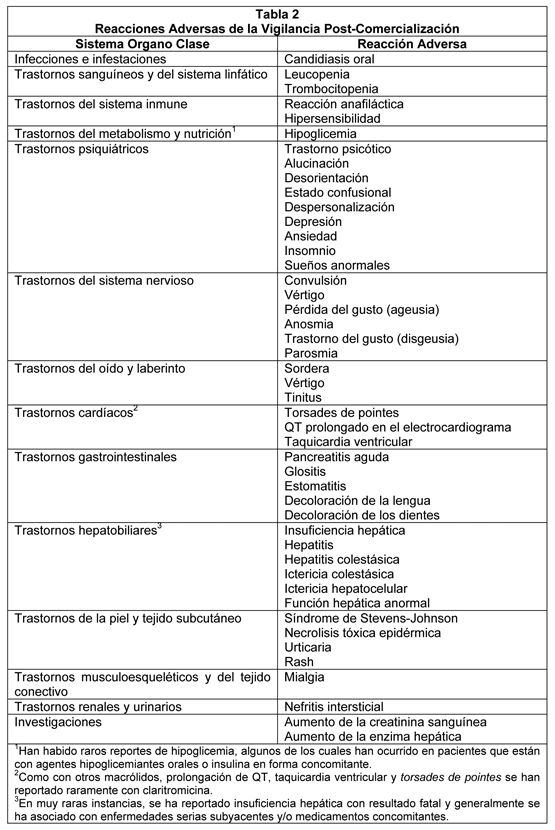
Existen reportes poscomercialización de toxicidad a colchicina con el uso concomitante de claritromicina y colchicina, especialmente en los mayores, algunos ocurrieron en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones: Colchicina y Advertencias). Pacientes inmunocomprometidos: Aunque actualmente no existen datos en relación al uso de claritromicina IV en esta población de pacientes, los datos disponibles se relacionan al uso de claritromicina oral en pacientes infectados con VIH. En pacientes con SIDA y otros inmunocomprometidos tratados con las dosis orales más altas de claritromicina por períodos largos de tiempo por infecciones micobacterianas, a menudo fue difícil distinguir eventos adversos posiblemente asociados con la administración de claritromicina de signos subyacentes de enfermedad por VIH o enfermedad intercurrente. En pacientes adultos, los eventos adversos más frecuentemente reportados por pacientes tratados con dosis diarias orales totales de 1000 mg de claritromicina fueron: náuseas, vómitos, alteración del gusto, dolor abdominal, diarrea, rash, flatulencia, cefalea, constipación, problemas de audición, elevaciones de SGOT y SGPT. Eventos adicionales de baja frecuencia incluyeron disnea, insomnio y boca seca. En estos pacientes inmunocomprometidos la evaluación de los valores de laboratorio se hicieron analizando aquellos valores seriamente fuera del nivel anormal (por ej. el extremo alto o el límite bajo) para el test específico. Basados en este criterio, alrededor del 2% a 3% de estos pacientes que recibieron 1000 mg de claritromicina diariamente tuvieron niveles elevados anormales de SGOT y SGPT, y conteo de glóbulos blancos y plaquetas anormalmente bajos. Un menor porcentaje de pacientes también tuvieron niveles elevados de BUN.
Advertencias.
El médico no debe prescribir claritromicina IV a mujeres embarazadas sin ponderar cuidadosamente los beneficios versus riesgo, especialmente durante los tres primeros meses de embarazo. El uso a largo plazo puede, como con otros antibióticos, producir colonización bacteriana con aumento del número de bacterias no susceptibles y hongos. Si ocurre sobreinfección, se debe instituir una terapia apropiada. Se ha informado de colitis seudomembranosa con prácticamente todos los agentes antibacterianos, incluyendo macrólidos y la severidad puede variar desde leve hasta el riesgo vital. Se ha reportado diarrea asociada con Clostridium difficile (CDAC) con el uso de prácticamente todos los agentes antibacterianos incluyendo claritromicina y la severidad puede variar desde diarrea leve hasta colitis fatal. El tratamiento con agentes antibacterianos altera la flora normal del colon, lo cual puede llevar a un sobrecrecimiento de C. difficile. La CDAC se debe considerar en todos los pacientes que presentan diarrea después del uso de antibiótico. Es necesario hacer una historia médica cuidadosa ya que CDAC se ha reportado que ocurre sobre dos meses después de la administración de agentes antibacterianos. Se ha reportado exacerbación de síntomas de miastenia gravis en pacientes que recibían terapia con claritromicina. La claritromicina es excretada principalmente por el hígado. Se debe tener precaución en la administración del antibiótico a pacientes con función hepática alterada. También se debe tener precaución cuando se administra claritromicina a pacientes con daño renal moderado a severo. Colchicina: Han existido reportes poscomercialización de toxicidad por colchicina con el uso concomitante de claritromicina y colchicina, especialmente en los mayores, algunos de los cuales ocurrió en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones: Colchicina). También se debe prestar atención a la posibilidad de resistencia cruzada entre la claritromicina y otros macrólidos, así como con lincomicina y clindamicina.
Interacciones.
El uso de las siguientes drogas está estrictamente contraindicado debido al potencial para efectos severos por interacción de droga: Se han reportado niveles elevados de cisaprida en pacientes que reciben claritromicina y cisaprida concomitantemente. Esto puede producir prolongación de QT y arritmias cardíacas incluyendo taquicardia ventricular, fibrilación ventricular y torsades de pointes. Efectos similares se han observado en pacientes que toman claritromicina y pimozida concomitantemente (ver Contraindicaciones). Se ha reportado que los macrólidos alteran el metabolismo de la terfenadina produciendo aumento de los niveles de terfenadina que ocasionalmente se ha asociado con arritmias cardíacas tales como prolongación de QT, taquicardia ventricular, fibrilación ventricular y torsades de pointes (ver Contraindicaciones). En un estudio en 14 voluntarios sanos, la administración concomitante de claritromicina (comprimidos) y terfenadina produjo aumento de dos a tres veces en el nivel sérico del metabolito ácido de la terfenadina y prolongación del intervalo QT que no llevó a ningún efecto clínicamente detectable. Efectos similares se han observado con la administración concomitante de astemizol y otros macrólidos. Ergotamina/dihidroergotamina: Reportes poscomercialización indican que la coadministración de claritromicina con ergotamina o dihidroergotamina se ha asociado con toxicidad aguda al ergot caracterizada por vasoespasmo e isquemia de las extremidades y otros tejidos incluyendo el sistema nervioso central. La administración concomitante de claritromicina y estos productos medicinales está contraindicada (ver Contraindicaciones). Efectos de Otros Productos Medicinales sobre la Claritromicina: Se conoce o sospecha que las siguientes drogas afectan las concentraciones circulantes de claritromicina; se puede requerir ajuste de dosis de claritromicina o consideración de tratamientos alternativos. Efavirenz, nevirapina. rifampicina, rifabutina y rifapentina: Fuertes inductores del metabolismo del sistema citocromo P450 tales como efavirenz, nevirapina, rifampicina, rifabutina y rifapentina pueden acelerar el metabolismo de la claritromicina y entonces disminuir los niveles plasmáticos de claritromicina, mientras aumentan los de 14(R)-hidroxi-claritromicina (14-OH-claritromicina), un metabolito que también es microbiológicamente activo. Dado que las actividades microbiológicas de claritromicina y 14-OH-claritromicina son diferentes para diferentes bacterias, el efecto terapéutico deseado podría estar deteriorado durante la administración concomitante de claritromicina e inductores de enzima. Fluconazol: La administración concomitante de fluconazol 200 mg diarios y claritromicina 500 mg dos veces al día a 21 voluntarios sanos llevó a incrementos en la concentración mínima estado estable (Cmín) de claritromicina y en el área bajo la curva (AUC) de 33% y 18%, respectivamente. Las concentraciones estado estable del metabolito activo 14-OH-claritromicina no se afectaron significativamente por la administración concomitante de fluconazol. No es necesario ajustar la dosis de claritromicina. Ritonavir: Un estudio farmacocinético demostró que la administración concomitante de ritonavir 200 mg cada ocho horas y claritromicina 500 mg cada 12 horas produjo una marcada inhibición del metabolismo de la claritromicina. La Cmáx de la claritromicina aumentó en 31%, Cmín aumentó 182% y AUC aumentó en 77% con la administración concomitante de ritonavir. Se observó una inhibición esencialmente completa de la formación de 14-OH-claritromicina. Debido a la amplia ventana terapéutica para claritromicina, no debe ser necesaria una reducción de la dosis en pacientes con función renal normal. Sin embargo, para pacientes con deterioro renal, se deben considerar los siguientes ajustes de dosis: Para pacientes con clearance de creatinina 30 a 60 mL/min la dosis de claritromicina se debe disminuir en 50%. Para pacientes con clearance de creatinina < 30 mL/min la dosis de claritromicina se debe disminuir en 75%. Dosis de claritromicina mayores de 1 g/día no se deben coadministrar con ritonavir. Efectos de Claritromicina sobre Otros Productos Medicinales: Antiarrítmicos: Existen reportes poscomercialización de torsades de pointes que ocurrieron con el uso concurrente de claritromicina y quinidina o disopiramida. Se deben monitorear los electrocardiogramas por prolongación de QTc durante la coadministración de claritromicina con estas drogas. Los niveles séricos de estos medicamentos se deben monitorear durante la terapia con claritromicina. Interacciones basadas en CYP3A: La coadministración de claritromicina, que se conoce que inhibe CYP3A y una droga metabolizada principalmente por CYP3A se puede asociar con elevaciones en las concentraciones de droga que podrían aumentar o prolongar tanto los efectos terapéuticos como los adversos de la droga concomitante. La claritromicina se debe usar con precaución en pacientes que reciben tratamiento con otras drogas que se conoce son sustratos de la enzima CYP3A, especialmente si el sustrato de CYP3A tiene un margen de seguridad estrecho (ej., carbamazepina) y/o el sustrato se metaboliza extensamente por esta enzima. Se pueden considerar ajustes de dosis y cuando sea posible, se deben monitorear de cerca las concentraciones séricas de drogas metabolizadas principalmente por CYP3A en pacientes que reciben claritromicina concurrentemente. Las siguientes drogas o clases de drogas son conocidas o se sospecha que se metabolizan mediante la misma isoenzima CYP3A: alprazolam, astemizol, carbamazepina, cilostazol, cisaprida, ciclosporina, disopiramida, alcaloides del ergot, lovastatina, metilprednisolona, midazolam, omeprazol, anticoagulantes orales (ej. warfarina), pimozida, quinidina, rifabutina, sildenafil, simvastatina, tacrolimus, terfenadina, triazolam y vinblastina. Las drogas que interactúan mediante mecanismos similares a través de otras isoenzimas dentro del sistema citocromo P450 incluyen fenitoína, teofilina y valproato. Inhibidores de HMG-CoA Reductasa: Como con otros macrólidos, se ha reportado que la claritromicina aumenta las concentraciones de inhibidores de la HMG-CoA reductasa (ej., lovastatina y simvastatina). Raros reportes de rabdomiólisis se han informado en pacientes que toman estas drogas concomitantemente. Omeprazol: Se entregó claritromicina (500 mg cada 8 horas) en combinación con omeprazol (40 mg diarios) a sujetos adultos sanos. Las concentraciones plasmáticas estado estable de omeprazol se aumentaron (Cmáx, AUC0-24 y t½ aumentaron en 30%, 89% y 34%, respectivamente), por la administración concomitante de claritromicina. La media del valor de pH gástrico de 24-horas fue 5.2 cuando el omeprazol se administró solo y 5.7 cuando el omeprazol se coadministró con claritromicina. Anticoagulantes orales: Reportes espontáneos en el período post-comercialización sugieren que la administración concomitante de claritromicina y anticoagulantes orales puede potenciar los efectos de los anticoagulantes orales. Se deben monitorear cuidadosamente los tiempos de protrombina mientras los pacientes estén recibiendo claritromicina y anticoagulantes orales simultáneamente. Sildenafil, tadalafil y vardenafil: Cada uno de estos inhibidores de fosfodiesterasa se metaboliza, al menos en parte, por CYP3A y el CYP3A puede ser inhibido por la claritromicina administrada concomitantemente. La coadministración de claritromicina con sildenafil, tadalafil o vardenafil produciría probablemente un aumento de la exposición al inhibidor de fosfodiesterasa. Se debe considerar reducción de las dosis de sildenafil, tadalafil y vardenafil cuando estas drogas son coadministradas con claritromicina. Teofilina, carbamazepina: Los resultados de los estudios clínicos indican que hubo un modesto pero estadísticamente significativo (p≤0.05) aumento de los niveles circulantes de teofilina o carbamazepina cuando cualquiera de estas drogas fueron administradas concomitantemente con claritromicina oral. Tolterodina: La principal vía del metabolismo de la tolterodina es vía la isoforma 2D6 del citocromo P450 (CYP2D6). Sin embargo, en un subgrupo de la población que carece de CYP2D6, la ruta identificada para el metabolismo es vía CYP3A. En este sub-grupo de población, la inhibición de CYP3A produce un significativo aumento en las concentraciones séricas de tolterodina. Puede ser necesaria una reducción de la dosis de tolterodina en presencia de inhibidores de CYP3A, tales como claritromicina en la población que es pobre metabolizador de CYP2D6. Triazolobenzodiazepinas (ej., alprazolam, midazolam, triazolam): Cuando se coadministra midazolam con claritromicina comprimidos (500 mg dos veces al día), el AUC de midazolam se incrementó 2.7 veces después de la administración oral. La administración concomitante de midazolam oral y claritromicina se debe evitar. Si se coadministra midazolam intravenoso con claritromicina, el paciente se debe monitorear cuidadosamente para permitir el ajuste de dosis. Las mismas precauciones también se deben aplicar a otras benzodiazepinas que son metabolizadas por CYP3A, incluyendo triazolam y alprazolam. Para las benzodiazepinas que no son dependientes del CYP3A para su eliminación (temazepam, nitrazepam, lorazepam), no es probable que ocurra una interacción clínicamente importante con claritromicina. Existen reportes postcomercialización de interacciones de droga y efectos en el sistema nervioso central (SNC) (ej, somnolencia y confusión) con el uso concomitante de claritromicina y triazolam. Se sugiere monitorear al paciente para aumento de efectos farmacológicos en el SNC. Interacciones de Otras Drogas: Colchicina: La colchicina es un sustrato tanto para CYP3A como para el eflujo transportador, P-glucoproteína (Pgp). La claritromicina y otros macrólidos son conocidos inhibidores de CYP3A y Pgp. Cuando claritromicina y colchicina se administran juntos, la inhibición de Pgp y/o CYP3A por la claritromicina puede llevar a aumento de la exposición a colchicina. Se deben monitorear los pacientes por síntomas clínicos de toxicidad a colchicina (ver Advertencias). Digoxina: Se piensa que la digoxina es un sustrato para el eflujo transportador, P-glucoproteína (Pgp). Se conoce que la claritromicina inhibe Pgp. Cuando claritromicina y digoxina se administran juntos, la inhibición de Pgp por la claritromicina puede llevar a un aumento de la exposición a digoxina. Concentraciones séricas elevadas de digoxina en pacientes que reciben claritromicina y digoxina concomitantemente también se han reportado en la vigilancia poscomercialización. Algunos pacientes han mostrado signos clínicos compatibles con toxicidad a digoxina, incluyendo arritmias potencialmente fatales. Las concentraciones séricas de digoxina se deben monitorear cuidadosamente mientras los pacientes estén recibiendo digoxina y claritromicina simultáneamente. Zidovudina: La administración oral simultánea de claritromicina en comprimidos y zidovudina en pacientes adultos infectados con VIH puede producir una disminución de las concentraciones estado estable de zidovudina. Esta interacción no parece ocurrir en pacientes pediátricos infectados con VIH que toman una formulación de claritromicina en suspensión concurrentemente con zidovudina o dideoxinosina. Debido a que la claritromicina parece interferir con la absorción en adultos administrados simultáneamente con zidovudina oral, esta interacción probablemente no sería un problema cuando la claritromicina se administra intravenosamente. Interacciones Bidireccionales de Droga: Atazanavir: Tanto claritromicina como atazanavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bidireccional de droga. La coadministración de claritromicina (500 mg dos veces al día) con atazanavir (400 mg una vez al día) produjo un aumento de 2 veces en la exposición a claritromicina y un 70% de disminución en la exposición a 14-OH-claritromicina, con un 28% de aumento en el AUC de atazanavir. Debido a la amplia ventana terapéutica para claritromicina, no es necesario hacer reducción de dosis en pacientes con función renal normal, Para pacientes con función renal moderada (clearance de creatinina 30 a 60 mL/min), la dosis de claritromicina se debe disminuir en 50%. Para los pacientes con clearance de creatinina < 30 mL/min, la dosis de claritromicina se debe disminuir en 75% usando una formulación adecuada de claritromicina. Dosis de claritromicina mayores de 1000 mg por día no se deben coadministrar con inhibidores de proteasa. Itraconazol: Tanto claritromicina como itraconazol son sustratos e inhibidores de CYP3A, llevando a una interacción bidireccional de droga. La claritromicina puede aumentar los niveles plasmáticos de itraconazol, mientras que itraconazol puede aumentar los niveles plasmáticos de claritromicina. Los pacientes que toman itraconazol y claritromicina concomitantemente se deben monitorear cuidadosamente por signos o síntomas de aumento o prolongación del efecto farmacológico. Saquinavir: Tanto claritromicina como saquinavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bidireccional de droga. La administración concomitante de claritromicina (500 mg dos veces al día) y saquinavir (cápsulas de gelatina blanda, 1200 mg tres veces al día) a 12 voluntarios sanos produjo valores estado estable de AUC y Cmáx de saquinavir, los cuales eran 177% y 187% más altos que aquellos observados con saquinavir solo, Los valores de AUC y Cmáx de claritromicina eran aproximadamente 40% mayores que aquellos observados con claritromicina sola. No se requiere ajuste de dosis cuando las dos drogas se coadministran por un tiempo limitado en las dosis/formulaciones estudiadas. Observaciones de estudios de interacción de droga usando la formulación de cápsula de gelatina blanda pueden no ser representativos de los efectos observados usando la cápsula de gelatina dura de saquinavir. Observaciones de estudios de interacción de droga realizados con saquinavir solo pueden no ser representativos de los efectos observados con la terapia con saquinavir/ritonavir. Cuando saquinavir se coadministra con ritonavir, se debe tener en consideración los efectos potenciales de ritonavir sobre claritromicina (ver Interacciones de droga). Verapamil: Se han observado hipotensión, bradiarritmias y acidosis láctica en pacientes que toman claritromicina y verapamil concomitantemente. En este momento no se han llevado a cabo estudios clínicamente relevantes dirigidos a la compatibilidad física de la claritromicina con otras mezclas intravenosas. Embarazo: No se ha establecido la seguridad de claritromicina IV durante el embarazo. Lactancia: No se ha establecido la seguridad de claritromicina IV durante la lactancia de niños. La claritromicina es excretada en la leche humana.
Conservación.
La claritromicina IV se debe almacenar a temperatura ambiente (menos de 30°C) y protegida de la luz.
Sobredosificación.
En caso de sobredosificación, la claritromicina IV se debe discontinuar y se deben establecer todas las otras medidas apropiadas de apoyo. Informes indican que con la ingestión de grandes cantidades de claritromicina se puede esperar que ocurran síntomas gastrointestinales. Un paciente que tenía una historia de trastorno bipolar ingirió 8 g de claritromicina comprimidos y mostró estado mental alterado, comportamiento paranoico, hipokalemia e hipoxemia. Las reacciones adversas que acompañan una sobredosis se deben tratar con la pronta eliminación de la droga no absorbida y medidas de apoyo. Como con otros macrólidos, no se espera que los niveles séricos de claritromicina sean afectados en forma importante por la hemodiálisis o diálisis peritoneal.
Presentación.
Claritromicina IV 50 mg/mL se suministra en un estuche que contiene un frasco-ampolla de vidrio claro de 30 mL de capacidad que contiene el polvo liofilizado más una ampolla de vidrio que contiene 10 mL de agua estéril para inyectable.
KLARICID
ABBOTT
Pediátrico gránulos para suspensión oral
Antibiótico.
Descripción.
Claritromicina Suspensión Pediátrica es una forma de dosificación oral de claritromicina para uso principalmente en niños. La claritromicina es un antibiótico macrólido semisintético obtenido por substitución de un grupo CH3O por el grupo hidroxilo (OH) en posición 6 del anillo lactónico de la eritromicina. Específicamente la claritromicina es 6-O-metil eritromicina A. El antibiótico es un polvo blanco a blanquecino, prácticamente inodoro, esencialmente insoluble en agua y ligeramente soluble en etanol, metanol y acetonitrilo. Su peso molecular es 747,96. Claritromicina Suspensión Pediátrica consiste de una granulación de claritromicina y Carbopol, el cual está cubierto con polímero HP-55 (ftalato metilcelulosa hidroxipropilo). Los gránulos recubiertos son mezclados con una combinación de ingredientes inactivos, tales como sucrosa, goma de xantano, dióxido de silicio, sorbato de potasio, ácido cítrico, maltodextrina, dióxido de titanio, saborizantes, povidona, aceite de ricino. Se agrega agua para reconstituir la suspensión antes de su uso. Después de la mezcla, cada 5 mL de los gránulos para suspensión contienen 250 mg de claritromicina. Consulte su Fórmula de Fabricación Internacional aprobada para los ingredientes específicos.
Farmacología.
Propiedades Farmacodinámicas: Microbiología: Claritromicina ejerce su acción antibacteriana ligándose a las sub-unidades ribosomales 50S de las bacterias susceptibles y suprime la síntesis de proteínas. Claritromicina ha demostrado una excelente actividad in vitro, tanto contra las cepas bacterianas estándar como contra aislados clínicos. Es altamente potente contra una amplia variedad de organismos aerobios y anaerobios Gram-positivos y Gram-negativos. Las concentraciones inhibitorias mínimas (CIMs) de la claritromicina son generalmente una dilución log2 más potentes que las CIMs de la eritromicina. Los datos in vitro también indican que la claritromicina tiene excelente actividad contra la Legionella pneumophila, Mycoplasma pneumoniae y Helicobacter (Campylobacter) pylori. Los datos in vitro e in vivo muestran que este antibiótico tiene actividad clínicamente significativa contra las especies micobacterianas. Los datos in vitro indican que la Enterobacteriaceae, especies pseudomonas y otros bacilos Gram-negativos que no fermentan lactosa no son susceptibles a claritromicina. Claritromicina ha mostrado ser activa contra la mayoría de las cepas de los siguientes microorganismos tanto in vitro como en infecciones clínicas como está descrito en la sección Indicaciones. Microbiologia: Microorganismos Aerobios Gram-positivos: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes. Microorganismos Aerobios Gram-negativos: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis. Otros microorganismos: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR). Micobacterias: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) que consisten de: Mycobacterium avium, Mycobacterium intracellulare. La producción de Beta-lactamasa no debe tener efecto en la actividad de la claritromicina. Nota: La mayoría de las cepas de estafilococos resistentes a la meticilina y oxacilina son resistentes a claritromicina. Helicobacter: Helicobacter pylori. En cultivos llevados a cabo antes de la terapia, el H. pylori fue aislado y las CIMs de la claritromicina se determinaron en 104 pacientes pre-tratamiento. De estos, cuatro pacientes tuvieron cepas resistentes, dos pacientes tenían cepas con susceptibilidad intermedia y 98 pacientes tenían cepas susceptibles. Los siguientes datos in vitro se encuentran disponibles, pero su significancia clínica es desconocida. La claritromicina in vitro exhibe actividad contra la mayoría de las cepas de los siguientes microorganismos; sin embargo, la seguridad y efectividad de la claritromicina en el tratamiento de infecciones clínicas debido a estos microorganismos no se ha establecido en estudios clínicos adecuados y bien controlados. Microorganismos aerobios Gram-positivos: Streptococcus agalactiae, Estreptococci (Grupo C, F, G), Estreptococci grupo Viridans. Microorganismos aerobios Gram-negativos: Bordetella pertussis, Pasteurella multocida. Microorganismos anaerobios Gram-positivos: Clostridium perfringens, Peptococcus niger, Propionibacteruim acnes. Microorganismos anaerobios Gram-negativos: Bacteroides melaninogenicus. Spirochetas: Borrelia burgdorferi, Treponema pallidum. Campylobacter: Campylobacter jejuni. El principal metabolito de claritromicina en el hombre y otros primates es un metabolito microbiológicamente activo, 14-OH-claritromicina. Este metabolito es tan activo o 1 a 2 veces menos activo que el compuesto padre para la mayoría de los organismos, excepto para H. Influenzae contra el cual es dos veces más activo. El compuesto padre y el metabolito 14-OH ejercen un efecto aditivo o sinérgico sobre H. influenzae in vitro e in vivo, dependiendo de las cepas bacterianas. Se encontró que la Claritromicina es dos a diez veces más activa que la eritromicina en varios modelos experimentales animales de infección. Se mostró, por ejemplo, ser más efectivo que la eritromicina en infección sistémica de ratón, abscesos subcutáneos de ratón e infecciones de las vías respiratorias del ratón causadas por S. pneumoniae, S. aureus, S. pyogenes y H. influenzae. En cuyes con infección por Legionella, este efecto fue más pronunciado, en una dosis intraperitoneal de 1,6 mg/kg/día de claritromicina fue más efectiva que 50 mg/kg/día de eritromicina. Pruebas de Susceptibilidad: Los métodos cuantitativos que requieren medición de diámetros de zona dan los estimados más precisos de susceptibilidad antibiótica. Un procedimiento recomendado utiliza discos impregnados con 15 mcg de claritromicina para la prueba de susceptibilidad, las interpretaciones correlacionan los diámetros de zona de este disco de prueba con los valores CIM para claritromicina. Las CIMs se determinan por el método de dilución agar o caldo. Con este procedimiento, un informe del laboratorio susceptible indica que el organismo infectante probablemente va a responder a la terapia. Un informe de resistente indica que el organismo infectante probablemente no va a responder a la terapia. Un informe de "susceptibilidad intermedia" sugiere que el efecto terapéutico de la droga puede ser equívoco o que el organismo sería susceptible si se usan dosis más altas (lo último también se refiere a moderadamente susceptible). Propiedades Farmacocinéticas: Los datos farmacocinéticos iniciales se obtuvieron con formulaciones de claritromicina en tabletas. Estos datos indicaron que la droga es rápidamente absorbida del tracto gastrointestinal y la biodisponibilidad absoluta de una tableta de claritromicina de 50 mg fue de aproximadamente 50%. Tanto al inicio de la absorción como de la formación del metabolito antimicrobiano activo, la claritromicina 14-0H, se retardaron levemente por los alimentos, pero la extensión de la biodisponibilidad no se afectó por la administración de la droga en estado de no ayuno. In vitro: Los estudios in vitro mostraron que la unión de la claritromicina a las proteínas en el plasma humano promedió alrededor del 70% en concentraciones clínicamente relevantes de 0,45 a 4,5 mcg/mL. Sujetos normales: Se investigó la biodisponibilidad y farmacocinética de la Claritromicina Suspensión Pediátrica, en pacientes pediátricos y sujetos adultos. En un estudio de dosis única en sujetos adultos se encontró una biodisponibilidad total de la formulación pediátrica equivalente a o levemente mayor que la del comprimido (con cada dosis de 250 mg). Como con el comprimido, la administración de la formulación pediátrica junto con alimentos conduce a una leve demora en el inicio de la absorción, pero no afecta la biodisponibilidad total de claritromicina. El Cmáx, ABC y T ½ de claritromicina comparativo para la formulación pediátrica (estado de no ayuno) fueron 0,95 mcg/mL, 6,5 mcg hr/mL y 3,7 horas, respectivamente, y para el comprimido de 250 mg (estado de ayuno) fueron de 1,10 mcg/mL, 6,3 mcg hr/mL y 3,3 horas, respectivamente. En un estudio con dosis múltiple en el cual se administraron 250 mg de Claritromicina Suspensión Pediátrica a sujetos adultos cada 12 horas, los niveles sanguíneos estado estable se alcanzaron cerca del tiempo de la quinta dosis. Los parámetros farmacocinéticos después de la quinta dosis para Claritromicina Suspensión Pediátrica fueron: Cmáx 1,98 mcg/mL, ABC 11,5 mcg hr/mL, Tmáx 2,8 horas y T½ 3,2 horas para claritromicina, y 0,67, 5,33, 2,9 y 4,9 respectivamente, para 14-0H-claritromicina. En sujetos humanos sanos en ayuno, las concentraciones séricas máximas se lograron dentro de las dos horas después de la dosis oral. Con dosis dos veces al día usando un comprimido de 250 mg cada 12 horas, las concentraciones séricas máximas estado estable de claritromicina se lograron en dos a tres días y fueron aproximadamente de 1 mcg/mL. Las concentraciones séricas máximas correspondientes fueron 2 a 3 mcg/mL con una dosis de 500 mg administrada cada 12 horas. La vida media de eliminación de claritromicina fue alrededor de tres a cuatro horas con un comprimido de 250 mg administrado cada 12 horas pero aumentó a cinco a siete horas con 500 mg administrados cada 12 horas. El metabolito principal, 14-OH-claritromicina, logra una concentración máxima estado estable de alrededor de 0,6 mcg/mL y tiene una vida media de eliminación de cinco a seis horas después de una dosis de 250 mg cada 12 horas. Con una dosis de 500 mg cada 12 horas, las concentraciones máximas estado estable de 14-OH-claritromicina son levemente más altas (hasta 1 mcg/mL), y su vida media de eliminación es de alrededor de siete horas. Con cualquier dosis, la concentración estado estable de este metabolito generalmente se alcanza dentro de dos a tres días. Aproximadamente 20% de una dosis oral de 250 mg cada 12 horas se excreta en la orina como claritromicina sin cambios. Después de una dosis de 500 mg cada 12 horas, la excreción urinaria de la droga padre sin cambio es de aproximadamente 30%. Sin embargo, el clearance renal de claritromicina es relativamente independiente del tamaño de la dosis y se aproxima a la tasa de filtración glomerular normal. El metabolito principal encontrado en la orina es la 14-OH-claritromicina la cual es responsable de un adicional de 10% a 15% de una dosis de 250 o 500 mg administrada cada 12 horas. Pacientes: La claritromicina y su 14-OH metabolito se distribuyen rápidamente en los tejidos y fluidos del cuerpo. Las concentraciones en los tejidos son usualmente varias veces más altas que las concentraciones séricas. Ejemplos de concentraciones séricas y del tejido se presentan a continuación:
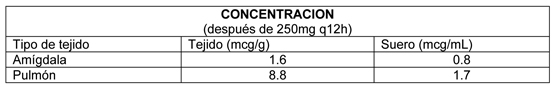
En pacientes pediátricos que requerían tratamiento antibiótico oral, la claritromicina demostró buena biodisponibilidad con un perfil farmacocinético consistente con resultados previos en sujetos adultos que usaron la misma formulación de suspensión. Los resultados indicaron una rápida y extensa absorción de la droga en los niños y, excepto por una leve demora en el inicio de la absorción, los alimentos parecieron no afectar significativamente la biodisponibilidad de la droga o perfiles farmacocinéticos. Los parámetros farmacocinéticos estado estable obtenidos después de la novena dosis en el día cinco de tratamiento fueron como sigue para la droga padre: Cmáx 4,60 mcg/mL, ABC 15,7 mcg/hr/mL y Tmáx 2,8 hr; los valores correspondientes para el 14-OH metabolito fueron: 1,64 mcg/mL, 6,69 mcg/hr/mL y 2,7 hrs., respectivamente. La vida media de eliminación se estimó en aproximadamente 2,2 hrs. y 4,3 hrs. para el compuesto padre y el metabolito, respectivamente. En otro estudio, se obtuvo información con respecto a la penetración de la claritromicina en el fluido del oído medio en pacientes con otitis media. Aproximadamente 2,5 horas después de recibir la quinta dosis (dosis de 7,5 mcg/kg dos veces al día), la concentración media de claritromicina fue de 2,53 mcg/g de fluido en el oído medio y para el 14-OH metabolito fue de 1,27 mcg/g. Generalmente, las concentraciones de la droga padre y el 14-OH metabolito fueron dos veces más altas que las concentraciones séricas correspondientes. Daño Hepático: Las concentraciones estado estables de claritromicina en sujetos con función hepática alterada no fue diferente de aquellas de los sujetos normales; sin embargo, las concentraciones de 14-OH-claritromicina fueron más bajas en los sujetos con daño hepático. La formación disminuida de 14-OH-claritromicina fue al menos parcialmente compensada por un aumento en el clearance renal de claritromicina en los sujetos con función hepática alterada cuando se comparó con sujetos sanos. Daño Renal: La farmacocinética de la claritromicina también se encontró alterada en sujetos con función renal alterada que recibieron múltiples dosis orales de 500 mg. Los niveles plasmáticos, vida media, Cmáx y Cmín tanto para claritromicina como para su 14-OH metabolito fueron más altos y el ABC fue más amplio en sujetos con daño renal que en sujetos normales. La extensión en que estos parámetros difirieron se correlacionó con el grado de daño renal; mientras más severo el daño renal, la diferencia es más significativa (ver Dosificación). Sujetos Ancianos: En un estudio comparativo en adultos jóvenes, sanos y sujetos ancianos, sanos a los que se les administró dosis múltiples de 500 mg orales de claritromicina, los niveles plasmáticos circulantes fueron más altos y la eliminación fue más lenta en el grupo de ancianos comparado con el grupo más joven. Sin embargo, no hubo diferencia entre los dos grupos cuando el clearance renal de claritromicina se correlacionó con el clearance de creatinina. De estos resultados se concluyó que ningún efecto en el manejo de la claritromicina se relaciona con la función renal ni con la edad del sujeto. Pacientes con Infecciones Micobacterianas: Las concentraciones estado estable de claritromicina y 14-OH-claritromicina observadas después de la administración de dosis usuales en pacientes con infección VIH (comprimidos para adultos; suspensión granular para niños) fueron similares a aquellas observadas en sujetos normales. Sin embargo, con las dosis más altas que se pueden requerir para tratar las infecciones micobacterianas, las concentraciones de claritromicina pueden ser mucho más altas que aquellas observadas en las dosis usuales. En niños infectados con VIH que toman 15 a 30 mg/kg/día de claritromicina divididas en dos dosis, generalmente los valores Cmáx estado estables variaron desde 8 a 20 mcg/mL. Sin embargo, se han observado valores Cmáx tan altos como 23 mcg/mL en pacientes pediátricos infectados con VIH que toman 30 mg/kg/día divididas en dos dosis de Claritromicina Suspensión Pediátrica. Las vidas medias de eliminación parecieron ser más largas con estas dosis más altas en comparación con aquellas observadas con dosis usuales en sujetos normales. Las concentraciones plasmáticas más altas y las vidas medias de eliminación más largas observadas en estas dosis son consistentes con la conocida farmacocinética no lineal de claritromicina. Datos de seguridad pre-clínica: Estudios de Toxicidad Oral Aguda y Subcrónica: Los valores LD50 orales agudos para claritromicina suspensión administrada en ratones de 3 días fueron 1290 mg/kg para machos y 1230 mg/kg para hembras. Los valores LD50 en ratas de 3 días fueron 1330 mg/kg para machos y 1270 mg/kg para hembras. Para la comparación, el LD50 de claritromicina administrada oralmente es alrededor de 2700 mg/kg para ratones adultos y aprox. 3000 mg/kg para ratas adultas. Estos resultados son consistentes con otros antibióticos del grupo de penicilinas, grupo cefalosporinas y grupo macrólidos en que el LD50 es generalmente más bajo en animales jóvenes que en adultos. Tanto en ratones como en ratas, se redujo el peso corporal o su aumento se suprimió y el comportamiento de succión y los movimientos espontáneos se deprimieron los primeros días después de la administración de la droga. La necropsia de los animales que murieron mostraron pulmones rojo oscuro en ratones y en alrededor del 25% de las ratas, las ratas tratadas con 2197 mg/kg o más de claritromicina suspensión también mostraron tener una sustancia rojiza a negra en los intestinos, probablemente debida a sangrado. Las muertes de estos animales se consideraron debido a la debilidad resultante de la supresión del comportamiento de succión o el sangrado de los intestinos. A ratas pre-destetadas (cinco días de edad) se les administró la formulación de claritromicina suspensión por dos semanas en dosis de 0, 15, 55 y 200 mg/kg/día. Los animales del grupo de 200 mg/kg/día habían disminuido su peso corporal, disminuido los valores de hemoglobina media y hematocrito, y aumentado los pesos medios relativos de los riñones comparado con los animales del grupo control. También se observó una mínima a leve degeneración vacuolar multifocal del epitelio de los ductos biliares intrahepáticos y un aumento en la incidencia de lesiones nefríticas relacionadas con el tratamiento en animales de este grupo de tratamiento. La dosis "efecto no tóxico" para este estudio fue de 55 mg/kg/día. Se realizó un estudio de toxicidad oral en el cual a ratas inmaduras se les administró claritromicina suspensión durante seis semanas en dosis diarias de 0, 15, 50 y 150 mg base/kg/día. No hubo muertes y el único signo clínico observado fue salivación excesiva en algunos de los animales con las dosis más altas, de una a dos horas después de la administración durante las últimas tres semanas de tratamiento. Ratas del grupo de dosis de 150 mg/kg tuvieron menores pesos corporales medios durante las primeras tres semanas, y se observaron que presentaban valores medios disminuidos de albúmina sérica y peso hepático relativo medio aumentado, comparado con los controles. No se encontraron cambios histopatológicos gruesos o microscópicos relacionados con el tratamiento. Una dosis de 150 mg/kg/día produjo una toxicidad leve en las ratas tratadas y la "dosis sin efecto" se consideró en 50 mg/kg/día. Perros beagles jóvenes de tres semanas de edad, fueron tratados en forma oral diariamente por cuatro semanas con 0, 30, 100 o 300 mg/kg de claritromicina, seguido por un período de recuperación de cuatro semanas. No se observaron muertes ni cambios en la condición general de los animales. La necropsia no reveló anormalidades. Una vez realizado el examen histológico, se obs
ervaron depósitos de grasa en los hepatocitos centrolobulares e infiltración celular en las áreas portales con el microscopio de luz, y se observó un aumento en las gotitas de grasa hepatocelular por microscopía electrónica en el grupo con dosis de 300 mg/kg. La dosis tóxica en perros beagles jóvenes se consideró mayor que 300 mg/kg y la dosis sin efecto 100 mg/kg. Fertilidad, Reproducción y Teratogenicidad: Los estudios sobre fertilidad y reproducción han mostrado que dosis diarias de 150 a 160 mg/kg/día en ratas hembras y machos no causaron eventos adversos en el ciclo reproductivo, fertilidad, parto y número y viabilidad de la descendencia. Dos estudios de teratogenicidad en ratas Wistar (v.o) y Sprague-Dawley (v.o. e i.v.), un estudio con conejos blancos de Nueva Zelanda y un estudio con monos cinomolgus fallaron para demostrar alguna teratogenicidad de claritromicina. Sólo en un estudio adicional en ratas Sprague-Dawley en dosis similares y en condiciones esencialmente semejantes ocurrió una incidencia muy baja, insignificante estadísticamente (aproximadamente 6%) de anomalías cardiovasculares. Estas anomalías parecieron ser debidas a expresión espontánea de cambios genéticos dentro de la colonia. Dos estudios en ratones también revelaron una incidencia variable de fisura palatina (3 a 30%) después de dosis de 70 veces el rango superior a la dosis clínica usual humana diaria (500 mg dos veces al día), pero no a 35 veces la dosis máxima clínica humana diaria, sugiriendo toxicidad fetal y maternal pero no teratogenicidad. Se ha mostrado que la claritromicina produce pérdida de embriones en monos cuando se administra aproximadamente diez veces el rango superior a la dosis usual humana diaria (500 mg dos veces al día), comenzando en el día 20 de la gestación. Este efecto se ha atribuido a la toxicidad materna de la droga en dosis muy altas. Un estudio adicional en monos hembras preñadas con dosis de aproximadamente 2,5 a 5 veces la dosis diaria máxima intentada de 500 mg dos veces al día no produjo riesgo único a la cría. Un test letal dominante en ratones con dosis de 1000 mg/kg/día (aproximadamente 70 veces la dosis clínica máxima humana diaria de 500 mg dos veces al día) fue claramente negativo para cualquier actividad mutagénica y en un estudio de Segmento I de ratas tratadas con hasta 500 mg/kg/día (aproximadamente 35 veces la dosis clínica máxima diaria humana de 500 mg dos veces al día) durante 80 días, no se mostró evidencia de deterioro funcional de la fertilidad masculina debido al largo período de exposición a estas dosis tan altas de claritromicina. Mutagenicidad: Se realizaron estudios para evaluar el potencial mutagénico de la claritromicina usando sistemas de prueba con microsomas activos y no activos del hígado de rata (Test Ames). Los resultados de estos estudios no proporcionaron evidencia de potencial mutagénico en las concentraciones de droga de 25 mcg/Placa de Petri o menos. En una concentración de 50 mcg, la droga fue tóxica para todas las cepas probadas. Estudios clínicos: Experiencia Clínica en Pacientes con Infecciones No-micobacterianas: En estudios clínicos, se demostró que la claritromicina en una dosis de 7,5 mg/kg dos veces al día es segura y efectiva en el tratamiento de pacientes pediátricos con infecciones que requieren tratamiento antibiótico oral. Se ha evaluado en más de 1200 niños, con edades de los seis meses a 12 años, con otitis media, faringitis, infecciones a la piel e infecciones del tracto respiratorio inferior. En estos estudios, la claritromicina en una dosis de 7,5 mg/kg dos veces al día demostró eficacia bacteriológica y clínica comparable a los agentes de referencia que incluyen penicilina V, amoxicilina, amoxicilina/clavulanato, etilsuccinato de eritromicina, cefaclor y cefadroxilo. Experiencia Clínica en Pacientes con Infecciones por Mycobacterias: Un estudio preliminar en pacientes pediátricos (algunos eran VIH positivos) con infecciones micobacterianas, demostró que la claritromicina era un tratamiento seguro y efectivo cuando se administra sola o en combinación con zidovudina o dideoxinosina. La Claritromicina Suspensión Pediátrica fue administrada en dos dosis divididas de 7,5, 15 o 30 mg/kg/día. Se observaron algunos efectos estadísticamente significativos sobre parámetros farmacocinéticos cuando la claritromicina se administró con compuestos antiretrovirales; sin embargo, estos cambios fueron menores y probablemente sin significancia clínica. La claritromicina en dosis de hasta 30 mg/kg/día fue bien tolerada. La claritromicina fue efectiva en el tratamiento de infecciones diseminadas por M. avium complex en pacientes pediátricos con SIDA, demostrando en algunos pacientes eficacia continua después de más de un año de terapia.
Indicaciones.
Claritromicina Suspensión Pediátrica está indicada para el tratamiento de infecciones debido a organismos susceptibles, en las siguientes condiciones: 1. Infecciones del tracto respiratorio superior (ej. faringitis estreptocócica). 2. Infecciones del tracto respiratorio inferior (ej. bronquitis, neumonía). 3. Otitis media aguda. 4. Infecciones de la piel y estructuras de la piel (ej. impétigo, foliculitis, celulitis, abscesos). 5. Infecciones mycobacterianas localizadas o diseminadas debido a Mycobacterium avium o Mycobacterium intracellulare. Infecciones localizadas debido a Mycobacterium chelonae, Mycobacterium fortuitum o Mycobacterium kansasii.
Dosificación.
La dosis diaria recomendada de Claritromicina Suspensión Pediátrica (250mg/5mL) en niños es de 7,5 mg/kg dos veces al día, hasta una dosis máxima de 500 mg dos veces al día para infecciones no mycobacterianas. La duración usual del tratamiento es de cinco a diez días dependiendo del patógeno involucrado y de la severidad de la condición. La suspensión preparada se puede ingerir con o sin alimento y se puede ser tomar con leche. La siguiente tabla es una guía sugerida para determinar las dosis:
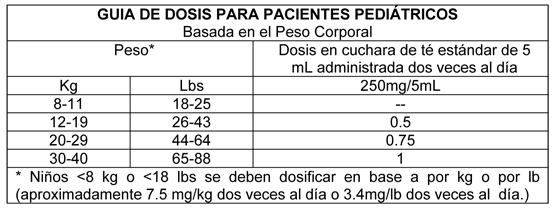
Dosis en Pacientes con Daño Renal: En niños con clearance de creatinina menor de 30 mL/min, la dosis de claritromicina se debe reducir a la mitad, por ej., hasta 250 mg una vez al día, o 250 mg dos veces al día en infecciones más severas. El tratamiento no se debe prolongar más allá de 14 días en estos pacientes. Dosis en Pacientes con Infecciones Mycobacterianas: En niños con infecciones mycobacterianas localizadas o diseminadas (M. avium, M. intracellulare, M. cheloae, M. fortuitum, M. kansasii), la dosis recomendada es 15 a 30 mg/kg de claritromicina por día divididas en dos dosis. El tratamiento con Claritromicina se debe continuar hasta que los beneficios clínicos se demuestren. La adición de otros agentes antimicrobianos puede ser de beneficio.
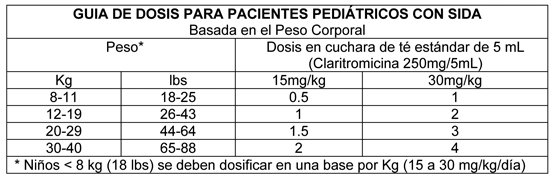
Preparación para el Uso: Consultar la Fórmula de Fabricación Internacional, se debe agregar una apropiada cantidad de agua a los gránulos en la botella y batir para convertir en una suspensión reconstituida. La concentración de claritromicina en la suspensión reconstituida es de 250 mg por 5mL. La suspensión reconstituida puede ser usada por hasta 14 días cuando se almacena a temperatura ambiente (15 a 30°C). Agitar bien antes de cada uso.
Contraindicaciones.
Claritromicina Suspensión Pediátrica está contraindicada en pacientes con hipersensibilidad conocida a los antibióticos macrólidos. La administración concomitante de claritromicina y cualquiera de las siguientes drogas está contraindicada: astemizol, cisaprida, pimozida, terfenadina y ergotamina o dihidroergotamina (ver Interacciones).
Reacciones adversas.
El perfil de seguridad de la formulación pediátrica es similar a la del comprimido de 250 mg en pacientes adultos. La Tabla 1 muestra los eventos adversos reportados en pacientes que tomaron claritromicina en estudios clínicos. Los eventos adversos de muestran por sistema corporal y frecuencia (común ≥1/100, < 1/10).
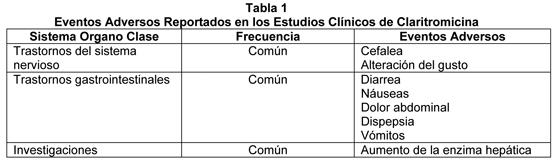
Experiencia Post-Comercialización: La claritromicina se comercializa en varias formulaciones diferentes. La Tabla 2 es una compilación de reacciones adversas para todas las formulaciones incluyendo claritromicina suspensión pediátrica. Debido a que estas reacciones se reportan voluntariamente desde una población de tamaño incierto, no siempre es posible estimar realmente su frecuencia o establecer una relación causal a la exposición a la droga. La exposición de paciente se estima ser mayor a 1 billón de días de tratamiento paciente para claritromicina.
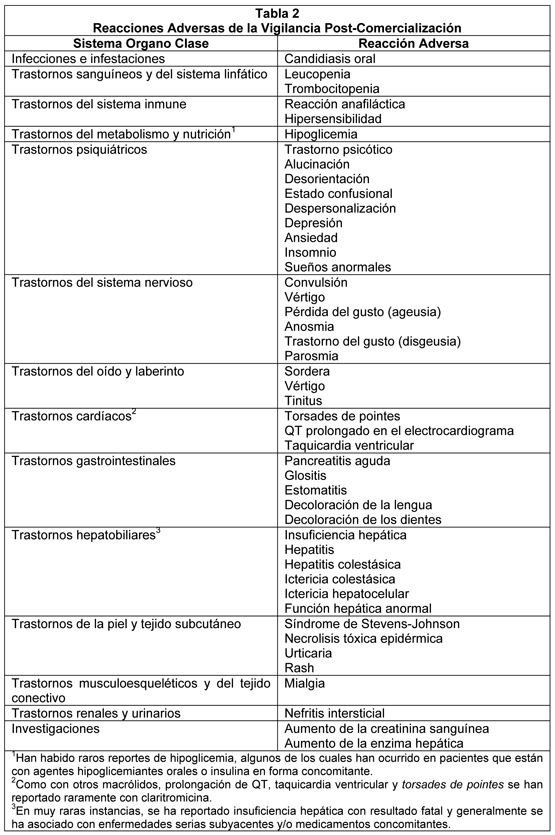
Han habido informes post-comercialización de toxicidad de la colchicina con uso concomitante de claritromicina y colchicina, especialmente en los ancianos, algunos de los cuales ocurrieron en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones de droga: Colchicina y Advertencias). Pacientes pediátricos inmunocomprometidos: En pacientes con SIDA y otros inmunocomprometidos tratados con las dosis más altas de claritromicina por períodos largos de tiempo por infecciones mycobacterianas, es a menudo difícil distinguir eventos adversos posiblemente asociados con la administración de claritromicina debido a los signos preexistentes de enfermedad por VIH o enfermedades intercurrentes. Un número limitado de pacientes pediátricos con SIDA han sido tratados con Claritromicina Suspensión Pediátrica por infecciones mycobacterianas. Los eventos adversos más frecuentemente informados, excluyendo aquellos debido a la condición concurrente del paciente, fueron tinnitus, sordera, vómitos, náuseas, dolor abdominal, rash purpúrico, pancreatitis y aumento de amilasas. Las evaluaciones de los valores de laboratorio para estos pacientes fueron realizados analizando aquellos valores seriamente fuera del nivel anormal (por ej. el extremo alto o el límite bajo) para el test específico. Basados en estos criterios, un paciente pediátrico con SIDA que recibió < 15 mg/kg/día de claritromicina tuvo una bilirrubina total seriamente anormal (elevada); de los pacientes que recibieron 15 a < 25 mg/kg/día de claritromicina, hubo uno informado como seriamente anormal SGPT, BUN y conteo de plaquetas seriamente disminuido. Ninguno de estos valores seriamente anormales para estos parámetros de laboratorio fueron informados por pacientes que recibieron las dosis más altas (25 mcg/kg/día) de claritromicina.
Advertencias.
Si la Claritromicina Suspensión Pediátrica se considera para pacientes en edad post puberal, el médico debe sopesar cuidadosamente los beneficios contra el riesgo, cuando existe sospecha o confirmación de embarazo. El uso a largo plazo, como con otros antibióticos, produce colonización con números aumentados de bacterias y hongos no susceptibles. Si ocurren superinfecciones, se debe instituir una terapia apropiada. Se ha reportado colitis pseudomembranosa con prácticamente todos los agentes antibacterianos, incluyendo macrólidos y puede variar desde leve hasta con riesgo vital. Se ha reportado diarrea asociada a Clostridium difficile (CDAD) con el uso de prácticamente todos los agentes antimicrobianos incluyendo claritromicina, y puede variar en severidad desde diarrea leve a colitis fatal. El tratamiento con agentes antibacterianos alteran la flora normal del colon, el cual puede llevar a un sobrecrecimiento de C. difficile. El CDAD se debe considerar en todos los pacientes que presentan diarrea después del uso de antibióticos. Es necesario una historia médica cuidadosa ya que CDAD se ha reportado que ocurre sobre dos meses después de la administración de agentes antibacterianos. Se ha reportado exacerbación de síntomas de miastenia gravis en pacientes que reciben terapia con claritromicina. La claritromicina se excreta principalmente por el hígado. Por lo tanto, se debe tener precaución en la administración del antibiótico a pacientes con función hepática alterada. También se debe tener cuidado cuando se administra claritromicina a pacientes con insuficiencia renal moderada a severa. Colchicina: Han habido informes post-comercialización de toxicidad de la colchicina con el uso concomitante de claritromicina y colchicina, especialmente en los ancianos, algunos de los cuales ocurrieron en pacientes con insuficiencia renal. Se han reportado muertes en algunos de esos pacientes (ver Interacciones: Colchicina). También se debe prestar atención a la posibilidad de resistencia cruzada entre claritromicina y otros macrólidos, como también con lincomicina y clindamicina.
Interacciones.
El uso de las siguientes drogas está estrictamente contraindicado debido al potencial para efectos severos por interacción de droga: Se han reportado niveles elevados de cisaprida en pacientes que reciben claritromicina y cisaprida concomitantemente. Esto puede producir prolongación de QT y arritmias cardíacas incluyendo taquicardia ventricular, fibrilación ventricular y torsades de pointes. Efectos similares se han observado en pacientes que toman claritromicina y pimozida concomitantemente (ver Contraindicaciones). Se ha informado de macrólidos que alteran el metabolismo de la terfenadina causando un aumento en los niveles de terfenadina que ocasionalmente se ha asociado con arritmias cardíacas tales como prolongación QT, taquicardia ventricular, fibrilación ventricular y torsades de pointes (ver Contraindicaciones). En un estudio en 14 voluntarios sanos, la administración concomitante de comprimidos de claritromicina y terfenadina produjo un aumento de dos a tres veces en los niveles séricos del metabolito ácido de la terfenadina y en la prolongación del intervalo QT que no llevó a ningún efecto clínicamente detectable. Ergotamina/dihidroergotamina: Los informes Post-comercialización indican que la co-administración de claritromicina con ergotamina o dihidroergotamina se ha asociado a toxicidad aguda por ergot caracterizada por vasoespasmo, e isquemia de las extremidades y de otros tejidos incluyendo sistema nervioso central. La administración concomitante de claritromicina y estos productos medicinales está contraindicada (ver Contraindicaciones). Efectos de Otros Productos Medicinales sobre Claritromicina: Las siguientes drogas son conocidas o sospechosas que afectan las concentraciones circulantes de claritromicina; se puede requerir ajustes de dosis de claritromicina o consideración de tratamientos alternativos. Efavirenz, nevirapina, rifampicina, rifabutina y rifapentina: Fuertes inductores del sistema del metabolismo de citocromo P450 tales como efavirenz, nevirapina, rifampicina, rifabutina y rifapentina pueden acelerar el metabolismo de claritromicina y por ende disminuir los niveles plasmáticos de claritromicina, mientras aumentan aquellos de 14(R)-hidroxi-claritromicina (14-OH-claritromicina), un metabolito que también es activo microbiológicamente, Dado que las actividades microbiológicas de claritromicina y 14-OH-claritromicina son diferentes para diferentes bacterias, el efecto terapéutico intentado podría estar impedido durante la administración concomitante de claritromicina e inductores de enzima. Fluconazol: La administración concomitante de fluconazol 200 mg diarios y claritromicina 500 mg dos veces al día a 21 voluntarios sanos llevó a incrementos en la concentración mínima media estado estable de claritromicina (Cmín) y área bajo la curva (ABC) de 33% y 18% respectivamente. Las concentraciones estado estable del metabolito activo 14-OH-claritromicina no se afectaron significativamente por la administración concomitante de fluconazol. No es necesario hacer ajuste de dosis de claritromicina. Ritonavir: Un estudio farmacocinético demostró que la administración concomitante de ritonavir 200 mg cada ocho horas y claritromicina 500 mg cada 12 horas produjo una inhibición marcada del metabolismo de claritromicina. La Cmáx de claritromicina aumentó en 31 %, Cmín aumentó 182% y ABC aumentó 77% con la administración concomitante de ritonavir. Se observó una inhibición esencialmente completa de la formación de 14-[R]-hidroxi-claritromicina. Debido a la gran ventana terapéutica para claritromicina, no debe ser necesaria una reducción en la dosificación en pacientes con función renal normal. Sin embargo, para pacientes con deterioro renal, se deben considerar los siguientes ajustes de dosificación: para pacientes con Clcr 30 a 60 mL/min, la dosis de claritromicina se debe reducir en 50%. Para pacientes con Clcr < 30 mL/min la dosis de claritromicina se debe reducir en 75%. Las dosis de claritromicina mayores a 1 g/día no se deben coadministrar con ritonavir. Efectos de Claritromicina sobre Otros Productos Medicinales: Antiarrítmicos: Existen reportes post-comercialización de torsades de pointes que ocurrieron con el uso concurrente de claritromicina y quinidina o disopiramida. Los electrocardiogramas se deben monitorear para prolongación de QTc durante la co-administración de claritromicina con estas drogas. Los niveles séricos de estos medicamentos se deben monitorear durante la terapia con claritromicina. Interacciones basadas en CYP3A4: La co-administración de claritromicina, conocido inhibidor de CYP3A y una droga principalmente metabolizada por CYP3A se puede asociar con elevaciones en las concentraciones de droga que pudieran incrementar o prolongar tanto los efectos terapéuticos como los adversos de la droga concomitante. La claritromicina se debe usar con precaución en pacientes que reciben tratamiento con otras drogas conocidas como sustratos de la enzima CYP3A, especialmente si el sustrato CYP3A tiene un margen de seguridad estrecho (ej. carbamazepina) y/o el sustrato es extensamente metabolizado por esta enzima. Se pueden considerar ajustes de dosis, y cuando sea posible, se deben monitorear de cerca las concentraciones séricas de drogas principalmente metabolizadas por CYP3A en pacientes que reciben claritromicina concurrentemente. Las siguientes drogas o clases de drogas son conocidas o se sospecha que se metabolizan por la misma isoenzima CYP3A: alprazolam, astemizol, carbamazepina, cilostazol, cisaprida, ciclosporina, disopiramida, alcaloides ergot, lovastatina, metilprednisolona, midazolam, omeprazol, anticoagulantes orales (ej. warfarina), pimozida, quinidina, rifabutina, sildenafil, simvastatina, tacrolimus, terfenadina, triazolam y vinblastina. Las drogas que interactúan por mecanismos similares a través de otras isoenzimas dentro del sistema citocromo P450 incluyen fenitoína, teofilina y valproato. Inhibidores de la HMG-CoA Reductasa: Como con otros macrólidos, se ha reportado que la claritromicina aumenta las concentraciones de inhibidores de la HMG-CoA reductasa (ej. lovastatina y simvastatina). Se han informado raros reportes de rabdomiólisis en pacientes que toman estas drogas concomitantemente. Omeprazol: Claritromicina (500 mg cada 8 horas) se administró en combinación con omeprazol (40 mg diarios) a sujetos adultos sanos. Las concentraciones plasmáticas estado estables de omeprazol se aumentaron (Cmáx, ABC0-24, y t½ aumentaron en 30%, 89% y 34%, respectivamente), por la administración concomitante de claritromicina. El valor medio del pH gástrico de 24 horas fue 5.2 cuando el omeprazol se administró solo y 5.7 cuando el omeprazol se co-administró con claritromicina. Anticoagulantes orales: Reportes espontáneos en el período post-comercialización sugieren que la administración concomitante de claritromicina y anticoagulantes orales puede potenciar los efectos de los anticoagulantes orales. Se deben monitorear cuidadosamente los tiempos de protrombina mientras los pacientes estén recibiendo claritromicina y anticoagulantes orales simultáneamente. Sildenafil, tadalafil y vardenafil: Cada uno de estos inhibidores de fosfodiesterasa se metaboliza, al menos en parte, por CYP3A, y CYP3A puede ser inhibido por la claritromicina administrada concomitantemente. La co-administración de claritromicina con sildenafil, tadalafil o vardenafil produciría probablemente un aumento de la exposición al inhibidor de fosfodiesterasa. Se debe considerar una reducción de las dosis de sildenafil, tadalafil y vardenafil cuando estas drogas se co-administran con claritromicina. Teofilina, carbamazepina: Los resultados de los estudios clínicos indican que hubo un modesto pero estadísticamente significativo (p≤0.05) aumento de los niveles circulantes de teofilina o carbamazepina cuando cualquiera de estas drogas se administraron concomitantemente con claritromicina. Tolterodina: La principal ruta del metabolismo de tolterodina es vía la isoforma 2D6 del citocromo P450 (CYP2D6). Sin embargo, en un subgrupo de la población dedicada de CYP2D6, la ruta identificada del metabolismo es vía CYP3A. En este subgrupo de la población, la inhibición de CYP3A produce concentraciones séricas significativamente mayores de tolterodina. Puede ser necesaria una reducción de la dosis de tolterodina en la presencia de inhibidores de CYP3A, tal como claritromicina en la población de metabolizadores pobres de CYP2D6. Triazolobenzodiazepinas (ej. alprazolam, midazolam, triazolam): Cuando se co-administra midazolam con claritromicina comprimidos (500 mg dos veces al día), el ABC de midazolam se incrementó 2.7 veces después de la administración intravenosa de midazolam y 7 veces después de la administración oral. La administración concomitante de midazolam oral y claritromicina se debe evitar. Si se co-administra midazolam intravenoso con claritromicina se debe monitorear cercanamente al paciente para permitir un ajuste de dosis. Las mismas precauciones se deben aplicar también a otras benzodiazepinas que se metabolizan por CYP3A, incluyendo triazolam y alprazolam. Para las benzodiazepinas que no son dependientes de CYP3A para su eliminación (temazepam, nitrazepam, lorazepam), no es probable una interacción clínicamente importante con claritromicina. Han existido reportes post-comercialización de interacciones de droga y efectos sobre el sistema nervioso central (SNC) (ej. somnolencia y confusión) con el uso concomitante de claritromicina y triazolam. Se sugiere monitoreo del paciente por aumento de los efectos farmacológicos sobre el SNC. Interacciones de Otras Drogas: Colchicina: La colchicina es un sustrato tanto para CYP3A como para el transportador del eflujo, P-glicoproteína (Pgp). Se sabe que la claritromicina y otros macrólidos inhiben CYP3A y Pgp. Cuando la claritromicina y la colchicina se administran juntas, la inhibición de Pgp y/o CYP3A por claritromicina puede llevar a aumento de la exposición a colchicina. Los pacientes se deben monitorear por síntomas clínicos de toxicidad a colchicina (ver Advertencias). Digoxina: Se piensa que la digoxina es un sustrato para el transportador del eflujo, P-glicoproteína (Pgp). Se conoce que la claritromicina inhibe Pgp. Cuando claritromicina y digoxina se administran juntas, la inhibición de Pgp por claritromicina puede llevar a aumento de la exposición a digoxina. En vigilancia post-comercialización se han reportado concentraciones séricas elevadas de digoxina en pacientes que reciben claritromicina y digoxina concomitantemente. Algunos pacientes han mostrado signos clínicos consistentes con toxicidad a digoxina, incluyendo arritmias potencialmente fatales. Las concentraciones séricas de digoxina se deben monitorear cuidadosamente si los pacientes reciben digoxina y claritromicina simultáneamente. Zidovudina: La administración oral simultánea de claritromicina comprimidos y zidovudina en pacientes adultos infectados con VIH puede producir una disminución en las concentraciones estado estables de zidovudina. Hoy en día, esta interacción no parece ocurrir en pacientes pediátricos infectados con VIH que toman Claritromicina Suspensión Pediátrica con zidovudina o dideoxinosina. Interacciones Bi-Direccionales de Droga: Atazanavir: Tanto claritromicina como atazanavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bi-direccional de droga. La co-administración de claritromicina (500 mg dos veces al día) con atazanavir (400 mg una vez al día) produjo 2 veces de aumento en la exposición a claritromicina y un 70% de disminución en la exposición a 14-OH-claritromicina, con un 28% de aumento en el ABC de atazanavir. Debido a la gran ventana terapéutica para claritromicina, no es necesaria una reducción de dosis en pacientes con función renal normal. Para pacientes con función renal moderada (clearance de creatinina 30 a 60 mL/min), la dosis de claritromicina se debe disminuir en 75% usando una formulación apropiada de claritromicina. No se deben co-administrar dosis de claritromicina mayores de 1000 mg por día con inhibidores de proteasa. Itraconazol: Tanto claritromicina como itraconazol son sustratos e inhibidores de CYP3A, llevando a una interacción bi-direccional de droga. Claritromicina puede aumentar los niveles plasmáticos de itraconazol, mientras itraconazol puede aumentar los niveles plasmáticos de claritromicina. Se debe monitorear cercanamente a los pacientes que toman itraconazol y claritromicina concomitantemente, por signos o síntomas de efecto farmacológico aumentado o prolongado. Saquinavir: Tanto claritromicina como saquinavir son sustratos e inhibidores de CYP3A, y existe evidencia de una interacción bi-direccional de droga. La administración concomitante de claritromicina (500 mg dos veces al día) y saquinavir (cápsulas de gelatina blanda, 1200 mg tres veces al día) a 12 voluntarios sanos produjo valores estado estable de ABC y Cmáx de saquinavir que eran 177% y 187% mayores que aquellos observados con saquinavir solo. Los valores ABC y Cmáx de claritromicina fueron aproximadamente 40% mayores que aquellos observados con claritromicina sola. No se requiere ajuste de dosis cuando las dos drogas se co-administran por un tiempo limitado en las dosis/formulaciones estudiadas. Observaciones de estudios de interacción de droga usando la formulación cápsula de gelatina blanda no puede ser representativa de los efectos observados usando la cápsula de gelatina dura de saquinavir. Observaciones de estudios de interacción de droga realizada con saquinavir solo no pueden ser representativas de los efectos observados con la terapia con saquinavir/ritonavir. Cuando saquinavir se co-administra con ritonavir, se deben considerar los efectos potenciales de ritonavir sobre claritromicina (ver Interacciones de droga). Verapamil: Se han observado hipotensión, bradiarritmias y acidosis láctica en pacientes que toman claritromicina y verapamil concomitantemente. Embarazo: No se ha establecido la seguridad de claritromicina para uso durante el embarazo y durante la lactancia en lactantes. La claritromicina es excretada en la leche humana.
Conservación.
La Claritromicina Suspensión Pediátrica en gránulos debe ser almacenada a temperatura ambiente (15 a 30°C). No refrigerar la suspensión reconstituida, mantenerla a temperatura ambiente.
Sobredosificación.
Informes indican que con la ingesta de grandes cantidades de claritromicina se puede esperar que ocurran síntomas gastrointestinales. Un paciente que tenía una historia de trastorno bipolar ingirió ocho gramos de claritromicina y mostró estado mental alterado, comportamiento paranoide, hipokalemia e hipoxemia. Las reacciones adversas que acompañan una sobredosis deben ser tratadas con la pronta eliminación de la droga no absorbida y medidas de apoyo. Como con otros macrólidos, no se espera que los niveles séricos de claritromicina sean afectados en forma importante por hemodiálisis o diálisis peritoneal.
Presentación.
Claritromicina Suspensión Pediátrica en gránulos se presenta como una preparación granular de claritromicina en botellas que permiten la capacidad de batir. Cuando se agrega la cantidad adecuada de agua (ver Preparación para el Uso) se convierte en una suspensión reconstituida, la concentración de claritromicina es de 250 mg/5mL.
Laboratorio que comercializa Klaricid
ABBOTT →

