ULTIVAMR
GLAXOSMITHKLINE
Polvo liof. p/solución inyectable 1 mg
Analgésico.
Composición.
El remifentanilo para inyección es un liofilizado sin preservativos, sin endotoxinas, estéril, de color blanco a blanco grisáceo, para ser reconstituido antes de su uso. Cuando se reconstituye en la forma recomendada, las soluciones de remifentanilo para inyección son claras e incoloras, y contienen 1 mg/ml de base de remifentanilo como clorhidrato de remifentanilo. Lista de excipientes: Glicina. Forma farmacéutica: Liofilizado para ser reconstituido y administrado vía intravenosa (I.V).
Farmacología.
Farmacodinamia: Código ATC: N01AH06. Mecanismo de Acción: El remifentaniloo es un agonista mu-opioide selectivo, con un rápido inicio y duración muy corta de acción. La actividad mu-opioide de ULTIVA es antagonizada por antagonistas narcóticos, como la naloxona. Efectos farmacodinámicos: Las mediciones de histamina, realizadas en pacientes y voluntarios normales, no han mostrado elevación en los niveles de histamina después de la administración de ULTIVA, en bolo a dosis de hasta 30 microgramos/kg.
Farmacocinética.
Absorción: Las concentraciones sanguíneas de ULTIVA son proporcionales a la dosis administrada en la extensión de los límites de dosis recomendados. Por cada aumento de 0,1 microgramos/kg/min en la velocidad de la perfusión, la concentración sanguínea de ULTIVA aumentará 2,5 nanogramos/mL. Distribución: El volumen central de distribución es de 100 mL/kg, y el volumen de distribución en estado estacionario es de 350 mL/kg. El remifentanilo exhibe un grado de fijación a proteínas plasmáticas de 70%. Metabolismo. El remifentanilo es un opioide metabolizado por esterasa, que es susceptible al metabolismo por esterasas inespecíficas de la sangre y tejidos. El metabolismo del remifentanilo da por resultado la formación del metabolito ácido carboxílico, esencialmente inactivo (1/4.600 de potencia del remifentanilo). La vida media del metabolito en adultos sanos es aproximadamente de 2 horas. Se recupera cerca de 95% de ULTIVA en la orina como el metabolito ácido carboxílico. El remifentanilo no es un sustrato de la colinesterasa plasmática. Eliminación: Después de la administración de las dosis recomendadas de remifentanilo, la vida media biológica efectiva es de 3 a 10 minutos. La depuración promedio del remifentanilo en adultos jóvenes sanos es de 40 mL/min/kg. Poblaciones de pacientes especiales: Anestesia cardiaca: La depuración del remifentanilo se ve reducida hasta en un 20% durante el bypass cardiopulmonar hipotérmico (28°C). La disminución de la temperatura corporal reduce la depuración de eliminación en 3% por°C. Insuficiencia renal: La recuperación rápida de la sedación y la analgesia, basada en el ULTIVA, no se ve afectada por el estado renal. La farmacocinética de ULTIVA no cambia significativamente en pacientes con varios grados de insuficiencia renal, aún después de la administración de hasta 3 días, en condiciones de cuidados intensivos. La depuración del metabolito ácido carboxílico está reducida en los pacientes con deterioro renal. En los pacientes en cuidados intensivos con insuficiencia renal de grado moderado/severo, la concentración del metabolito ácido carboxílico puede exceder 250 veces el nivel del remifentanilo en estado estacionario en algunos pacientes. Los datos clínicos demuestran que la acumulación del metabolito no da por resultado efectos mu-opioides clínicamente pertinentes, aún después de la administración de perfusiones de ULTIVA por hasta 3 días en estos pacientes. No hay indicios de que el remifentanilo sea extraído durante la terapia de reemplazo renal. El metabolito ácido carboxílico es extraído durante la hemodiálisis, en cuando menos 30%. Insuficiencia hepática: La farmacocinética de ULTIVA no sufre cambios en los pacientes con insuficiencia hepática severa que están en espera de trasplante de hígado, o durante la fase anhepática de la cirugía de trasplante de hígado. Es posible que los pacientes con insuficiencia hepática severa sean ligeramente más sensibles a los efectos depresores respiratorios del remifentanilo. Estos pacientes deben ser vigilados estrechamente, y la dosis de ULTIVA debe titularse de acuerdo a la necesidad del paciente. Pacientes pediátricos: En los pacientes pediátricos de 5 días a 17 años de edad, la depuración promedio y el volumen de distribución en estado estacionario de remifentanilo son mayores en los niños más pequeños, y declinan a valores de adulto joven sano, hacia los 17 años de edad. La vida media del remifentanilo no es significativamente distinta en los neonatos, lo que sugiere que los cambios en el efecto analgésico, después de los cambios en la velocidad de perfusión de ULTIVA, deben ser rápidos y similares a los que se observan en adultos jóvenes sanos. La farmacocinética del metabolito ácido carboxílico en los pacientes pediátricos de 2 a 17 años de edad, es similar a la observada en adultos después de la corrección por las diferencias en peso corporal. Personas de edad avanzada: La depuración del remifentanilo está ligeramente reducida (aproximadamente en 25%) en los pacientes de edad avanzada (mayores de 65 años de edad), en comparación con los pacientes jóvenes. La actividad farmacodinámica del remifentanilo aumenta con la edad. Los pacientes de edad avanzada tienen EC50 de remifentanilo en la formación de ondas delta en el electroencefalograma (EEG), que es 50% inferior que en pacientes jóvenes, por lo cual la dosis inicial de ULTIVA se debe reducir en 50% en los sujetos de edad avanzada, y luego titularse cuidadosamente para cubrir la necesidad individual del paciente. Transferencia placentaria y a la leche: En una prueba clínica realizada en mujeres, la concentración de remifentanilo en la sangre fetal fue aproximadamente del 50% de la sangre materna. La relación arteriovenosa fetal de las concentraciones de remifentanilo fue aproximadamente 30%, lo que sugiere metabolismo del remifentanilo en el neonato. Datos preclínicos de seguridad: La administración intratecal de la formulación de glicina sin remifentanilo a perros causó agitación, dolor y disfunción de los miembros posteriores, e incoordinación. Se cree que estos efectos son secundarios al excipiente glicina. La glicina es un excipiente usado comúnmente en productos i.v., y este hallazgo no tiene pertinencia respecto a la administración i.v., de remifentanilo. El remifentanilo, como otros agonistas opioides, produjo aumentos en la duración del potencial de acción (APD, del inglés action potential duration) en fibras de Purkinje aisladas de perro. Con remifentanilo, los efectos se observaron a concentraciones de 1 micromolar, o más altas (que son más altas que las concentraciones plasmáticas que se observan en la práctica clínica). No hubo efectos a una concentración de 0,1 micromolar. El metabolito principal del remifentanilo, ácido carboxílico, no tuvo efecto alguno sobre la APD hasta la máxima concentración probada de 10 micromolar. Se encontró material relacionado con remifentanilo en la leche de ratas después de la dosificación con ese fármaco. Los estudios de transferencia placentaria realizados en ratas y conejas mostraron que las crías están expuestas a ULTIVA o sus metabolitos, o ambos, durante el crecimiento y el desarrollo. No se han encontrado hallazgos adicionales clínicamente pertinentes.
Indicaciones.
ULTIVA se indica como un agente analgésico para usarse durante la inducción y/o mantenimiento de la anestesia general durante procedimientos quirúrgicos, con inclusión de la cirugía cardiaca, así como para la continuación de la analgesia en el período postoperatorio inmediato, bajo vigilancia cercana, durante la transición a una analgesia de acción más prolongada. ULTIVA se indica para proveer analgesia y sedación a pacientes en cuidados intensivos, ventilados mecánicamente.
Dosificación.
ULTIVA debe administrarse únicamente en servicios completamente equipados para la vigilancia y el soporte de las funciones cardiovascular y respiratoria, y por personas capacitadas específicamente para usar fármacos anestésicos y reconocer y tratar los efectos adversos esperados de los opioides potentes, con inclusión de la reanimación respiratoria y cardiaca. Tal capacitación debe incluir el establecimiento y mantenimiento de una vía respiratoria permeable y una ventilación asistida. Las perfusiones continuas de ULTIVA deben administrarse mediante un dispositivo de perfusión calibrado a una línea i.v., de flujo rápido, o a través de una línea i.v. dedicada especialmente. Esta línea de perfusión debe estar conectada a la cánula venosa, o estar cerca de la misma y preparada para minimizar la posibilidad de un espacio muerto (ver Instrucciones para su Uso/Manejo para obtener información adicional, que incluye tablas con ejemplos de velocidades de perfusión por peso corporal, para ayudar a titular ULTIVA según las necesidades anestésicas del paciente). Se debe tener cuidado, tanto en evitar la obstrucción o desconexión de las líneas de perfusión, como al limpiar las líneas para retirar los residuos de ULTIVA después de su uso (ver Advertencias). ULTIVA sólo debe utilizarse vía intravenosa, por lo cual no se debe administrar mediante inyección epidural o intratecal (ver Contraindicaciones). Después de su reconstitución, ULTIVA para inyección es estable durante un periodo de 24 horas, a temperatura ambiente (25°C), y se recomienda diluir adicionalmente 20 a 250 microgramos/ml (50 microgramos/ml es la dilución recomendada para adultos, y 20 a 25 microgramos/ml para pacientes pediátricos de un año de edad o mayores) con uno de los siguientes líquidos intravenosos, listados a continuación: agua esterilizada para inyección, dextrosa al 5% para inyección, dextrosa al 5% y cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,45% para inyección (ver Instrucciones para su Uso/Manejo para obtener información adicional, que incluye tablas para ayudar a titular ULTIVA según las necesidades anestésicas del paciente). La administración de ULTIVA durante la anestesia general debe individualizarse con base en la respuesta del paciente. No se recomienda para emplearse como único agente en anestesia general. Anestesia general: Adultos: La siguiente tabla resume las velocidades de perfusión iniciales y los límites de la dosis.
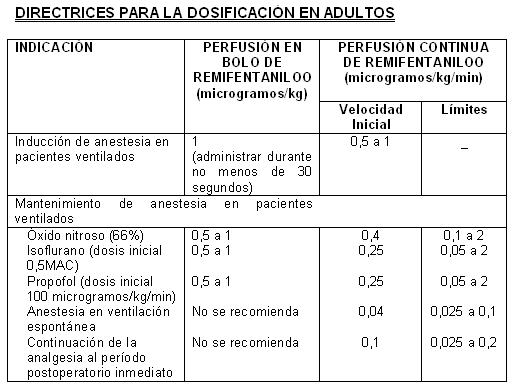
Cuando se administra con perfusión en bolo en la inducción, ULTIVA debe administrarse durante un lapso no inferior a 30 segundos. Administrado a las dosis recomendadas anteriormente, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tanto, el isoflurano y el propofol deben administrarse según las recomendaciones anteriores para evitar una profundidad excesiva de la anestesia (ver Medicación concomitante en esta sección). No se dispone de datos sobre recomendaciones de dosificación concernientes al uso simultáneo de otros hipnóticos con ULTIVA. Inducción de la anestesia: En la inducción de la anestesia, ULTIVA debe administrarse con un agente hipnótico, como propofol, tiopentona o isoflurano. ULTIVA puede administrarse a una velocidad de perfusión de 0,5 a 1 microgramos/kg/min, con o sin una perfusión en bolo inicial de 1 microgramo/kg, durante un lapso no inferior a 30 segundos. Si ha de realizarse una intubación endotraqueal después de transcurrir más de 8 a 10 minutos a partir de la iniciación de la perfusión de ULTIVA, entonces no es necesario practicar una perfusión en bolo. Mantenimiento de la anestesia: Después de la intubación endotraqueal, es necesario disminuir la velocidad de perfusión de ULTIVA, de acuerdo a la técnica anestésica y en la forma indicada en la tabla de arriba. Debido a la rápida iniciación y corta duración de la acción del remifentanilo, la velocidad de administración durante la anestesia puede titularse ascendentemente, en incrementos de 25% a 100%, o descendentemente, en reducciones de 25% a 50%, cada 2 a 5 minutos, para alcanzar el nivel deseado de respuesta mu-opioide. En respuesta a una anestesia ligera, es posible administrar perfusiones complementarias en bolo cada 2 a 5 minutos. Anestesia en pacientes anestesiados, en respiración espontánea y con vía aérea asegurada (p.ej., anestesia con mascarilla laríngea): En pacientes anestesiados con ventilación espontánea y con vía aérea asegurada, es probable que ocurra una depresión respiratoria. Es necesario tener un cuidado especial al ajustar la dosis a los requerimientos del paciente, ya que puede requerirse un soporte ventilatorio. La velocidad inicial de perfusión recomendada para analgesia complementaria en pacientes anestesiados con ventilación espontánea, es de 0,04 microgramos/kg/min titulados hasta alcanzar el efecto. Se han estudiado límites de velocidades de perfusión de 0,025 a 0,1 microgramos/kg/min. No se recomiendan inyecciones en bolo en pacientes anestesiados con ventilación espontánea. Continuación al período postoperatorio inmediato: En caso de que no se haya establecido anteriormente alguna analgesia de duración más prolongada al final de la cirugía, podría ser necesario continuar con ULTIVA para mantener la analgesia durante el período postoperatorio inmediato, hasta que la analgesia de acción más prolongada haya alcanzado su efecto máximo. En los pacientes ventilados, se debe seguir titulando la velocidad de perfusión hasta alcanzar el efecto. En los pacientes que se encuentran respirando espontáneamente, la velocidad de perfusión de ULTIVA debe disminuirse inicialmente a una tasa de 0,1 microgramos/kg/min. Posteriormente, la velocidad de perfusión puede aumentarse o reducirse, en no más de 0,025 microgramos/kg/min cada 5 minutos, con el fin de equilibrar el nivel de analgesia y la frecuencia respiratoria del paciente. ULTIVA sólo debe emplearse en un servicio completamente equipado para la vigilancia y el soporte de las funciones cardiovascular y respiratoria, bajo estrecha supervisión de personas capacitadas específicamente en el reconocimiento y tratamiento de los efectos respiratorios de los opioides potentes. No se recomienda el uso de inyecciones en bolo de ULTIVA para tratar el dolor durante el período postoperatorio en pacientes que estén respirando espontáneamente. Medicación concomitante: ULTIVA disminuye las cantidades o dosis de anestésicos inhalados, hipnóticos o benzodiacepinas, requeridos para la anestesia (ver Interacciones). Las dosis de los siguientes agentes utilizados en anestesia: isoflurano, tiopentona, propofol y temazepam, han sido reducidas hasta en un 75%, cuando se emplean concurrentemente con ULTIVA. Directrices para la discontinuación: Debido al muy rápido efecto de acción de ULTIVA, no se presentará actividad opioide residual dentro de un lapso de 5 a 10 minutos después de su discontinuación. En aquellos pacientes sometidos a procedimientos quirúrgicos, en los cuales se anticipa dolor postoperatorio, se deben administrar analgésicos de manera previa, o inmediatamente después de la discontinuación de ULTIVA. Se debe permitir que transcurra un tiempo suficiente para que se alcance el efecto máximo del analgésico de acción prolongada. La elección del analgésico debe ser adecuada, según el procedimiento quirúrgico del paciente y el nivel de atención postoperatoria. Pacientes pediátricos (1 a 12 años de edad): Inducción de la anestesia. Los datos disponibles resultan insuficientes para hacer una recomendación sobre dosificación. Mantenimiento de la anestesia:
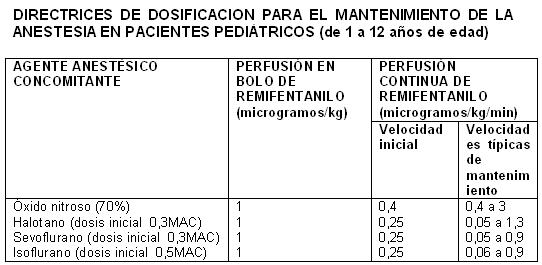
Cuando se practica la perfusión en bolo, ULTIVA debe administrarse durante un lapso no inferior a 30 segundos. Si no se ha administrado una dosis simultánea en bolo, no se debe iniciar la cirugía sino hasta que hayan transcurrido cuando menos 5 minutos después de iniciar la perfusión de ULTIVA. Se debe vigilar a los pacientes pediátricos, y se debe titular la dosis hasta alcanzar la profundidad de analgesia apropiada para el procedimiento quirúrgico. Medicación concomitante: A las dosis recomendadas arriba, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tal razón, el isoflurano, halotano y sevoflurano deben administrarse en la forma recomendada arriba, para evitar una profundidad excesiva de la anestesia. No se dispone de datos sobre las recomendaciones de dosificación en el uso simultáneo de otros hipnóticos con ULTIVA (ver Dosificación - Anestesia general, Adultos, Medicación concomitante). Directrices para la discontinuación: Después de la discontinuación de la perfusión, la desaparición del efecto analgésico de ULTIVA es rápida y similar a la que se observa en los pacientes adultos. Deben anticiparse e implementarse requerimientos analgésicos postoperatorios apropiados (ver Dosificación - Anestesia general, Adultos, Directrices para la discontinuación). Neonatos y lactantes (de edad menor a 1 año): El perfil farmacocinético de ULTIVA en neonatos y lactantes (de edad menor a un año) es comparable al que se observa en los adultos, después de la corrección por las diferencias en el peso corporal. Sin embargo, los datos clínicos disponibles son insuficientes para hacer recomendaciones sobre dosificación para este grupo de edad. Anestesia cardiaca: Adultos:

Período de inducción de la anestesia: Después de la administración de hipnótico para lograr la pérdida de la consciencia, ULTIVA se debe administrar a una velocidad inicial de perfusión de 1 microgramo/kg/min. En los pacientes quirúrgicos cardiacos no se recomienda el uso de perfusiones en bolo de ULTIVA durante la inducción. No se debe practicar intubación endotraqueal durante un lapso de cuando menos 5 minutos después de iniciarse la perfusión. Período de Mantenimiento de la anestesia: Después de la intubación endotraqueal, la velocidad de la perfusión de ULTIVA se debe titular de acuerdo a la necesidad del paciente. También se pueden administrar dosis complementarias en bolo, según se requiera. A los pacientes cardiacos de alto riesgo, como los que presentan función ventricular deficiente, se debe administrar una dosis máxima en bolo de 0,5 microgramos/kg. Estas recomendaciones de dosificación también aplican durante el bypass cardiopulmonar hipotérmico (ver Farmacocinética). Medicación concomitante: A las dosis recomendadas arriba, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tanto, se deben administrar isoflurano y propofol en la forma que se recomienda arriba, para evitar una profundidad excesiva en la anestesia. No se dispone de datos sobre las recomendaciones de dosificación en el uso simultáneo de otros hipnóticos con ULTIVA (ver Dosificación - Anestesia general, Adultos, Medicación concomitante). Continuación de la analgesia postoperatoria antes de la extubación: Se recomienda que la perfusión de ULTIVA se mantenga a la velocidad intraoperatoria final, durante la transferencia de los pacientes al área de cuidados postoperatorios. Al llegar a esta área, el nivel de analgesia y sedación del paciente debe vigilarse estrechamente, y la velocidad de la perfusión de ULTIVA ajustarse, para cubrir los requerimientos individuales del paciente. Directrices para la discontinuación: Con anterioridad a la discontinuación de ULTIVA, los pacientes deben recibir analgésicos y sedantes alternativos, con un tiempo suficiente de anticipación. La elección y dosis del agente o agentes, deben ser apropiadas para el nivel de cuidados postoperatorios del paciente (ver Dosificación - Anestesia general, Adultos, Directrices para la discontinuación). Se recomienda que la perfusión de ULTIVA sea discontinuada, reduciendo la velocidad de la perfusión con disminuciones de 25% a intervalos de cuando menos 10 minutos, hasta que la perfusión se suspenda. Durante la separación del paciente del ventilador, la perfusión de ULTIVA no se debe aumentar; sólo se debe producir titulación en descenso complementada, según se requiera, con analgésicos alternativos. Se recomienda que los cambios hemodinámicos, como hipertensión y taquicardia, se traten con agentes alternativos, según sea apropiado. Pacientes pediátricos: Los datos disponibles son insuficientes para hacer una recomendación sobre dosificación para el uso durante la cirugía cardiaca. Uso en cuidados intensivos: Adultos: ULTIVA puede usarse inicialmente, sólo para proporcionar analgesia y sedación en pacientes en cuidados intensivos, ventilados mecánicamente. Se recomienda que ULTIVA se inicie a una velocidad de perfusión de 0,1 microgramos/kg/min a 0,15 microgramos/kg/min. La velocidad de la perfusión se debe titular con incrementos de 0,025 microgramos/kg/min, para alcanzar el nivel deseado de analgesia y sedación. Se debe permitir que transcurra un período de cuando menos 5 minutos entre los ajustes de las dosis. El nivel de analgesia y sedación debe vigilarse cuidadosamente, reevaluarse regularmente, y la velocidad de perfusión de ULTIVA debe ajustarse de acuerdo a la situación que exista. Si se alcanza una velocidad de perfusión de 0,2 microgramos/kg/min y no se logra el nivel deseado de sedación, se recomienda que se inicie la dosificación con un agente sedante apropiado. La dosis del agente sedante debe titularse para obtener el nivel deseado de sedación. Pueden hacerse aumentos adicionales a la velocidad de la perfusión de ULTIVA, en incrementos de 0,025 microgramos/kg/min, si se requiere analgesia adicional. ULTIVA ha sido estudiado en pacientes en cuidados intensivos, en pruebas clínicas bien controladas, por períodos de hasta 3 días. Existen datos limitados de pruebas clínicas adicionales por períodos de duración más prolongados. La siguiente tabla resume las velocidades de perfusión iniciales y los límites típicos de dosis para proporcionar analgesia y sedación en pacientes individuales:

No se recomiendan dosis en bolo de ULTIVA en situaciones de cuidados intensivos. El uso de ULTIVA reducirá los requerimientos de dosificación de cualquier agente sedantes concomitantes. Las dosis iniciales típicas de agentes sedantes, si se requieren, se proporcionan a continuación.

Para permitir la titulación por separado de agentes respectivos, los agentes sedantes no se deben preparar como una mezcla en la misma bolsa de perfusión. Analgesia adicional para pacientes ventilados sometidos a procedimientos estimulantes: Puede requerirse un aumento en la velocidad de la infusión de ULTIVA, para proporcionar una cobertura analgésica adicional, en los pacientes ventilados sometidos a procedimientos estimulantes o dolorosos, o ambos, como la aspiración endotraqueal, aplicación de apósitos a heridas y fisioterapia. Se recomienda mantener una velocidad de infusión de ULTIVA de cuando menos 0,1 microgramos/kg/min, durante cuando menos 5 minutos antes del inicio del procedimiento estimulante. Pueden practicarse ajustes adicionales en la dosis cada 2 a 5 minutos, en incrementos de 25% a 50%, en anticipación o en respuesta a un requerimiento adicional de analgesia. Se ha administrado una velocidad media de perfusión de 0,25 microgramos/kg/min, máximo de 0,75 microgramos/kg/min, para proporcionar anestesia adicional durante procedimientos estimulantes. Directrices para la discontinuación: Con anterioridad a la discontinuación de ULTIVA, los pacientes deben recibir agentes analgésicos y sedantes alternativos con un tiempo suficiente de anticipación. Se deben anticipar e implementar la selección y dosis apropiadas del agente o agentes. Con el propósito de asegurar una emergencia tranquila de un régimen basado en remifentanilo, se recomienda que la velocidad de la perfusión de ULTIVA se titule en etapas a 0,1 microgramos/kg/min, durante un período de hasta 1 hora anterior a la extubación. Después de la extubación, la velocidad de la perfusión debe disminuirse en reducciones de 25%, a intervalos de cuando menos 10 minutos, hasta que se suspenda la perfusión. Durante la separación del paciente del ventilador, la perfusión de ULTIVA no se debe aumentar; sólo se debe producir titulación en descenso complementada, según se requiera, con analgésicos alternativos. Pacientes pediátricos en cuidados intensivos: No se dispone de datos sobre el uso en pacientes pediátricos. Otras poblaciones: Personas de edad avanzada (mayores de 65 años de edad). Anestesia general: La dosis inicial de ULTIVA administrada a pacientes mayores de 65 años de edad debe ser la mitad de la dosis recomendada para adultos, y titularse de acuerdo a la necesidad individual del paciente, ya que se ha visto un aumento en la sensibilidad a los efectos farmacológicos de ULTIVA en esta población de pacientes. Este ajuste de la dosis aplica para su uso en todas las fases de la anestesia, con inclusión de la inducción, mantenimiento y analgesia postoperatoria inmediata. Anestesia cardiaca: No se requiere reducción de la dosis inicial (ver Dosificación, Anestesia cardiaca, Directrices de dosificación). Cuidados intensivos: No se requiere reducción de la dosis inicial (ver Dosificación, Uso en Cuidados Intensivos). Pacientes obesos: Se recomienda que en los pacientes obesos se reduzca la dosificación de ULTIVA con base en el peso corporal ideal, puesto que la depuración y el volumen de distribución del remifentanilo se correlacionan mejor en esta población, con el peso corporal ideal que con el peso corporal real. Insuficiencia renal: En los pacientes con insuficiencia renal, incluyendo a los sometidos a terapia de reemplazo renal, no es necesario realizar ajustes en la dosificación en relación a la usada en adultos sanos, ya que el perfil farmacocinético de ULTIVA está inalterado en esta población de pacientes. Insuficiencia hepática: No es necesario realizar ajuste alguno en la dosis inicial, en relación con la usada en adultos sanos, puesto que el perfil farmacocinético de ULTIVA no está alterado en esta población de pacientes. Sin embargo, es posible que los pacientes con insuficiencia hepática severa sean ligeramente más sensibles a los efectos depresores respiratorios del remifentanilo. Estos pacientes deben ser motivo de vigilancia estrecha, y la dosis de ULTIVA titularse de acuerdo a la necesidad del paciente. Neurocirugía: La experiencia clínica limitada en los pacientes sometidos a neurocirugía no ha mostrado que se requieran recomendaciones especiales de dosificación. Pacientes con ASA III/IV. Anestesia general: Como debe esperarse que los efectos hemodinámicos de los opioides potentes sean más pronunciados en los pacientes con ASA III/IV, debe tenerse precaución en la administración de ULTIVA en esta población. Por tanto, se recomienda reducción de la dosis inicial y titulación subsiguiente hasta lograr el efecto. Anestesia cardiaca: No se requiere reducción de la dosis inicial (ver Dosificación, Anestesia Cardiaca, Directrices de dosificación).
Contraindicaciones.
Como la formulación contiene glicina, ULTIVA está contraindicado para uso epidural e intratecal (ver Datos preclínicos de seguridad). ULTIVA se contraindica en pacientes con hipersensibilidad conocida a cualquier componente de la preparación, y otros análogos del fentanilo.
Reacciones adversas.
Los efectos adversos se listan a continuación por clase de sistema de órganos y frecuencia de ocurrencia. Las frecuencias se definen como muy común (≥ 1/10), común (≥ 1/100 a < 1/10), no común (≥ 1/1.000 a < 1/100), raro (≥ 1/10.000 a < 1/1.000) y muy raro ( < 1/10.000). Datos de pruebas clínicas:Los efectos adversos más comunes que se asocian con ULTIVA son extensiones directas de farmacología agonista mu-opioide. A continuación se presenta la incidencia general comunicada, determinada por todas las fases de estudios de anestesia controlados, a dosis recomendadas. Estos efectos adversos se resuelven en cuestión de minutos, después de la discontinuación o reducción de la velocidad de administración de ULTIVA. Trastornos del sistema nervioso: Muy común: Rigidez del músculo esquelético. Raro: Sedación (durante la recuperación de la anestesia general). Trastornos cardiacos: Común: Bradicardia. Trastornos vasculares: Muy común: Hipotensión. Común: Hipertensión postoperatoria. Trastornos respiratorias, torácicos y mediastínicos: Comunes: Depresión respiratoria aguda, apnea. No común: Hipoxia. Trastornos gastrointestinales:Muy comunes: Náusea, vómitos. No común: Estreñimiento. Trastornos de la piel y del tejido subcutáneo:Común: Prurito. Trastornos generales y del sitio de administración:Comunes: Temblor postoperatorio. No comunes: Dolores postoperatorios. Datos posteriores a la comercialización: Los siguientes efectos adversos y frecuencias comunicadas se han determinado a partir de comunicaciones posteriores a la comercialización. Trastornos del sistema inmunitario: Raros: Se han comunicado reacciones alérgicas que incluyen anafilaxia, en pacientes que reciben ULTIVA junto con uno o más agentes anestésicos. Trastornos cardiacos:Raros: Se han comunicado asistolia/paro cardiaco, usualmente precedidos por bradicardia, en pacientes que reciben ULTIVA junto con uno o más agentes anestésicos.
Advertencias.
ULTIVA sólo debe administrarse en un servicio totalmente equipado para la vigilancia y soporte de las funciones respiratoria y cardiovascular, y por personas capacitadas específicamente en el uso de fármacos anestésicos y en el reconocimiento y tratamiento de los efectos adversos esperados de los opioides potentes, incluyendo reanimación respiratoria y cardiaca. Esta capacitación debe incluir el establecimiento y mantenimiento de una vía respiratoria permeable y ventilación asistida. Como ocurre con todos los opioides, ULTIVA no se recomienda para emplearse como único agente en anestesia general. Los pacientes con hipersensibilidad conocida a los opioides de una clase diferente pueden presentar una reacción de hipersensibilidad después de la administración de ULTIVA. Debe tenerse precaución antes de administrar remifentaniloo en esos pacientes (ver Contraindicaciones). Rigidez muscular - prevención y tratamiento: A las dosis recomendadas puede producirse rigidez muscular. Como sucede con otros opioides, la incidencia de la rigidez muscular está relacionada con la dosis y velocidad de administración. Por tanto, las perfusiones en bolo deben administrarse durante períodos no menores de 30 segundos. La rigidez muscular inducida por ULTIVA debe tratarse en el contexto del trastorno clínico de los pacientes, con medidas de soporte apropiadas. La rigidez muscular excesiva que ocurre durante la inducción de la anestesia debe tratarse con la administración de un agente bloqueador neuromuscular o agentes hipnóticos adicionales, o ambas cosas. La rigidez muscular que se observa durante el uso de ULTIVA como un analgésico, puede tratarse suspendiendo o disminuyendo la velocidad de administración de ULTIVA. La resolución de la rigidez muscular después de la suspensión de la perfusión de ULTIVA se produce en el transcurso de unos minutos. En forma alternativa se puede administrar un antagonista opioide, aunque esto puede revertir o atenuar el efecto analgésico del ULTIVA. Depresión respiratoria - tratamiento: Como sucede con todos los opioides potentes, la analgesia profunda se acompaña con depresión respiratoria de grado muy manifiesto. Por tanto, ULTIVA solamente debe usarse en áreas en las cuales se disponga de servicios para vigilar y atender depresión respiratoria. La aparición de depresión respiratoria debe tratarse en forma apropiada, incluyendo la reducción de 50% en la velocidad de la perfusión, o su suspensión temporal. A diferencia de otros análogos del fentanilo, no se ha visto que ULTIVA cause depresión respiratoria recurrente, aún después de una administración prolongada. Sin embargo, como existen muchos factores que pueden afectar la recuperación postoperatoria, es importante asegurar que se hayan alcanzado la consciencia plena y la ventilación espontánea adecuada antes que el paciente sea dado de alta del área de recuperación. Efectos cardiovasculares: La hipotensión y la bradicardia (ver Reacciones adversas) pueden tratarse con la reducción de la velocidad de la perfusión de ULTIVA, o la dosis de anestésicos concurrentes, o mediante el uso de líquidos intravenosos, agentes vasopresores o anticolinérgicos, según sea apropiado. Es posible que los pacientes debilitados, hipovolémicos y de edad avanzada, sean más sensibles a los efectos cardiovasculares del ULTIVA. Desaparición rápida de acción: Debido a la neutralización muy rápida del ULTIVA, no habrá actividad opioide residual dentro de 5 a 10 minutos después de la discontinuación de este fármaco. En los pacientes sometidos a procedimientos quirúrgicos, en los cuales se anticipa dolor postoperatorio, se deben administrar analgésicos antes, o inmediatamente después de la discontinuación de ULTIVA. Debe permitirse que transcurra un tiempo suficiente para alcanzar el efecto máximo del analgésico de acción más prolongada. La elección del analgésico debe ser apropiada para el procedimiento quirúrgico del paciente y el nivel de cuidados postoperatorios. Suspensión del Tratamiento: Al suspender abruptamente el tratamiento, en especial después de la administración de remifentanilo durante periodos prolongados, con poca frecuencia se han reportado síntomas, incluyendo taquicardia, hipertensión y agitación. Cuando se han presentado estos síntomas, ha sido beneficioso reintroducir la perfusión y disminuir progresivamente su uso. Administración inadvertida: Puede persistir una cantidad de ULTIVA en el espacio muerto de la línea i.v., o en la cánula, o en ambos sitios, suficiente para causar depresión respiratoria, apnea y/o rigidez muscular, si la línea se somete a una descarga copiosa de líquidos i.v., u otros fármacos. Esto se puede evitar administrando ULTIVA en una línea i.v., de flujo rápido, o dedicada que sea limpiada adecuadamente de fármaco residual, o que se retire al suspenderse la administración de ULTIVA. Farmacodependencia: Como ocurre con otros opioides ULTIVA puede producir dependencia.
Interacciones.
ULTIVA no se metaboliza por la plasmacolinesterasa, por lo cual no se anticipan interacciones con fármacos metabolizados por esta enzima. Como sucede con otros opioides, ULTIVA disminuye las cantidades o dosis de anestésicos i.v., e inhalados, y benzodiacepinas requeridas para la anestesia (ver Dosificación). Si no se reducen las dosis de fármacos depresores del SNC administrados concomitantemente, es posible que los pacientes experimenten un aumento en la incidencia de efectos adversos asociados con estos agentes. Los efectos cardiovasculares de ULTIVA (hipotensión y bradicardia), se pueden exacerbar en los pacientes que reciben concomitantemente fármacos depresores cardiacos, como beta-bloqueadores y agentes bloqueadores del canal del calcio. Embarazo y lactancia: Embarazo: No se dispone de estudios adecuados y bien controlados en mujeres embarazadas. ULTIVA sólo debe usarse durante el embarazo si el beneficio potencial justifica el riesgo potencial para el feto. Trabajo de parto y parto: No se ha demostrado el perfil de seguridad de ULTIVA durante el trabajo del parto y el parto. Los datos disponibles son insuficientes para recomendar ULTIVA para uso durante el trabajo de parto y la operación cesárea. El remifentanilo cruza la barrera placentaria, y los análogos del fentanilo pueden causar depresión respiratoria en el niño. Lactancia: Se desconoce si el remifentanilo se excreta en la leche humana. Sin embargo, como los análogos del fentanilo se excretan en la leche humana, y se ha encontrado material relacionado con el remifentanilo en la leche de rata con dosificación de este fármaco, debe tenerse cuidado cuando se administre ULTIVA a una madre lactante. Efectos sobre la capacidad de conducir y operar maquinaria: Si se considera una posible alta temprana, después de un tratamiento con el uso de agentes anestésicos, debe recomendarse a los pacientes no conducir vehículos ni operar maquinaria.
Incompatibilidades.
ULTIVA sólo debe reconstituirse y diluirse con las soluciones de perfusión recomendadas (ver Instrucciones para su Uso/Manejo). No debe reconstituirse y diluirse o mezclarse con solución de Ringer Lactato o con solución de dextrosa al 5% y Ringer lactato. ULTIVA no se debe mezclar con propofol en la misma bolsa de perfusión previo a la administración. No se recomienda la administración de ULTIVA en la misma línea i.v., con sangre/suero/plasma. Esterasas no especificas presentes en los hemoderivados pueden causar hidrólisis de ULTIVA a su metabolito inactivo. ULTIVA no debe mezclarse con otros agentes terapéuticos previamente a su administración.
Conservación.
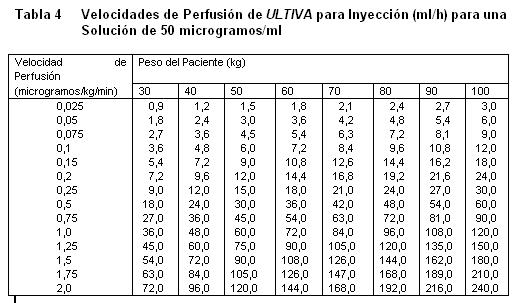
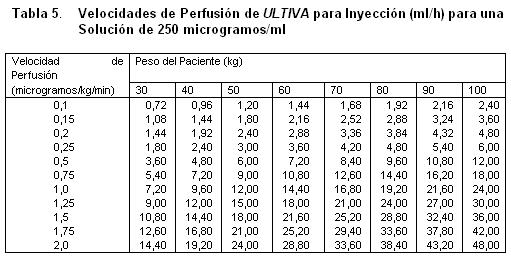
Almacenar a 25°C, o por debajo de esta temperatura. La solución reconstituida de ULTIVA es química y físicamente estable durante 24 horas a temperatura ambiente (25°C). Sin embargo, ULTIVA no contiene un preservativo antimicrobiano y, por tanto, debe tenerse cuidado en asegurar la esterilidad de las soluciones preparadas, el producto reconstituido debe usarse prontamente, y descartarse el material no usado. Vida de Anaquel: La fecha de caducidad se indica en el empaque. Instrucciones para su Uso/Manejo: ULTIVA es estable durante 24 horas a temperatura ambiente (25°C) después de su reconstitución y dilución adicional a 20 a 250 microgramos/mL (50 microgramos/ml es la dilución recomendada para adultos y 20 a 25 microgramos/mL para pacientes pediátricos de 1 ó más años de edad) con uno de los siguientes líquidos i.v., listados a continuación: Agua esterilizada para inyecciones, dextrosa al 5% para inyección, dextrosa al 5% y cloruro de sodio al 0,9% para inyección. cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,45% para inyección. Se ha visto que ULTIVA es compatible con los siguientes líquidos i.v., cuando se administra en una perfusión i.v., corriente: Solución de Ringer Lactato para inyección. Solución de dextrosa al 5% y Ringer Lactato para inyección. Remifentanilo puede ser administrado en bolo a través de una vía intravenosa por la cual se estén administrando soluciones de propofol, solución Ringer Lactato y solución de Dextrosa 5%/Ringer Lactato. Sin embargo Remifentanilo no debe ser agregado a soluciones destinadas a ser administradas por perfusión, que contengan propofol, Solución de Ringer lactatro o Solución de dextrosa 5%/Ringer lactato. Es decir, no debe ser mezclado con estas soluciones antes de la administración. Las siguientes tablas proporcionan directrices para las velocidades de perfusión de ULTIVA:
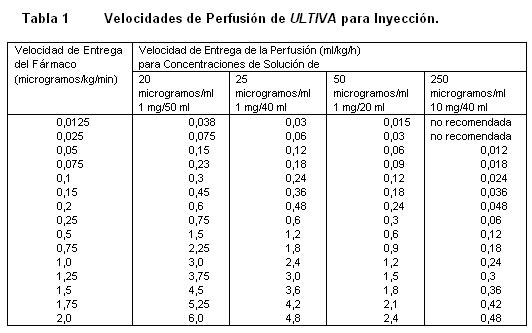
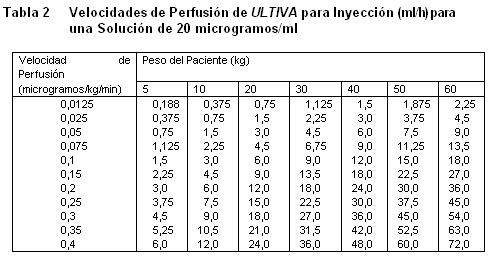
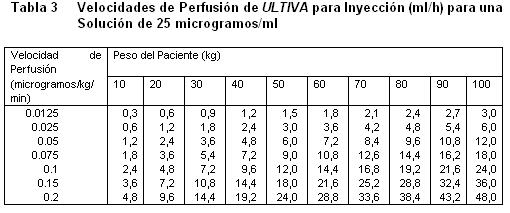
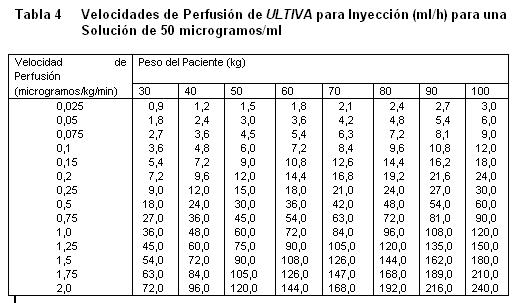
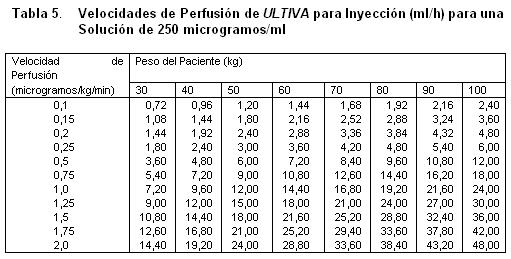
Sobredosificación.
Síntomas y Signos: Como ocurre con todos los analgésicos opioides potentes, la sobredosificación se manifestaría por una extensión de acciones farmacológicamente predecibles del remifentanilo. Debido a la duración de acción muy corta del
ULTIVA, el potencial de efectos perjudiciales debidos a su sobredosificación, está limitado al período inmediatamente posterior a la administración del fármaco. La respuesta a la suspensión del medicamento es rápida, con retorno a la línea basal dentro de un lapso de 10 minutos. Tratamiento: En el caso de una sobredosificación, o sospecha de una sobredosis, realice las siguientes acciones: suspenda la administración de ULTIVA, mantenga una vía respiratoria permeable, inicie ventilación asistida o controlada con oxígeno, y mantenga una función cardiovascular adecuada. Si la respiración deprimida se asocia con rigidez muscular, puede requerirse un agente bloqueador neuromuscular para facilitar la respiración asistida o controlada. Se pueden emplear líquidos intravenosos y agentes vasopresores para el tratamiento de la hipotensión, y otras medidas de soporte. Es posible proporcionar la administración intravenosa de un antagonista opioide, como la naloxona, como un antídoto específico para tratar la depresión respiratoria severa y la rigidez muscular. Es improbable que la duración de la depresión respiratoria, después de una sobredosis de ULTIVA, exceda la duración de acción del antagonista opioide.
Presentación.
Ultiva 1 mg: envases conteniendo 5 ampollas de 3 mL cada una. Ultiva 2 mg: ULTIVA inyección para uso i.v., está disponible como: 1 mg de polvo liofilizado de remifentanilo en frascos de 3 ml. 2 mg de polvo liofilizado de remifentanilo en frascos de 5 ml. 5 mg de polvo liofilizado de remifentanilo en frascos de 10 ml. Envases conteniendo 5 ampollas de 5 mL cada una. Ultiva 5 mg: envases conteniendo 5 ampollas de 10 mL cada una.
ULTIVAMR
GLAXOSMITHKLINE
Polvo liof. p/solución inyectable 2 mg
Analgésico.
Composición.
El remifentanilo para inyección es un liofilizado sin preservativos, sin endotoxinas, estéril, de color blanco a blanco grisáceo, para ser reconstituido antes de su uso. Cuando se reconstituye en la forma recomendada, las soluciones de remifentanilo para inyección son claras e incoloras, y contienen 1 mg/ml de base de remifentanilo como clorhidrato de remifentanilo. Lista de excipientes: Glicina. Forma farmacéutica: Liofilizado para ser reconstituido y administrado vía intravenosa (I.V).
Farmacología.
Farmacodinamia: Código ATC: N01AH06. Mecanismo de Acción: El remifentaniloo es un agonista mu-opioide selectivo, con un rápido inicio y duración muy corta de acción. La actividad mu-opioide de ULTIVA es antagonizada por antagonistas narcóticos, como la naloxona. Efectos farmacodinámicos: Las mediciones de histamina, realizadas en pacientes y voluntarios normales, no han mostrado elevación en los niveles de histamina después de la administración de ULTIVA, en bolo a dosis de hasta 30 microgramos/kg.
Farmacocinética.
Absorción: Las concentraciones sanguíneas de ULTIVA son proporcionales a la dosis administrada en la extensión de los límites de dosis recomendados. Por cada aumento de 0,1 microgramos/kg/min en la velocidad de la perfusión, la concentración sanguínea de ULTIVA aumentará 2,5 nanogramos/mL. Distribución: El volumen central de distribución es de 100 mL/kg, y el volumen de distribución en estado estacionario es de 350 mL/kg. El remifentanilo exhibe un grado de fijación a proteínas plasmáticas de 70%. Metabolismo. El remifentanilo es un opioide metabolizado por esterasa, que es susceptible al metabolismo por esterasas inespecíficas de la sangre y tejidos. El metabolismo del remifentanilo da por resultado la formación del metabolito ácido carboxílico, esencialmente inactivo (1/4.600 de potencia del remifentanilo). La vida media del metabolito en adultos sanos es aproximadamente de 2 horas. Se recupera cerca de 95% de ULTIVA en la orina como el metabolito ácido carboxílico. El remifentanilo no es un sustrato de la colinesterasa plasmática. Eliminación: Después de la administración de las dosis recomendadas de remifentanilo, la vida media biológica efectiva es de 3 a 10 minutos. La depuración promedio del remifentanilo en adultos jóvenes sanos es de 40 mL/min/kg. Poblaciones de pacientes especiales: Anestesia cardiaca: La depuración del remifentanilo se ve reducida hasta en un 20% durante el bypass cardiopulmonar hipotérmico (28°C). La disminución de la temperatura corporal reduce la depuración de eliminación en 3% por oC. Insuficiencia renal: La recuperación rápida de la sedación y la analgesia, basada en el ULTIVA, no se ve afectada por el estado renal. La farmacocinética de ULTIVA no cambia significativamente en pacientes con varios grados de insuficiencia renal, aún después de la administración de hasta 3 días, en condiciones de cuidados intensivos. La depuración del metabolito ácido carboxílico está reducida en los pacientes con deterioro renal. En los pacientes en cuidados intensivos con insuficiencia renal de grado moderado/severo, la concentración del metabolito ácido carboxílico puede exceder 250 veces el nivel del remifentanilo en estado estacionario en algunos pacientes. Los datos clínicos demuestran que la acumulación del metabolito no da por resultado efectos mu-opioides clínicamente pertinentes, aún después de la administración de perfusiones de ULTIVA por hasta 3 días en estos pacientes. No hay indicios de que el remifentanilo sea extraído durante la terapia de reemplazo renal. El metabolito ácido carboxílico es extraído durante la hemodiálisis, en cuando menos 30%. Insuficiencia hepática: La farmacocinética de ULTIVA no sufre cambios en los pacientes con insuficiencia hepática severa que están en espera de trasplante de hígado, o durante la fase anhepática de la cirugía de trasplante de hígado. Es posible que los pacientes con insuficiencia hepática severa sean ligeramente más sensibles a los efectos depresores respiratorios del remifentanilo. Estos pacientes deben ser vigilados estrechamente, y la dosis de ULTIVA debe titularse de acuerdo a la necesidad del paciente. Pacientes pediátricos: En los pacientes pediátricos de 5 días a 17 años de edad, la depuración promedio y el volumen de distribución en estado estacionario de remifentanilo son mayores en los niños más pequeños, y declinan a valores de adulto joven sano, hacia los 17 años de edad. La vida media del remifentanilo no es significativamente distinta en los neonatos, lo que sugiere que los cambios en el efecto analgésico, después de los cambios en la velocidad de perfusión de ULTIVA, deben ser rápidos y similares a los que se observan en adultos jóvenes sanos. La farmacocinética del metabolito ácido carboxílico en los pacientes pediátricos de 2 a 17 años de edad, es similar a la observada en adultos después de la corrección por las diferencias en peso corporal. Personas de edad avanzada: La depuración del remifentanilo está ligeramente reducida (aproximadamente en 25%) en los pacientes de edad avanzada (mayores de 65 años de edad), en comparación con los pacientes jóvenes. La actividad farmacodinámica del remifentanilo aumenta con la edad. Los pacientes de edad avanzada tienen EC50 de remifentanilo en la formación de ondas delta en el electroencefalograma (EEG), que es 50% inferior que en pacientes jóvenes, por lo cual la dosis inicial de ULTIVA se debe reducir en 50% en los sujetos de edad avanzada, y luego titularse cuidadosamente para cubrir la necesidad individual del paciente. Transferencia placentaria y a la leche: En una prueba clínica realizada en mujeres, la concentración de remifentanilo en la sangre fetal fue aproximadamente del 50% de la sangre materna. La relación arteriovenosa fetal de las concentraciones de remifentanilo fue aproximadamente 30%, lo que sugiere metabolismo del remifentanilo en el neonato. Datos preclínicos de seguridad: La administración intratecal de la formulación de glicina sin remifentanilo a perros causó agitación, dolor y disfunción de los miembros posteriores, e incoordinación. Se cree que estos efectos son secundarios al excipiente glicina. La glicina es un excipiente usado comúnmente en productos i.v., y este hallazgo no tiene pertinencia respecto a la administración i.v., de remifentanilo. El remifentanilo, como otros agonistas opioides, produjo aumentos en la duración del potencial de acción (APD, del inglés action potential duration) en fibras de Purkinje aisladas de perro. Con remifentanilo, los efectos se observaron a concentraciones de 1 micromolar, o más altas (que son más altas que las concentraciones plasmáticas que se observan en la práctica clínica). No hubo efectos a una concentración de 0,1 micromolar. El metabolito principal del remifentanilo, ácido carboxílico, no tuvo efecto alguno sobre la APD hasta la máxima concentración probada de 10 micromolar. Se encontró material relacionado con remifentanilo en la leche de ratas después de la dosificación con ese fármaco. Los estudios de transferencia placentaria realizados en ratas y conejas mostraron que las crías están expuestas a ULTIVA o sus metabolitos, o ambos, durante el crecimiento y el desarrollo. No se han encontrado hallazgos adicionales clínicamente pertinentes.
Indicaciones.
ULTIVA se indica como un agente analgésico para usarse durante la inducción y/o mantenimiento de la anestesia general durante procedimientos quirúrgicos, con inclusión de la cirugía cardiaca, así como para la continuación de la analgesia en el período postoperatorio inmediato, bajo vigilancia cercana, durante la transición a una analgesia de acción más prolongada. ULTIVA se indica para proveer analgesia y sedación a pacientes en cuidados intensivos, ventilados mecánicamente.
Dosificación.
ULTIVA debe administrarse únicamente en servicios completamente equipados para la vigilancia y el soporte de las funciones cardiovascular y respiratoria, y por personas capacitadas específicamente para usar fármacos anestésicos y reconocer y tratar los efectos adversos esperados de los opioides potentes, con inclusión de la reanimación respiratoria y cardiaca. Tal capacitación debe incluir el establecimiento y mantenimiento de una vía respiratoria permeable y una ventilación asistida. Las perfusiones continuas de ULTIVA deben administrarse mediante un dispositivo de perfusión calibrado a una línea i.v., de flujo rápido, o a través de una línea i.v. dedicada especialmente. Esta línea de perfusión debe estar conectada a la cánula venosa, o estar cerca de la misma y preparada para minimizar la posibilidad de un espacio muerto (ver Instrucciones para su Uso/Manejo para obtener información adicional, que incluye tablas con ejemplos de velocidades de perfusión por peso corporal, para ayudar a titular ULTIVA según las necesidades anestésicas del paciente). Se debe tener cuidado, tanto en evitar la obstrucción o desconexión de las líneas de perfusión, como al limpiar las líneas para retirar los residuos de ULTIVA después de su uso (ver Advertencias). ULTIVA sólo debe utilizarse vía intravenosa, por lo cual no se debe administrar mediante inyección epidural o intratecal (ver Contraindicaciones). Después de su reconstitución, ULTIVA para inyección es estable durante un periodo de 24 horas, a temperatura ambiente (25°C), y se recomienda diluir adicionalmente 20 a 250 microgramos/ml (50 microgramos/ml es la dilución recomendada para adultos, y 20 a 25 microgramos/ml para pacientes pediátricos de un año de edad o mayores) con uno de los siguientes líquidos intravenosos, listados a continuación: agua esterilizada para inyección, dextrosa al 5% para inyección, dextrosa al 5% y cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,45% para inyección (ver Instrucciones para su Uso/Manejo para obtener información adicional, que incluye tablas para ayudar a titular ULTIVA según las necesidades anestésicas del paciente). La administración de ULTIVA durante la anestesia general debe individualizarse con base en la respuesta del paciente. No se recomienda para emplearse como único agente en anestesia general. Anestesia general: Adultos: La siguiente tabla resume las velocidades de perfusión iniciales y los límites de la dosis.
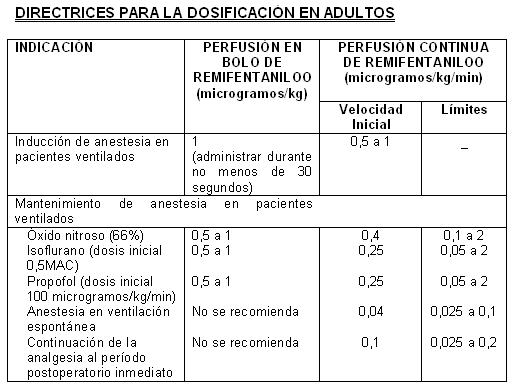
Cuando se administra con perfusión en bolo en la inducción, ULTIVA debe administrarse durante un lapso no inferior a 30 segundos. Administrado a las dosis recomendadas anteriormente, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tanto, el isoflurano y el propofol deben administrarse según las recomendaciones anteriores para evitar una profundidad excesiva de la anestesia (ver Medicación concomitante en esta sección). No se dispone de datos sobre recomendaciones de dosificación concernientes al uso simultáneo de otros hipnóticos con ULTIVA. Inducción de la anestesia: En la inducción de la anestesia, ULTIVA debe administrarse con un agente hipnótico, como propofol, tiopentona o isoflurano. ULTIVA puede administrarse a una velocidad de perfusión de 0,5 a 1 microgramos/kg/min, con o sin una perfusión en bolo inicial de 1 microgramo/kg, durante un lapso no inferior a 30 segundos. Si ha de realizarse una intubación endotraqueal después de transcurrir más de 8 a 10 minutos a partir de la iniciación de la perfusión de ULTIVA, entonces no es necesario practicar una perfusión en bolo. Mantenimiento de la anestesia: Después de la intubación endotraqueal, es necesario disminuir la velocidad de perfusión de ULTIVA, de acuerdo a la técnica anestésica y en la forma indicada en la tabla de arriba. Debido a la rápida iniciación y corta duración de la acción del remifentanilo, la velocidad de administración durante la anestesia puede titularse ascendentemente, en incrementos de 25% a 100%, o descendentemente, en reducciones de 25% a 50%, cada 2 a 5 minutos, para alcanzar el nivel deseado de respuesta mu-opioide. En respuesta a una anestesia ligera, es posible administrar perfusiones complementarias en bolo cada 2 a 5 minutos. Anestesia en pacientes anestesiados, en respiración espontánea y con vía aérea asegurada (p.ej., anestesia con mascarilla laríngea): En pacientes anestesiados con ventilación espontánea y con vía aérea asegurada, es probable que ocurra una depresión respiratoria. Es necesario tener un cuidado especial al ajustar la dosis a los requerimientos del paciente, ya que puede requerirse un soporte ventilatorio. La velocidad inicial de perfusión recomendada para analgesia complementaria en pacientes anestesiados con ventilación espontánea, es de 0,04 microgramos/kg/min titulados hasta alcanzar el efecto. Se han estudiado límites de velocidades de perfusión de 0,025 a 0,1 microgramos/kg/min. No se recomiendan inyecciones en bolo en pacientes anestesiados con ventilación espontánea. Continuación al período postoperatorio inmediato: En caso de que no se haya establecido anteriormente alguna analgesia de duración más prolongada al final de la cirugía, podría ser necesario continuar con ULTIVA para mantener la analgesia durante el período postoperatorio inmediato, hasta que la analgesia de acción más prolongada haya alcanzado su efecto máximo. En los pacientes ventilados, se debe seguir titulando la velocidad de perfusión hasta alcanzar el efecto. En los pacientes que se encuentran respirando espontáneamente, la velocidad de perfusión de ULTIVA debe disminuirse inicialmente a una tasa de 0,1 microgramos/kg/min. Posteriormente, la velocidad de perfusión puede aumentarse o reducirse, en no más de 0,025 microgramos/kg/min cada 5 minutos, con el fin de equilibrar el nivel de analgesia y la frecuencia respiratoria del paciente. ULTIVA sólo debe emplearse en un servicio completamente equipado para la vigilancia y el soporte de las funciones cardiovascular y respiratoria, bajo estrecha supervisión de personas capacitadas específicamente en el reconocimiento y tratamiento de los efectos respiratorios de los opioides potentes. No se recomienda el uso de inyecciones en bolo de ULTIVA para tratar el dolor durante el período postoperatorio en pacientes que estén respirando espontáneamente. Medicación concomitante: ULTIVA disminuye las cantidades o dosis de anestésicos inhalados, hipnóticos o benzodiacepinas, requeridos para la anestesia (ver Interacciones). Las dosis de los siguientes agentes utilizados en anestesia: isoflurano, tiopentona, propofol y temazepam, han sido reducidas hasta en un 75%, cuando se emplean concurrentemente con ULTIVA. Directrices para la discontinuación: Debido al muy rápido efecto de acción de ULTIVA, no se presentará actividad opioide residual dentro de un lapso de 5 a 10 minutos después de su discontinuación. En aquellos pacientes sometidos a procedimientos quirúrgicos, en los cuales se anticipa dolor postoperatorio, se deben administrar analgésicos de manera previa, o inmediatamente después de la discontinuación de ULTIVA. Se debe permitir que transcurra un tiempo suficiente para que se alcance el efecto máximo del analgésico de acción prolongada. La elección del analgésico debe ser adecuada, según el procedimiento quirúrgico del paciente y el nivel de atención postoperatoria. Pacientes pediátricos (1 a 12 años de edad): Inducción de la anestesia. Los datos disponibles resultan insuficientes para hacer una recomendación sobre dosificación. Mantenimiento de la anestesia:
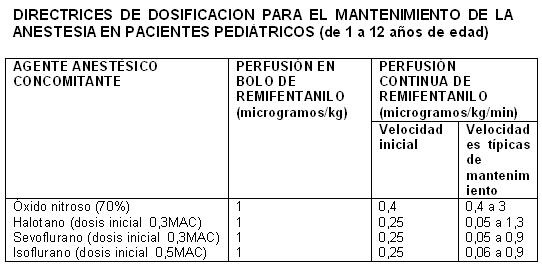
Cuando se practica la perfusión en bolo, ULTIVA debe administrarse durante un lapso no inferior a 30 segundos. Si no se ha administrado una dosis simultánea en bolo, no se debe iniciar la cirugía sino hasta que hayan transcurrido cuando menos 5 minutos después de iniciar la perfusión de ULTIVA. Se debe vigilar a los pacientes pediátricos, y se debe titular la dosis hasta alcanzar la profundidad de analgesia apropiada para el procedimiento quirúrgico. Medicación concomitante: A las dosis recomendadas arriba, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tal razón, el isoflurano, halotano y sevoflurano deben administrarse en la forma recomendada arriba, para evitar una profundidad excesiva de la anestesia. No se dispone de datos sobre las recomendaciones de dosificación en el uso simultáneo de otros hipnóticos con ULTIVA (ver Dosificación - Anestesia general, Adultos, Medicación concomitante). Directrices para la discontinuación: Después de la discontinuación de la perfusión, la desaparición del efecto analgésico de ULTIVA es rápida y similar a la que se observa en los pacientes adultos. Deben anticiparse e implementarse requerimientos analgésicos postoperatorios apropiados (ver Dosificación - Anestesia general, Adultos, Directrices para la discontinuación). Neonatos y lactantes (de edad menor a 1 año): El perfil farmacocinético de ULTIVA en neonatos y lactantes (de edad menor a un año) es comparable al que se observa en los adultos, después de la corrección por las diferencias en el peso corporal. Sin embargo, los datos clínicos disponibles son insuficientes para hacer recomendaciones sobre dosificación para este grupo de edad. Anestesia cardiaca: Adultos:

Período de inducción de la anestesia: Después de la administración de hipnótico para lograr la pérdida de la consciencia, ULTIVA se debe administrar a una velocidad inicial de perfusión de 1 microgramo/kg/min. En los pacientes quirúrgicos cardiacos no se recomienda el uso de perfusiones en bolo de ULTIVA durante la inducción. No se debe practicar intubación endotraqueal durante un lapso de cuando menos 5 minutos después de iniciarse la perfusión. Período de Mantenimiento de la anestesia: Después de la intubación endotraqueal, la velocidad de la perfusión de ULTIVA se debe titular de acuerdo a la necesidad del paciente. También se pueden administrar dosis complementarias en bolo, según se requiera. A los pacientes cardiacos de alto riesgo, como los que presentan función ventricular deficiente, se debe administrar una dosis máxima en bolo de 0,5 microgramos/kg. Estas recomendaciones de dosificación también aplican durante el bypass cardiopulmonar hipotérmico (ver Farmacocinética). Medicación concomitante: A las dosis recomendadas arriba, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tanto, se deben administrar isoflurano y propofol en la forma que se recomienda arriba, para evitar una profundidad excesiva en la anestesia. No se dispone de datos sobre las recomendaciones de dosificación en el uso simultáneo de otros hipnóticos con ULTIVA (ver Dosificación - Anestesia general, Adultos, Medicación concomitante). Continuación de la analgesia postoperatoria antes de la extubación: Se recomienda que la perfusión de ULTIVA se mantenga a la velocidad intraoperatoria final, durante la transferencia de los pacientes al área de cuidados postoperatorios. Al llegar a esta área, el nivel de analgesia y sedación del paciente debe vigilarse estrechamente, y la velocidad de la perfusión de ULTIVA ajustarse, para cubrir los requerimientos individuales del paciente. Directrices para la discontinuación: Con anterioridad a la discontinuación de ULTIVA, los pacientes deben recibir analgésicos y sedantes alternativos, con un tiempo suficiente de anticipación. La elección y dosis del agente o agentes, deben ser apropiadas para el nivel de cuidados postoperatorios del paciente (ver Dosificación - Anestesia general, Adultos, Directrices para la discontinuación). Se recomienda que la perfusión de ULTIVA sea discontinuada, reduciendo la velocidad de la perfusión con disminuciones de 25% a intervalos de cuando menos 10 minutos, hasta que la perfusión se suspenda. Durante la separación del paciente del ventilador, la perfusión de ULTIVA no se debe aumentar; sólo se debe producir titulación en descenso complementada, según se requiera, con analgésicos alternativos. Se recomienda que los cambios hemodinámicos, como hipertensión y taquicardia, se traten con agentes alternativos, según sea apropiado. Pacientes pediátricos: Los datos disponibles son insuficientes para hacer una recomendación sobre dosificación para el uso durante la cirugía cardiaca. Uso en cuidados intensivos: Adultos: ULTIVA puede usarse inicialmente, sólo para proporcionar analgesia y sedación en pacientes en cuidados intensivos, ventilados mecánicamente. Se recomienda que ULTIVA se inicie a una velocidad de perfusión de 0,1 microgramos/kg/min a 0,15 microgramos/kg/min. La velocidad de la perfusión se debe titular con incrementos de 0,025 microgramos/kg/min, para alcanzar el nivel deseado de analgesia y sedación. Se debe permitir que transcurra un período de cuando menos 5 minutos entre los ajustes de las dosis. El nivel de analgesia y sedación debe vigilarse cuidadosamente, reevaluarse regularmente, y la velocidad de perfusión de ULTIVA debe ajustarse de acuerdo a la situación que exista. Si se alcanza una velocidad de perfusión de 0,2 microgramos/kg/min y no se logra el nivel deseado de sedación, se recomienda que se inicie la dosificación con un agente sedante apropiado. La dosis del agente sedante debe titularse para obtener el nivel deseado de sedación. Pueden hacerse aumentos adicionales a la velocidad de la perfusión de ULTIVA, en incrementos de 0,025 microgramos/kg/min, si se requiere analgesia adicional. ULTIVA ha sido estudiado en pacientes en cuidados intensivos, en pruebas clínicas bien controladas, por períodos de hasta 3 días. Existen datos limitados de pruebas clínicas adicionales por períodos de duración más prolongados. La siguiente tabla resume las velocidades de perfusión iniciales y los límites típicos de dosis para proporcionar analgesia y sedación en pacientes individuales:

No se recomiendan dosis en bolo de ULTIVA en situaciones de cuidados intensivos. El uso de ULTIVA reducirá los requerimientos de dosificación de cualquier agente sedantes concomitantes. Las dosis iniciales típicas de agentes sedantes, si se requieren, se proporcionan a continuación.

Para permitir la titulación por separado de agentes respectivos, los agentes sedantes no se deben preparar como una mezcla en la misma bolsa de perfusión. Analgesia adicional para pacientes ventilados sometidos a procedimientos estimulantes: Puede requerirse un aumento en la velocidad de la infusión de ULTIVA, para proporcionar una cobertura analgésica adicional, en los pacientes ventilados sometidos a procedimientos estimulantes o dolorosos, o ambos, como la aspiración endotraqueal, aplicación de apósitos a heridas y fisioterapia. Se recomienda mantener una velocidad de infusión de ULTIVA de cuando menos 0,1 microgramos/kg/min, durante cuando menos 5 minutos antes del inicio del procedimiento estimulante. Pueden practicarse ajustes adicionales en la dosis cada 2 a 5 minutos, en incrementos de 25% a 50%, en anticipación o en respuesta a un requerimiento adicional de analgesia. Se ha administrado una velocidad media de perfusión de 0,25 microgramos/kg/min, máximo de 0,75 microgramos/kg/min, para proporcionar anestesia adicional durante procedimientos estimulantes. Directrices para la discontinuación: Con anterioridad a la discontinuación de ULTIVA, los pacientes deben recibir agentes analgésicos y sedantes alternativos con un tiempo suficiente de anticipación. Se deben anticipar e implementar la selección y dosis apropiadas del agente o agentes. Con el propósito de asegurar una emergencia tranquila de un régimen basado en remifentanilo, se recomienda que la velocidad de la perfusión de ULTIVA se titule en etapas a 0,1 microgramos/kg/min, durante un período de hasta 1 hora anterior a la extubación. Después de la extubación, la velocidad de la perfusión debe disminuirse en reducciones de 25%, a intervalos de cuando menos 10 minutos, hasta que se suspenda la perfusión. Durante la separación del paciente del ventilador, la perfusión de ULTIVA no se debe aumentar; sólo se debe producir titulación en descenso complementada, según se requiera, con analgésicos alternativos. Pacientes pediátricos en cuidados intensivos: No se dispone de datos sobre el uso en pacientes pediátricos. Otras poblaciones: Personas de edad avanzada (mayores de 65 años de edad). Anestesia general: La dosis inicial de ULTIVA administrada a pacientes mayores de 65 años de edad debe ser la mitad de la dosis recomendada para adultos, y titularse de acuerdo a la necesidad individual del paciente, ya que se ha visto un aumento en la sensibilidad a los efectos farmacológicos de ULTIVA en esta población de pacientes. Este ajuste de la dosis aplica para su uso en todas las fases de la anestesia, con inclusión de la inducción, mantenimiento y analgesia postoperatoria inmediata. Anestesia cardiaca: No se requiere reducción de la dosis inicial (ver Dosificación, Anestesia cardiaca, Directrices de dosificación). Cuidados intensivos: No se requiere reducción de la dosis inicial (ver Dosificación, Uso en Cuidados Intensivos). Pacientes obesos: Se recomienda que en los pacientes obesos se reduzca la dosificación de ULTIVA con base en el peso corporal ideal, puesto que la depuración y el volumen de distribución del remifentanilo se correlacionan mejor en esta población, con el peso corporal ideal que con el peso corporal real. Insuficiencia renal: En los pacientes con insuficiencia renal, incluyendo a los sometidos a terapia de reemplazo renal, no es necesario realizar ajustes en la dosificación en relación a la usada en adultos sanos, ya que el perfil farmacocinético de ULTIVA está inalterado en esta población de pacientes. Insuficiencia hepática: No es necesario realizar ajuste alguno en la dosis inicial, en relación con la usada en adultos sanos, puesto que el perfil farmacocinético de ULTIVA no está alterado en esta población de pacientes. Sin embargo, es posible que los pacientes con insuficiencia hepática severa sean ligeramente más sensibles a los efectos depresores respiratorios del remifentanilo. Estos pacientes deben ser motivo de vigilancia estrecha, y la dosis de ULTIVA titularse de acuerdo a la necesidad del paciente. Neurocirugía: La experiencia clínica limitada en los pacientes sometidos a neurocirugía no ha mostrado que se requieran recomendaciones especiales de dosificación. Pacientes con ASA III/IV. Anestesia general: Como debe esperarse que los efectos hemodinámicos de los opioides potentes sean más pronunciados en los pacientes con ASA III/IV, debe tenerse precaución en la administración de ULTIVA en esta población. Por tanto, se recomienda reducción de la dosis inicial y titulación subsiguiente hasta lograr el efecto. Anestesia cardiaca: No se requiere reducción de la dosis inicial (ver Dosificación, Anestesia Cardiaca, Directrices de dosificación).
Contraindicaciones.
Como la formulación contiene glicina, ULTIVA está contraindicado para uso epidural e intratecal (ver Datos preclínicos de seguridad). ULTIVA se contraindica en pacientes con hipersensibilidad conocida a cualquier componente de la preparación, y otros análogos del fentanilo.
Reacciones adversas.
Los efectos adversos se listan a continuación por clase de sistema de órganos y frecuencia de ocurrencia. Las frecuencias se definen como muy común (≥ 1/10), común (≥ 1/100 a < 1/10), no común (≥ 1/1.000 a < 1/100), raro (≥ 1/10.000 a < 1/1.000) y muy raro ( < 1/10.000). Datos de pruebas clínicas:Los efectos adversos más comunes que se asocian con ULTIVA son extensiones directas de farmacología agonista mu-opioide. A continuación se presenta la incidencia general comunicada, determinada por todas las fases de estudios de anestesia controlados, a dosis recomendadas. Estos efectos adversos se resuelven en cuestión de minutos, después de la discontinuación o reducción de la velocidad de administración de ULTIVA. Trastornos del sistema nervioso: Muy común: Rigidez del músculo esquelético. Raro: Sedación (durante la recuperación de la anestesia general). Trastornos cardiacos: Común: Bradicardia. Trastornos vasculares: Muy común: Hipotensión. Común: Hipertensión postoperatoria. Trastornos respiratorias, torácicos y mediastínicos: Comunes: Depresión respiratoria aguda, apnea. No común: Hipoxia. Trastornos gastrointestinales: Muy comunes: Náusea, vómitos. No común: Estreñimiento. Trastornos de la piel y del tejido subcutáneo: Común: Prurito. Trastornos generales y del sitio de administración: Comunes: Temblor postoperatorio. No comunes: Dolores postoperatorios. Datos posteriores a la comercialización: Los siguientes efectos adversos y frecuencias comunicadas se han determinado a partir de comunicaciones posteriores a la comercialización. Trastornos del sistema inmunitario: Raros: Se han comunicado reacciones alérgicas que incluyen anafilaxia, en pacientes que reciben ULTIVA junto con uno o más agentes anestésicos. Trastornos cardiacos: Raros: Se han comunicado asistolia/paro cardiaco, usualmente precedidos por bradicardia, en pacientes que reciben ULTIVA junto con uno o más agentes anestésicos.
Advertencias.
ULTIVA sólo debe administrarse en un servicio totalmente equipado para la vigilancia y soporte de las funciones respiratoria y cardiovascular, y por personas capacitadas específicamente en el uso de fármacos anestésicos y en el reconocimiento y tratamiento de los efectos adversos esperados de los opioides potentes, incluyendo reanimación respiratoria y cardiaca. Esta capacitación debe incluir el establecimiento y mantenimiento de una vía respiratoria permeable y ventilación asistida. Como ocurre con todos los opioides, ULTIVA no se recomienda para emplearse como único agente en anestesia general. Los pacientes con hipersensibilidad conocida a los opioides de una clase diferente pueden presentar una reacción de hipersensibilidad después de la administración de ULTIVA. Debe tenerse precaución antes de administrar remifentaniloo en esos pacientes (ver Contraindicaciones). Rigidez muscular - prevención y tratamiento: A las dosis recomendadas puede producirse rigidez muscular. Como sucede con otros opioides, la incidencia de la rigidez muscular está relacionada con la dosis y velocidad de administración. Por tanto, las perfusiones en bolo deben administrarse durante períodos no menores de 30 segundos. La rigidez muscular inducida por ULTIVA debe tratarse en el contexto del trastorno clínico de los pacientes, con medidas de soporte apropiadas. La rigidez muscular excesiva que ocurre durante la inducción de la anestesia debe tratarse con la administración de un agente bloqueador neuromuscular o agentes hipnóticos adicionales, o ambas cosas. La rigidez muscular que se observa durante el uso de ULTIVA como un analgésico, puede tratarse suspendiendo o disminuyendo la velocidad de administración de ULTIVA. La resolución de la rigidez muscular después de la suspensión de la perfusión de ULTIVA se produce en el transcurso de unos minutos. En forma alternativa se puede administrar un antagonista opioide, aunque esto puede revertir o atenuar el efecto analgésico del ULTIVA. Depresión respiratoria - tratamiento: Como sucede con todos los opioides potentes, la analgesia profunda se acompaña con depresión respiratoria de grado muy manifiesto. Por tanto, ULTIVA solamente debe usarse en áreas en las cuales se disponga de servicios para vigilar y atender depresión respiratoria. La aparición de depresión respiratoria debe tratarse en forma apropiada, incluyendo la reducción de 50% en la velocidad de la perfusión, o su suspensión temporal. A diferencia de otros análogos del fentanilo, no se ha visto que ULTIVA cause depresión respiratoria recurrente, aún después de una administración prolongada. Sin embargo, como existen muchos factores que pueden afectar la recuperación postoperatoria, es importante asegurar que se hayan alcanzado la consciencia plena y la ventilación espontánea adecuada antes que el paciente sea dado de alta del área de recuperación. Efectos cardiovasculares: La hipotensión y la bradicardia (ver Reacciones Adversas) pueden tratarse con la reducción de la velocidad de la perfusión de ULTIVA, o la dosis de anestésicos concurrentes, o mediante el uso de líquidos intravenosos, agentes vasopresores o anticolinérgicos, según sea apropiado. Es posible que los pacientes debilitados, hipovolémicos y de edad avanzada, sean más sensibles a los efectos cardiovasculares del ULTIVA. Desaparición rápida de acción: Debido a la neutralización muy rápida del ULTIVA, no habrá actividad opioide residual dentro de 5 a 10 minutos después de la discontinuación de este fármaco. En los pacientes sometidos a procedimientos quirúrgicos, en los cuales se anticipa dolor postoperatorio, se deben administrar analgésicos antes, o inmediatamente después de la discontinuación de ULTIVA. Debe permitirse que transcurra un tiempo suficiente para alcanzar el efecto máximo del analgésico de acción más prolongada. La elección del analgésico debe ser apropiada para el procedimiento quirúrgico del paciente y el nivel de cuidados postoperatorios. Suspensión del Tratamiento: Al suspender abruptamente el tratamiento, en especial después de la administración de remifentanilo durante periodos prolongados, con poca frecuencia se han reportado síntomas, incluyendo taquicardia, hipertensión y agitación. Cuando se han presentado estos síntomas, ha sido beneficioso reintroducir la perfusión y disminuir progresivamente su uso. Administración inadvertida: Puede persistir una cantidad de ULTIVA en el espacio muerto de la línea i.v., o en la cánula, o en ambos sitios, suficiente para causar depresión respiratoria, apnea y/o rigidez muscular, si la línea se somete a una descarga copiosa de líquidos i.v., u otros fármacos. Esto se puede evitar administrando ULTIVA en una línea i.v., de flujo rápido, o dedicada que sea limpiada adecuadamente de fármaco residual, o que se retire al suspenderse la administración de ULTIVA. Farmacodependencia: Como ocurre con otros opioides ULTIVA puede producir dependencia.
Interacciones.
ULTIVA no se metaboliza por la plasmacolinesterasa, por lo cual no se anticipan interacciones con fármacos metabolizados por esta enzima. Como sucede con otros opioides, ULTIVA disminuye las cantidades o dosis de anestésicos i.v., e inhalados, y benzodiacepinas requeridas para la anestesia (ver Dosificación). Si no se reducen las dosis de fármacos depresores del SNC administrados concomitantemente, es posible que los pacientes experimenten un aumento en la incidencia de efectos adversos asociados con estos agentes. Los efectos cardiovasculares de ULTIVA (hipotensión y bradicardia), se pueden exacerbar en los pacientes que reciben concomitantemente fármacos depresores cardiacos, como beta-bloqueadores y agentes bloqueadores del canal del calcio. Embarazo y lactancia: Embarazo: No se dispone de estudios adecuados y bien controlados en mujeres embarazadas. ULTIVA sólo debe usarse durante el embarazo si el beneficio potencial justifica el riesgo potencial para el feto. Trabajo de parto y parto: No se ha demostrado el perfil de seguridad de ULTIVA durante el trabajo del parto y el parto. Los datos disponibles son insuficientes para recomendar ULTIVA para uso durante el trabajo de parto y la operación cesárea. El remifentanilo cruza la barrera placentaria, y los análogos del fentanilo pueden causar depresión respiratoria en el niño. Lactancia: Se desconoce si el remifentanilo se excreta en la leche humana. Sin embargo, como los análogos del fentanilo se excretan en la leche humana, y se ha encontrado material relacionado con el remifentanilo en la leche de rata con dosificación de este fármaco, debe tenerse cuidado cuando se administre ULTIVA a una madre lactante. Efectos sobre la capacidad de conducir y operar maquinaria: Si se considera una posible alta temprana, después de un tratamiento con el uso de agentes anestésicos, debe recomendarse a los pacientes no conducir vehículos ni operar maquinaria.
Incompatibilidades.
ULTIVA sólo debe reconstituirse y diluirse con las soluciones de perfusión recomendadas (ver Instrucciones para su Uso/Manejo). No debe reconstituirse y diluirse o mezclarse con solución de Ringer Lactato o con solución de dextrosa al 5% y Ringer lactato. ULTIVA no se debe mezclar con propofol en la misma bolsa de perfusión previo a la administración. No se recomienda la administración de ULTIVA en la misma línea i.v., con sangre/suero/plasma. Esterasas no especificas presentes en los hemoderivados pueden causar hidrólisis de ULTIVA a su metabolito inactivo. ULTIVA no debe mezclarse con otros agentes terapéuticos previamente a su administración.
Conservación.
Almacenar a 25°C, o por debajo de esta temperatura. La solución reconstituida de ULTIVA es química y físicamente estable durante 24 horas a temperatura ambiente (25°C). Sin embargo, ULTIVA no contiene un preservativo antimicrobiano y, por tanto, debe tenerse cuidado en asegurar la esterilidad de las soluciones preparadas, el producto reconstituido debe usarse prontamente, y descartarse el material no usado. Vida de Anaquel: La fecha de caducidad se indica en el empaque. Instrucciones para su Uso/Manejo: ULTIVA es estable durante 24 horas a temperatura ambiente (25°C) después de su reconstitución y dilución adicional a 20 a 250 microgramos/mL (50 microgramos/ml es la dilución
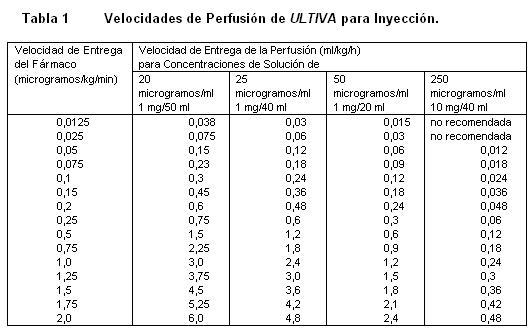
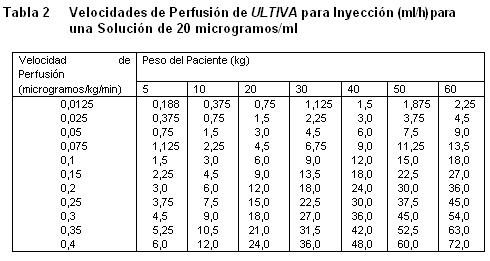
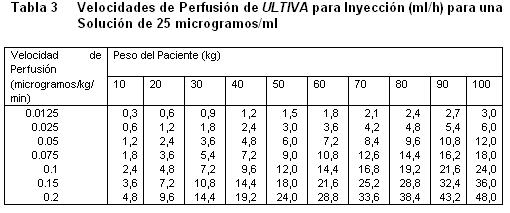
recomendada para adultos y 20 a 25 microgramos/mL para pacientes pediátricos de 1 ó más años de edad) con uno de los siguientes líquidos i.v., listados a continuación: Agua esterilizada para inyecciones, dextrosa al 5% para inyección, dextrosa al 5% y cloruro de sodio al 0,9% para inyección. cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,45% para inyección. Se ha visto que ULTIVA es compatible con los siguientes líquidos i.v., cuando se administra en una perfusión i.v., corriente: Solución de Ringer Lactato para inyección. Solución de dextrosa al 5% y Ringer Lactato para inyección. Remifentanilo puede ser administrado en bolo a través de una vía intravenosa por la cual se estén administrando soluciones de propofol, solución Ringer Lactato y solución de Dextrosa 5%/Ringer Lactato. Sin embargo, Remifentanilo no debe ser agregado a soluciones destinadas a ser administradas por perfusión, que contengan propofol, Solución de Ringer lactatro o Solución de dextrosa 5%/ Ringer lactato. Es decir, no debe ser mezclado con estas soluciones antes de la administración. Las siguientes tablas proporcionan directrices para las velocidades de perfusión de ULTIVA:
Sobredosificación.
Síntomas y Signos: Como ocurre con todos los analgésicos opioides potentes, la sobredosificación se manifestaría por una extensión de acciones farmacológicamente predecibles del remifentanilo. Debido a la duración de acción muy corta del ULTIVA, el potencial de efectos perjudiciales debidos a su sobredosificación, está limitado al período inmediatamente posterior a la administración del fármaco. La respuesta a la suspensión del medicamento es rápida, con retorno a la línea basal dentro de un lapso de 10 minutos. Tratamiento: En el caso de una sobredosificación, o sospecha de una sobredosis, realice las siguientes acciones: suspenda la administración de ULTIVA, mantenga una vía respiratoria permeable, inicie ventilación asistida o controlada con oxígeno, y mantenga una función cardiovascular adecuada. Si la respiración deprimida se asocia con rigidez muscular, puede requerirse un agente bloqueador neuromuscular para facilitar la respiración asistida o controlada. Se pueden emplear líquidos intravenosos y agentes vasopresores para el tratamiento de la hipotensión, y otras medidas de soporte. Es posible proporcionar la administración intravenosa de un antagonista opioide, como la naloxona, como un antídoto específico para tratar la depresión respiratoria severa y la rigidez muscular. Es improbable que la duración de la depresión respiratoria, después de una sobredosis de ULTIVA, exceda la duración de acción del antagonista opioide.
Presentación.
Ultiva 1 mg: envases conteniendo 5 ampollas de 3 mL cada una. Ultiva 2 mg: ULTIVA inyección para uso i.v., está disponible como: 1 mg de polvo liofilizado de remifentanilo en frascos de 3 ml. 2 mg de polvo liofilizado de remifentanilo en frascos de 5 ml. 5 mg de polvo liofilizado de remifentanilo en frascos de 10 ml. Envases conteniendo 5 ampollas de 5 mL cada una. Ultiva 5 mg: envases conteniendo 5 ampollas de 10 mL cada una.
ULTIVAMR
GLAXOSMITHKLINE
Polvo liof. p/solución inyectable 5 mg
Analgésico.
Composición.
El remifentanilo para inyección es un liofilizado sin preservativos, sin endotoxinas, estéril, de color blanco a blanco grisáceo, para ser reconstituido antes de su uso. Cuando se reconstituye en la forma recomendada, las soluciones de remifentanilo para inyección son claras e incoloras, y contienen 1 mg/ml de base de remifentanilo como clorhidrato de remifentanilo. Lista de excipientes: Glicina. Forma farmacéutica: Liofilizado para ser reconstituido y administrado vía intravenosa (I.V).
Farmacología.
Farmacodinamia: Código ATC: N01AH06. Mecanismo de Acción: El remifentaniloo es un agonista mu-opioide selectivo, con un rápido inicio y duración muy corta de acción. La actividad mu-opioide de ULTIVA es antagonizada por antagonistas narcóticos, como la naloxona. Efectos farmacodinámicos: Las mediciones de histamina, realizadas en pacientes y voluntarios normales, no han mostrado elevación en los niveles de histamina después de la administración de ULTIVA, en bolo a dosis de hasta 30 microgramos/kg.
Farmacocinética.
Absorción: Las concentraciones sanguíneas de ULTIVA son proporcionales a la dosis administrada en la extensión de los límites de dosis recomendados. Por cada aumento de 0,1 microgramos/kg/min en la velocidad de la perfusión, la concentración sanguínea de ULTIVA aumentará 2,5 nanogramos/mL. Distribución: El volumen central de distribución es de 100 mL/kg, y el volumen de distribución en estado estacionario es de 350 mL/kg. El remifentanilo exhibe un grado de fijación a proteínas plasmáticas de 70%. Metabolismo. El remifentanilo es un opioide metabolizado por esterasa, que es susceptible al metabolismo por esterasas inespecíficas de la sangre y tejidos. El metabolismo del remifentanilo da por resultado la formación del metabolito ácido carboxílico, esencialmente inactivo (1/4.600 de potencia del remifentanilo). La vida media del metabolito en adultos sanos es aproximadamente de 2 horas. Se recupera cerca de 95% de ULTIVA en la orina como el metabolito ácido carboxílico. El remifentanilo no es un sustrato de la colinesterasa plasmática. Eliminación: Después de la administración de las dosis recomendadas de remifentanilo, la vida media biológica efectiva es de 3 a 10 minutos. La depuración promedio del remifentanilo en adultos jóvenes sanos es de 40 mL/min/kg. Poblaciones de pacientes especiales: Anestesia cardiaca: La depuración del remifentanilo se ve reducida hasta en un 20% durante el bypass cardiopulmonar hipotérmico (28°C). La disminución de la temperatura corporal reduce la depuración de eliminación en 3% por oC. Insuficiencia renal: La recuperación rápida de la sedación y la analgesia, basada en el ULTIVA, no se ve afectada por el estado renal. La farmacocinética de ULTIVA no cambia significativamente en pacientes con varios grados de insuficiencia renal, aún después de la administración de hasta 3 días, en condiciones de cuidados intensivos. La depuración del metabolito ácido carboxílico está reducida en los pacientes con deterioro renal. En los pacientes en cuidados intensivos con insuficiencia renal de grado moderado/severo, la concentración del metabolito ácido carboxílico puede exceder 250 veces el nivel del remifentanilo en estado estacionario en algunos pacientes. Los datos clínicos demuestran que la acumulación del metabolito no da por resultado efectos mu-opioides clínicamente pertinentes, aún después de la administración de perfusiones de ULTIVA por hasta 3 días en estos pacientes. No hay indicios de que el remifentanilo sea extraído durante la terapia de reemplazo renal. El metabolito ácido carboxílico es extraído durante la hemodiálisis, en cuando menos 30%. Insuficiencia hepática: La farmacocinética de ULTIVA no sufre cambios en los pacientes con insuficiencia hepática severa que están en espera de trasplante de hígado, o durante la fase anhepática de la cirugía de trasplante de hígado. Es posible que los pacientes con insuficiencia hepática severa sean ligeramente más sensibles a los efectos depresores respiratorios del remifentanilo. Estos pacientes deben ser vigilados estrechamente, y la dosis de ULTIVA debe titularse de acuerdo a la necesidad del paciente. Pacientes pediátricos: En los pacientes pediátricos de 5 días a 17 años de edad, la depuración promedio y el volumen de distribución en estado estacionario de remifentanilo son mayores en los niños más pequeños, y declinan a valores de adulto joven sano, hacia los 17 años de edad. La vida media del remifentanilo no es significativamente distinta en los neonatos, lo que sugiere que los cambios en el efecto analgésico, después de los cambios en la velocidad de perfusión de ULTIVA, deben ser rápidos y similares a los que se observan en adultos jóvenes sanos. La farmacocinética del metabolito ácido carboxílico en los pacientes pediátricos de 2 a 17 años de edad, es similar a la observada en adultos después de la corrección por las diferencias en peso corporal. Personas de edad avanzada: La depuración del remifentanilo está ligeramente reducida (aproximadamente en 25%) en los pacientes de edad avanzada (mayores de 65 años de edad), en comparación con los pacientes jóvenes. La actividad farmacodinámica del remifentanilo aumenta con la edad. Los pacientes de edad avanzada tienen EC50 de remifentanilo en la formación de ondas delta en el electroencefalograma (EEG), que es 50% inferior que en pacientes jóvenes, por lo cual la dosis inicial de ULTIVA se debe reducir en 50% en los sujetos de edad avanzada, y luego titularse cuidadosamente para cubrir la necesidad individual del paciente. Transferencia placentaria y a la leche: En una prueba clínica realizada en mujeres, la concentración de remifentanilo en la sangre fetal fue aproximadamente del 50% de la sangre materna. La relación arteriovenosa fetal de las concentraciones de remifentanilo fue aproximadamente 30%, lo que sugiere metabolismo del remifentanilo en el neonato. Datos preclínicos de seguridad: La administración intratecal de la formulación de glicina sin remifentanilo a perros causó agitación, dolor y disfunción de los miembros posteriores, e incoordinación. Se cree que estos efectos son secundarios al excipiente glicina. La glicina es un excipiente usado comúnmente en productos i.v., y este hallazgo no tiene pertinencia respecto a la administración i.v., de remifentanilo. El remifentanilo, como otros agonistas opioides, produjo aumentos en la duración del potencial de acción (APD, del inglés action potential duration) en fibras de Purkinje aisladas de perro. Con remifentanilo, los efectos se observaron a concentraciones de 1 micromolar, o más altas (que son más altas que las concentraciones plasmáticas que se observan en la práctica clínica). No hubo efectos a una concentración de 0,1 micromolar. El metabolito principal del remifentanilo, ácido carboxílico, no tuvo efecto alguno sobre la APD hasta la máxima concentración probada de 10 micromolar. Se encontró material relacionado con remifentanilo en la leche de ratas después de la dosificación con ese fármaco. Los estudios de transferencia placentaria realizados en ratas y conejas mostraron que las crías están expuestas a ULTIVA o sus metabolitos, o ambos, durante el crecimiento y el desarrollo. No se han encontrado hallazgos adicionales clínicamente pertinentes.
Indicaciones.
ULTIVA se indica como un agente analgésico para usarse durante la inducción y/o mantenimiento de la anestesia general durante procedimientos quirúrgicos, con inclusión de la cirugía cardiaca, así como para la continuación de la analgesia en el período postoperatorio inmediato, bajo vigilancia cercana, durante la transición a una analgesia de acción más prolongada. ULTIVA se indica para proveer analgesia y sedación a pacientes en cuidados intensivos, ventilados mecánicamente.
Dosificación.
ULTIVA debe administrarse únicamente en servicios completamente equipados para la vigilancia y el soporte de las funciones cardiovascular y respiratoria, y por personas capacitadas específicamente para usar fármacos anestésicos y reconocer y tratar los efectos adversos esperados de los opioides potentes, con inclusión de la reanimación respiratoria y cardiaca. Tal capacitación debe incluir el establecimiento y mantenimiento de una vía respiratoria permeable y una ventilación asistida. Las perfusiones continuas de ULTIVA deben administrarse mediante un dispositivo de perfusión calibrado a una línea i.v., de flujo rápido, o a través de una línea i.v. dedicada especialmente. Esta línea de perfusión debe estar conectada a la cánula venosa, o estar cerca de la misma y preparada para minimizar la posibilidad de un espacio muerto (ver Instrucciones para su Uso/Manejo para obtener información adicional, que incluye tablas con ejemplos de velocidades de perfusión por peso corporal, para ayudar a titular ULTIVA según las necesidades anestésicas del paciente). Se debe tener cuidado, tanto en evitar la obstrucción o desconexión de las líneas de perfusión, como al limpiar las líneas para retirar los residuos de ULTIVA después de su uso (ver Advertencias). ULTIVA sólo debe utilizarse vía intravenosa, por lo cual no se debe administrar mediante inyección epidural o intratecal (ver Contraindicaciones). Después de su reconstitución, ULTIVA para inyección es estable durante un periodo de 24 horas, a temperatura ambiente (25°C), y se recomienda diluir adicionalmente 20 a 250 microgramos/ml (50 microgramos/ml es la dilución recomendada para adultos, y 20 a 25 microgramos/ml para pacientes pediátricos de un año de edad o mayores) con uno de los siguientes líquidos intravenosos, listados a continuación: agua esterilizada para inyección, dextrosa al 5% para inyección, dextrosa al 5% y cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,45% para inyección (ver Instrucciones para su Uso/Manejo para obtener información adicional, que incluye tablas para ayudar a titular ULTIVA según las necesidades anestésicas del paciente). La administración de ULTIVA durante la anestesia general debe individualizarse con base en la respuesta del paciente. No se recomienda para emplearse como único agente en anestesia general. Anestesia general: Adultos: La siguiente tabla resume las velocidades de perfusión iniciales y los límites de la dosis.
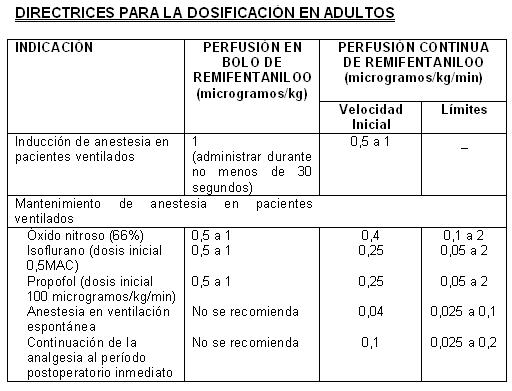
Cuando se administra con perfusión en bolo en la inducción, ULTIVA debe administrarse durante un lapso no inferior a 30 segundos. Administrado a las dosis recomendadas anteriormente, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tanto, el isoflurano y el propofol deben administrarse según las recomendaciones anteriores para evitar una profundidad excesiva de la anestesia (ver Medicación concomitante en esta sección). No se dispone de datos sobre recomendaciones de dosificación concernientes al uso simultáneo de otros hipnóticos con ULTIVA. Inducción de la anestesia: En la inducción de la anestesia, ULTIVA debe administrarse con un agente hipnótico, como propofol, tiopentona o isoflurano. ULTIVA puede administrarse a una velocidad de perfusión de 0,5 a 1 microgramos/kg/min, con o sin una perfusión en bolo inicial de 1 microgramo/kg, durante un lapso no inferior a 30 segundos. Si ha de realizarse una intubación endotraqueal después de transcurrir más de 8 a 10 minutos a partir de la iniciación de la perfusión de ULTIVA, entonces no es necesario practicar una perfusión en bolo. Mantenimiento de la anestesia: Después de la intubación endotraqueal, es necesario disminuir la velocidad de perfusión de ULTIVA, de acuerdo a la técnica anestésica y en la forma indicada en la tabla de arriba. Debido a la rápida iniciación y corta duración de la acción del remifentanilo, la velocidad de administración durante la anestesia puede titularse ascendentemente, en incrementos de 25% a 100%, o descendentemente, en reducciones de 25% a 50%, cada 2 a 5 minutos, para alcanzar el nivel deseado de respuesta mu-opioide. En respuesta a una anestesia ligera, es posible administrar perfusiones complementarias en bolo cada 2 a 5 minutos. Anestesia en pacientes anestesiados, en respiración espontánea y con vía aérea asegurada (p.ej., anestesia con mascarilla laríngea): En pacientes anestesiados con ventilación espontánea y con vía aérea asegurada, es probable que ocurra una depresión respiratoria. Es necesario tener un cuidado especial al ajustar la dosis a los requerimientos del paciente, ya que puede requerirse un soporte ventilatorio. La velocidad inicial de perfusión recomendada para analgesia complementaria en pacientes anestesiados con ventilación espontánea, es de 0,04 microgramos/kg/min titulados hasta alcanzar el efecto. Se han estudiado límites de velocidades de perfusión de 0,025 a 0,1 microgramos/kg/min. No se recomiendan inyecciones en bolo en pacientes anestesiados con ventilación espontánea. Continuación al período postoperatorio inmediato: En caso de que no se haya establecido anteriormente alguna analgesia de duración más prolongada al final de la cirugía, podría ser necesario continuar con ULTIVA para mantener la analgesia durante el período postoperatorio inmediato, hasta que la analgesia de acción más prolongada haya alcanzado su efecto máximo. En los pacientes ventilados, se debe seguir titulando la velocidad de perfusión hasta alcanzar el efecto. En los pacientes que se encuentran respirando espontáneamente, la velocidad de perfusión de ULTIVA debe disminuirse inicialmente a una tasa de 0,1 microgramos/kg/min. Posteriormente, la velocidad de perfusión puede aumentarse o reducirse, en no más de 0,025 microgramos/kg/min cada 5 minutos, con el fin de equilibrar el nivel de analgesia y la frecuencia respiratoria del paciente. ULTIVA sólo debe emplearse en un servicio completamente equipado para la vigilancia y el soporte de las funciones cardiovascular y respiratoria, bajo estrecha supervisión de personas capacitadas específicamente en el reconocimiento y tratamiento de los efectos respiratorios de los opioides potentes. No se recomienda el uso de inyecciones en bolo de ULTIVA para tratar el dolor durante el período postoperatorio en pacientes que estén respirando espontáneamente. Medicación concomitante: ULTIVA disminuye las cantidades o dosis de anestésicos inhalados, hipnóticos o benzodiacepinas, requeridos para la anestesia (ver Interacciones). Las dosis de los siguientes agentes utilizados en anestesia: isoflurano, tiopentona, propofol y temazepam, han sido reducidas hasta en un 75%, cuando se emplean concurrentemente con ULTIVA. Directrices para la discontinuación: Debido al muy rápido efecto de acción de ULTIVA, no se presentará actividad opioide residual dentro de un lapso de 5 a 10 minutos después de su discontinuación. En aquellos pacientes sometidos a procedimientos quirúrgicos, en los cuales se anticipa dolor postoperatorio, se deben administrar analgésicos de manera previa, o inmediatamente después de la discontinuación de ULTIVA. Se debe permitir que transcurra un tiempo suficiente para que se alcance el efecto máximo del analgésico de acción prolongada. La elección del analgésico debe ser adecuada, según el procedimiento quirúrgico del paciente y el nivel de atención postoperatoria. Pacientes pediátricos (1 a 12 años de edad): Inducción de la anestesia. Los datos disponibles resultan insuficientes para hacer una recomendación sobre dosificación. Mantenimiento de la anestesia:
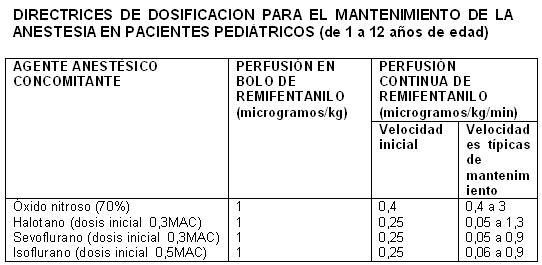
Cuando se practica la perfusión en bolo, ULTIVA debe administrarse durante un lapso no inferior a 30 segundos. Si no se ha administrado una dosis simultánea en bolo, no se debe iniciar la cirugía sino hasta que hayan transcurrido cuando menos 5 minutos después de iniciar la perfusión de ULTIVA. Se debe vigilar a los pacientes pediátricos, y se debe titular la dosis hasta alcanzar la profundidad de analgesia apropiada para el procedimiento quirúrgico. Medicación concomitante: A las dosis recomendadas arriba, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tal razón, el isoflurano, halotano y sevoflurano deben administrarse en la forma recomendada arriba, para evitar una profundidad excesiva de la anestesia. No se dispone de datos sobre las recomendaciones de dosificación en el uso simultáneo de otros hipnóticos con ULTIVA (ver Dosificación - Anestesia general, Adultos, Medicación concomitante). Directrices para la discontinuación: Después de la discontinuación de la perfusión, la desaparición del efecto analgésico de ULTIVA es rápida y similar a la que se observa en los pacientes adultos. Deben anticiparse e implementarse requerimientos analgésicos postoperatorios apropiados (ver Dosificación - Anestesia general, Adultos, Directrices para la discontinuación). Neonatos y lactantes (de edad menor a 1 año): El perfil farmacocinético de ULTIVA en neonatos y lactantes (de edad menor a un año) es comparable al que se observa en los adultos, después de la corrección por las diferencias en el peso corporal. Sin embargo, los datos clínicos disponibles son insuficientes para hacer recomendaciones sobre dosificación para este grupo de edad. Anestesia cardiaca: Adultos:

Período de inducción de la anestesia: Después de la administración de hipnótico para lograr la pérdida de la consciencia, ULTIVA se debe administrar a una velocidad inicial de perfusión de 1 microgramo/kg/min. En los pacientes quirúrgicos cardiacos no se recomienda el uso de perfusiones en bolo de ULTIVA durante la inducción. No se debe practicar intubación endotraqueal durante un lapso de cuando menos 5 minutos después de iniciarse la perfusión. Período de Mantenimiento de la anestesia: Después de la intubación endotraqueal, la velocidad de la perfusión de ULTIVA se debe titular de acuerdo a la necesidad del paciente. También se pueden administrar dosis complementarias en bolo, según se requiera. A los pacientes cardiacos de alto riesgo, como los que presentan función ventricular deficiente, se debe administrar una dosis máxima en bolo de 0,5 microgramos/kg. Estas recomendaciones de dosificación también aplican durante el bypass cardiopulmonar hipotérmico (ver Farmacocinética). Medicación concomitante: A las dosis recomendadas arriba, ULTIVA reduce significativamente la cantidad de agente hipnótico requerida para mantener la anestesia. Por tanto, se deben administrar isoflurano y propofol en la forma que se recomienda arriba, para evitar una profundidad excesiva en la anestesia. No se dispone de datos sobre las recomendaciones de dosificación en el uso simultáneo de otros hipnóticos con ULTIVA (ver Dosificación - Anestesia general, Adultos, Medicación concomitante). Continuación de la analgesia postoperatoria antes de la extubación: Se recomienda que la perfusión de ULTIVA se mantenga a la velocidad intraoperatoria final, durante la transferencia de los pacientes al área de cuidados postoperatorios. Al llegar a esta área, el nivel de analgesia y sedación del paciente debe vigilarse estrechamente, y la velocidad de la perfusión de ULTIVA ajustarse, para cubrir los requerimientos individuales del paciente. Directrices para la discontinuación: Con anterioridad a la discontinuación de ULTIVA, los pacientes deben recibir analgésicos y sedantes alternativos, con un tiempo suficiente de anticipación. La elección y dosis del agente o agentes, deben ser apropiadas para el nivel de cuidados postoperatorios del paciente (ver Dosificación - Anestesia general, Adultos, Directrices para la discontinuación). Se recomienda que la perfusión de ULTIVA sea discontinuada, reduciendo la velocidad de la perfusión con disminuciones de 25% a intervalos de cuando menos 10 minutos, hasta que la perfusión se suspenda. Durante la separación del paciente del ventilador, la perfusión de ULTIVA no se debe aumentar; sólo se debe producir titulación en descenso complementada, según se requiera, con analgésicos alternativos. Se recomienda que los cambios hemodinámicos, como hipertensión y taquicardia, se traten con agentes alternativos, según sea apropiado. Pacientes pediátricos: Los datos disponibles son insuficientes para hacer una recomendación sobre dosificación para el uso durante la cirugía cardiaca. Uso en cuidados intensivos: Adultos: ULTIVA puede usarse inicialmente, sólo para proporcionar analgesia y sedación en pacientes en cuidados intensivos, ventilados mecánicamente. Se recomienda que ULTIVA se inicie a una velocidad de perfusión de 0,1 microgramos/kg/min a 0,15 microgramos/kg/min. La velocidad de la perfusión se debe titular con incrementos de 0,025 microgramos/kg/min, para alcanzar el nivel deseado de analgesia y sedación. Se debe permitir que transcurra un período de cuando menos 5 minutos entre los ajustes de las dosis. El nivel de analgesia y sedación debe vigilarse cuidadosamente, reevaluarse regularmente, y la velocidad de perfusión de ULTIVA debe ajustarse de acuerdo a la situación que exista. Si se alcanza una velocidad de perfusión de 0,2 microgramos/kg/min y no se logra el nivel deseado de sedación, se recomienda que se inicie la dosificación con un agente sedante apropiado. La dosis del agente sedante debe titularse para obtener el nivel deseado de sedación. Pueden hacerse aumentos adicionales a la velocidad de la perfusión de ULTIVA, en incrementos de 0,025 microgramos/kg/min, si se requiere analgesia adicional. ULTIVA ha sido estudiado en pacientes en cuidados intensivos, en pruebas clínicas bien controladas, por períodos de hasta 3 días. Existen datos limitados de pruebas clínicas adicionales por períodos de duración más prolongados. La siguiente tabla resume las velocidades de perfusión iniciales y los límites típicos de dosis para proporcionar analgesia y sedación en pacientes individuales:

No se recomiendan dosis en bolo de ULTIVA en situaciones de cuidados intensivos. El uso de ULTIVA reducirá los requerimientos de dosificación de cualquier agente sedantes concomitantes. Las dosis iniciales típicas de agentes sedantes, si se requieren, se proporcionan a continuación.

Para permitir la titulación por separado de agentes respectivos, los agentes sedantes no se deben preparar como una mezcla en la misma bolsa de perfusión. Analgesia adicional para pacientes ventilados sometidos a procedimientos estimulantes: Puede requerirse un aumento en la velocidad de la infusión de ULTIVA, para proporcionar una cobertura analgésica adicional, en los pacientes ventilados sometidos a procedimientos estimulantes o dolorosos, o ambos, como la aspiración endotraqueal, aplicación de apósitos a heridas y fisioterapia. Se recomienda mantener una velocidad de infusión de ULTIVA de cuando menos 0,1 microgramos/kg/min, durante cuando menos 5 minutos antes del inicio del procedimiento estimulante. Pueden practicarse ajustes adicionales en la dosis cada 2 a 5 minutos, en incrementos de 25% a 50%, en anticipación o en respuesta a un requerimiento adicional de analgesia. Se ha administrado una velocidad media de perfusión de 0,25 microgramos/kg/min, máximo de 0,75 microgramos/kg/min, para proporcionar anestesia adicional durante procedimientos estimulantes. Directrices para la discontinuación: Con anterioridad a la discontinuación de ULTIVA, los pacientes deben recibir agentes analgésicos y sedantes alternativos con un tiempo suficiente de anticipación. Se deben anticipar e implementar la selección y dosis apropiadas del agente o agentes. Con el propósito de asegurar una emergencia tranquila de un régimen basado en remifentanilo, se recomienda que la velocidad de la perfusión de ULTIVA se titule en etapas a 0,1 microgramos/kg/min, durante un período de hasta 1 hora anterior a la extubación. Después de la extubación, la velocidad de la perfusión debe disminuirse en reducciones de 25%, a intervalos de cuando menos 10 minutos, hasta que se suspenda la perfusión. Durante la separación del paciente del ventilador, la perfusión de ULTIVA no se debe aumentar; sólo se debe producir titulación en descenso complementada, según se requiera, con analgésicos alternativos. Pacientes pediátricos en cuidados intensivos: No se dispone de datos sobre el uso en pacientes pediátricos. Otras poblaciones: Personas de edad avanzada (mayores de 65 años de edad). Anestesia general: La dosis inicial de ULTIVA administrada a pacientes mayores de 65 años de edad debe ser la mitad de la dosis recomendada para adultos, y titularse de acuerdo a la necesidad individual del paciente, ya que se ha visto un aumento en la sensibilidad a los efectos farmacológicos de ULTIVA en esta población de pacientes. Este ajuste de la dosis aplica para su uso en todas las fases de la anestesia, con inclusión de la inducción, mantenimiento y analgesia postoperatoria inmediata. Anestesia cardiaca: No se requiere reducción de la dosis inicial (ver Dosificación, Anestesia cardiaca, Directrices de dosificación). Cuidados intensivos: No se requiere reducción de la dosis inicial (ver Dosificación, Uso en Cuidados Intensivos). Pacientes obesos: Se recomienda que en los pacientes obesos se reduzca la dosificación de ULTIVA con base en el peso corporal ideal, puesto que la depuración y el volumen de distribución del remifentanilo se correlacionan mejor en esta población, con el peso corporal ideal que con el peso corporal real. Insuficiencia renal: En los pacientes con insuficiencia renal, incluyendo a los sometidos a terapia de reemplazo renal, no es necesario realizar ajustes en la dosificación en relación a la usada en adultos sanos, ya que el perfil farmacocinético de ULTIVA está inalterado en esta población de pacientes. Insuficiencia hepática: No es necesario realizar ajuste alguno en la dosis inicial, en relación con la usada en adultos sanos, puesto que el perfil farmacocinético de ULTIVA no está alterado en esta población de pacientes. Sin embargo, es posible que los pacientes con insuficiencia hepática severa sean ligeramente más sensibles a los efectos depresores respiratorios del remifentanilo. Estos pacientes deben ser motivo de vigilancia estrecha, y la dosis de ULTIVA titularse de acuerdo a la necesidad del paciente. Neurocirugía: La experiencia clínica limitada en los pacientes sometidos a neurocirugía no ha mostrado que se requieran recomendaciones especiales de dosificación. Pacientes con ASA III/IV. Anestesia general: Como debe esperarse que los efectos hemodinámicos de los opioides potentes sean más pronunciados en los pacientes con ASA III/IV, debe tenerse precaución en la administración de ULTIVA en esta población. Por tanto, se recomienda reducción de la dosis inicial y titulación subsiguiente hasta lograr el efecto. Anestesia cardiaca: No se requiere reducción de la dosis inicial (ver Dosificación, Anestesia Cardiaca, Directrices de dosificación).
Contraindicaciones.
Como la formulación contiene glicina, ULTIVA está contraindicado para uso epidural e intratecal (ver Datos preclínicos de seguridad). ULTIVA se contraindica en pacientes con hipersensibilidad conocida a cualquier componente de la preparación, y otros análogos del fentanilo.
Reacciones adversas.
Los efectos adversos se listan a continuación por clase de sistema de órganos y frecuencia de ocurrencia. Las frecuencias se definen como muy común (≥ 1/10), común (≥ 1/100 a < 1/10), no común (≥ 1/1.000 a < 1/100), raro (≥ 1/10.000 a < 1/1.000) y muy raro ( < 1/10.000). Datos de pruebas clínicas:Los efectos adversos más comunes que se asocian con ULTIVA son extensiones directas de farmacología agonista mu-opioide. A continuación se presenta la incidencia general comunicada, determinada por todas las fases de estudios de anestesia controlados, a dosis recomendadas. Estos efectos adversos se resuelven en cuestión de minutos, después de la discontinuación o reducción de la velocidad de administración de ULTIVA. Trastornos del sistema nervioso: Muy común: Rigidez del músculo esquelético. Raro: Sedación (durante la recuperación de la anestesia general). Trastornos cardiacos: Común: Bradicardia. Trastornos vasculares: Muy común: Hipotensión. Común: Hipertensión postoperatoria. Trastornos respiratorias, torácicos y mediastínicos: Comunes: Depresión respiratoria aguda, apnea. No común: Hipoxia. Trastornos gastrointestinales: Muy comunes: Náusea, vómitos. No común: Estreñimiento. Trastornos de la piel y del tejido subcutáneo: Común: Prurito. Trastornos generales y del sitio de administración: Comunes: Temblor postoperatorio. No comunes: Dolores postoperatorios. Datos posteriores a la comercialización: Los siguientes efectos adversos y frecuencias comunicadas se han determinado a partir de comunicaciones posteriores a la comercialización. Trastornos del sistema inmunitario: Raros: Se han comunicado reacciones alérgicas que incluyen anafilaxia, en pacientes que reciben ULTIVA junto con uno o más agentes anestésicos. Trastornos cardiacos: Raros: Se han comunicado asistolia/paro cardiaco, usualmente precedidos por bradicardia, en pacientes que reciben ULTIVA junto con uno o más agentes anestésicos.
Advertencias.
ULTIVA sólo debe administrarse en un servicio totalmente equipado para la vigilancia y soporte de las funciones respiratoria y cardiovascular, y por personas capacitadas específicamente en el uso de fármacos anestésicos y en el reconocimiento y tratamiento de los efectos adversos esperados de los opioides potentes, incluyendo reanimación respiratoria y cardiaca. Esta capacitación debe incluir el establecimiento y mantenimiento de una vía respiratoria permeable y ventilación asistida. Como ocurre con todos los opioides, ULTIVA no se recomienda para emplearse como único agente en anestesia general. Los pacientes con hipersensibilidad conocida a los opioides de una clase diferente pueden presentar una reacción de hipersensibilidad después de la administración de ULTIVA. Debe tenerse precaución antes de administrar remifentaniloo en esos pacientes (ver Contraindicaciones). Rigidez muscular - prevención y tratamiento: A las dosis recomendadas puede producirse rigidez muscular. Como sucede con otros opioides, la incidencia de la rigidez muscular está relacionada con la dosis y velocidad de administración. Por tanto, las perfusiones en bolo deben administrarse durante períodos no menores de 30 segundos. La rigidez muscular inducida por ULTIVA debe tratarse en el contexto del trastorno clínico de los pacientes, con medidas de soporte apropiadas. La rigidez muscular excesiva que ocurre durante la inducción de la anestesia debe tratarse con la administración de un agente bloqueador neuromuscular o agentes hipnóticos adicionales, o ambas cosas. La rigidez muscular que se observa durante el uso de ULTIVA como un analgésico, puede tratarse suspendiendo o disminuyendo la velocidad de administración de ULTIVA. La resolución de la rigidez muscular después de la suspensión de la perfusión de ULTIVA se produce en el transcurso de unos minutos. En forma alternativa se puede administrar un antagonista opioide, aunque esto puede revertir o atenuar el efecto analgésico del ULTIVA. Depresión respiratoria - tratamiento: Como sucede con todos los opioides potentes, la analgesia profunda se acompaña con depresión respiratoria de grado muy manifiesto. Por tanto, ULTIVA solamente debe usarse en áreas en las cuales se disponga de servicios para vigilar y atender depresión respiratoria. La aparición de depresión respiratoria debe tratarse en forma apropiada, incluyendo la reducción de 50% en la velocidad de la perfusión, o su suspensión temporal. A diferencia de otros análogos del fentanilo, no se ha visto que ULTIVA cause depresión respiratoria recurrente, aún después de una administración prolongada. Sin embargo, como existen muchos factores que pueden afectar la recuperación postoperatoria, es importante asegurar que se hayan alcanzado la consciencia plena y la ventilación espontánea adecuada antes que el paciente sea dado de alta del área de recuperación. Efectos cardiovasculares: La hipotensión y la bradicardia (ver Efectos Adversos) pueden tratarse con la reducción de la velocidad de la perfusión de ULTIVA, o la dosis de anestésicos concurrentes, o mediante el uso de líquidos intravenosos, agentes vasopresores o anticolinérgicos, según sea apropiado. Es posible que los pacientes debilitados, hipovolémicos y de edad avanzada, sean más sensibles a los efectos cardiovasculares del ULTIVA. Desaparición rápida de acción: Debido a la neutralización muy rápida del ULTIVA, no habrá actividad opioide residual dentro de 5 a 10 minutos después de la discontinuación de este fármaco. En los pacientes sometidos a procedimientos quirúrgicos, en los cuales se anticipa dolor postoperatorio, se deben administrar analgésicos antes, o inmediatamente después de la discontinuación de ULTIVA. Debe permitirse que transcurra un tiempo suficiente para alcanzar el efecto máximo del analgésico de acción más prolongada. La elección del analgésico debe ser apropiada para el procedimiento quirúrgico del paciente y el nivel de cuidados postoperatorios. Suspensión del Tratamiento: Al suspender abruptamente el tratamiento, en especial después de la administración de remifentanilo durante periodos prolongados, con poca frecuencia se han reportado síntomas, incluyendo taquicardia, hipertensión y agitación. Cuando se han presentado estos síntomas, ha sido beneficioso reintroducir la perfusión y disminuir progresivamente su uso. Administración inadvertida: Puede persistir una cantidad de ULTIVA en el espacio muerto de la línea i.v., o en la cánula, o en ambos sitios, suficiente para causar depresión respiratoria, apnea y/o rigidez muscular, si la línea se somete a una descarga copiosa de líquidos i.v., u otros fármacos. Esto se puede evitar administrando ULTIVA en una línea i.v., de flujo rápido, o dedicada que sea limpiada adecuadamente de fármaco residual, o que se retire al suspenderse la administración de ULTIVA. Farmacodependencia: Como ocurre con otros opioides ULTIVA puede producir dependencia.
Interacciones.
ULTIVA no se metaboliza por la plasmacolinesterasa, por lo cual no se anticipan interacciones con fármacos metabolizados por esta enzima. Como sucede con otros opioides, ULTIVA disminuye las cantidades o dosis de anestésicos i.v., e inhalados, y benzodiacepinas requeridas para la anestesia (ver Dosificación). Si no se reducen las dosis de fármacos depresores del SNC administrados concomitantemente, es posible que los pacientes experimenten un aumento en la incidencia de efectos adversos asociados con estos agentes. Los efectos cardiovasculares de ULTIVA (hipotensión y bradicardia), se pueden exacerbar en los pacientes que reciben concomitantemente fármacos depresores cardiacos, como beta-bloqueadores y agentes bloqueadores del canal del calcio. Embarazo y lactancia: Embarazo: No se dispone de estudios adecuados y bien controlados en mujeres embarazadas. ULTIVA sólo debe usarse durante el embarazo si el beneficio potencial justifica el riesgo potencial para el feto. Trabajo de parto y parto: No se ha demostrado el perfil de seguridad de ULTIVA durante el trabajo del parto y el parto. Los datos disponibles son insuficientes para recomendar ULTIVA para uso durante el trabajo de parto y la operación cesárea. El remifentanilo cruza la barrera placentaria, y los análogos del fentanilo pueden causar depresión respiratoria en el niño. Lactancia: Se desconoce si el remifentanilo se excreta en la leche humana. Sin embargo, como los análogos del fentanilo se excretan en la leche humana, y se ha encontrado material relacionado con el remifentanilo en la leche de rata con dosificación de este fármaco, debe tenerse cuidado cuando se admi
nistre ULTIVA a una madre lactante. Efectos sobre la capacidad de conducir y operar maquinaria: Si se considera una posible alta temprana, después de un tratamiento con el uso de agentes anestésicos, debe recomendarse a los pacientes no conducir vehículos ni operar maquinaria.
Incompatibilidades.
ULTIVA sólo debe reconstituirse y diluirse con las soluciones de perfusión recomendadas (ver Instrucciones para su Uso/Manejo). No debe reconstituirse y diluirse o mezclarse con solución de Ringer Lactato o con solución de dextrosa al 5% y Ringer lactato. ULTIVA no se debe mezclar con propofol en la misma bolsa de perfusión previo a la administración. No se recomienda la administración de ULTIVA en la misma línea i.v., con sangre/suero/plasma. Esterasas no especificas presentes en los hemoderivados pueden causar hidrólisis de ULTIVA a su metabolito inactivo. ULTIVA no debe mezclarse con otros agentes terapéuticos previamente a su administración.
Conservación.
Almacenar a 25°C, o por debajo de esta temperatura. La solución reconstituida de ULTIVA es química y físicamente estable durante 24 horas a temperatura ambiente (25°C). Sin embargo, ULTIVA no contiene un preservativo antimicrobiano y, por tanto, debe tenerse cuidado en asegurar la esterilidad de las soluciones preparadas, el producto reconstituido debe usarse prontamente, y descartarse el material no usado. Vida de Anaquel: La fecha de caducidad se indica en el empaque. Instrucciones para su Uso/Manejo: ULTIVA es estable durante 24 horas a temperatura ambiente (25°C) después de su reconstitución y dilución adicional a 20 a 250 microgramos/mL (50 microgramos/ml es la dilución recomendada para adultos y 20 a 25 microgramos/mL para pacientes pediátricos de 1 ó más años de edad) con uno de los siguientes líquidos i.v., listados a continuación: Agua esterilizada para inyecciones, dextrosa al 5% para inyección, dextrosa al 5% y cloruro de sodio al 0,9% para inyección. cloruro de sodio al 0,9% para inyección, cloruro de sodio al 0,45% para inyección. Se ha visto que ULTIVA es compatible con los siguientes líquidos i.v., cuando se administra en una perfusión i.v., corriente: Solución de Ringer Lactato para inyección. Solución de dextrosa al 5% y Ringer Lactato para inyección. Remifentanilo puede ser administrado en bolo a través de una vía intravenosa por la cual se estén administrando soluciones de propofol, solución Ringer Lactato y solución de Dextrosa 5%/Ringer Lactato. Sin embargo Remifentanilo no debe ser agregado a soluciones destinadas a ser administradas por perfusión, que contengan propofol, Solución de Ringer lactatro o Solución de dextrosa 5%/ Ringer lactato. Es decir, no debe ser mezclado con estas soluciones antes de la administración. Las siguientes tablas proporcionan directrices para las velocidades de perfusión de ULTIVA:
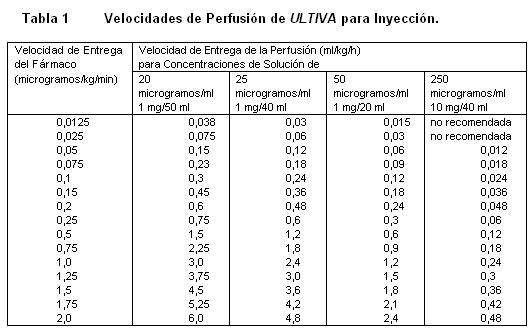
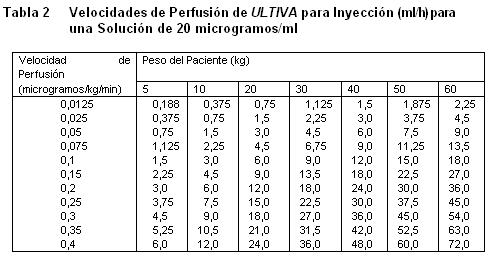
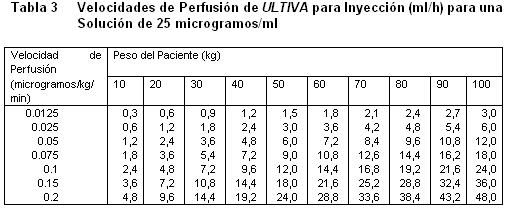
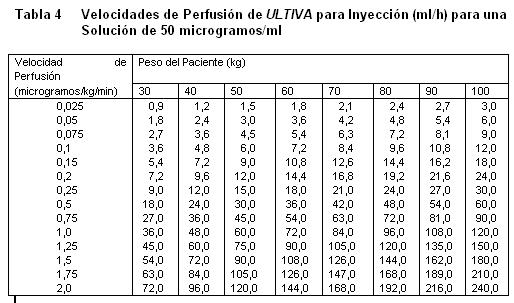
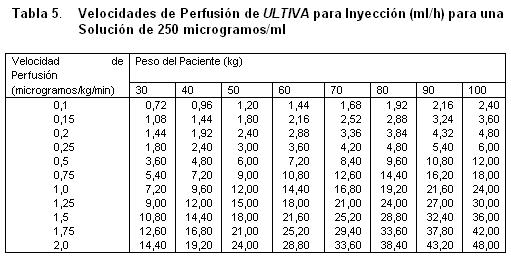
Sobredosificación.
Síntomas y Signos: Como ocurre con todos los analgésicos opioides potentes, la sobredosificación se manifestaría por una extensión de acciones farmacológicamente predecibles del remifentanilo. Debido a la duración de acción muy corta del ULTIVA, el potencial de efectos perjudiciales debidos a su sobredosificación, está limitado al período inmediatamente posterior a la administración del fármaco. La respuesta a la suspensión del medicamento es rápida, con retorno a la línea basal dentro de un lapso de 10 minutos. Tratamiento: En el caso de una sobredosificación, o sospecha de una sobredosis, realice las siguientes acciones: suspenda la administración de ULTIVA, mantenga una vía respiratoria permeable, inicie ventilación asistida o controlada con oxígeno, y mantenga una función cardiovascular adecuada. Si la respiración deprimida se asocia con rigidez muscular, puede requerirse un agente bloqueador neuromuscular para facilitar la respiración asistida o controlada. Se pueden emplear líquidos intravenosos y agentes vasopresores para el tratamiento de la hipotensión, y otras medidas de soporte. Es posible proporcionar la administración intravenosa de un antagonista opioide, como la naloxona, como un antídoto específico para tratar la depresión respiratoria severa y la rigidez muscular. Es improbable que la duración de la depresión respiratoria, después de una sobredosis de ULTIVA, exceda la duración de acción del antagonista opioide.
Presentación.
Ultiva 1 mg: envases conteniendo 5 ampollas de 3 mL cada una. Ultiva 2 mg: ULTIVA inyección para uso i.v., está disponible como: 1 mg de polvo liofilizado de remifentanilo en frascos de 3 ml. 2 mg de polvo liofilizado de remifentanilo en frascos de 5 ml. 5 mg de polvo liofilizado de remifentanilo en frascos de 10 ml. Envases conteniendo 5 ampollas de 5 mL cada una. Ultiva 5 mg: envases conteniendo 5 ampollas de 10 mL cada una.

