VALCOTE ER Comprimidos recubiertos 250mg
ABBOTT
Anticonvulsivo. Antiepiléptico.
Descripción.
El Divalproato de Sodio es un compuesto estable combinado que incluye valproato de sodio y ácido valproico en una relación 1:1 molar y formado durante la neutralización parcial de ácido valproico con 0.5 equivalentes de hidróxido de sodio. El Divalproato de Sodio es designado químicamente como hidrógeno de sodio bis(2- propilpentanoato). El Divalproato de Sodio tiene un peso molecular de 310,41 y se presenta como un polvo blanco con un olor característico. Su fórmula empírica es C16H31NaO4. El Divalproato de Sodio comprimidos de liberación prolongada (ER) está pensado para la administración oral. El Divalproato de Sodio comprimidos de liberación prolongada contiene Divalproato de Sodio en formulación de liberación prolongada para una sola dosis al día equivalente a 250 mg y 500 mg de ácido valproico. Ingredientes Inactivos: Las formulaciones contienen varios ingredientes inactivos. Excipientes: ER 250 mg: Hipromelosa, celulosa microcristalina, lactosa monohidrato, dióxido de silicio, sorbato de potasio, dióxido de titanio, triacetato de glicerol, macrogol, Shellac Glaze en alcohol, alcohol butílico, isopropanol, propilenglicol y colorante FD&C azul N°1. ER 500 mg: Hipromelosa, celulosa microcristalina, lactosa monohidrato, dióxido de silicio, sorbato de potasio, dióxido de titanio, triacetina, triacetato de glicerol, macrogol, óxido de hierro negro y colorante FD&C azul N°1.
Farmacología.
Farmacodinámica: El Divalproato de Sodio se disocia a ion valproato en el tracto gastrointestinal. Los mecanismos por los cuales el valproato ejerce sus efectos terapéuticos no se han establecido. Se ha sugerido que su actividad en la epilepsia está relacionada con las concentraciones crecientes en el cerebro del ácido gamma-aminobutírico (GABA). Farmacocinética - Absorción /Biodisponibilidad: La biodisponibilidad absoluta del divalproato de sodio comprimidos de liberación prolongada (ER), administrado en una dosis única después de una comida fue aproximadamente 90% en relación con la infusión intravenosa. Cuando se administra en dosis diarias totales iguales, la biodisponibilidad del divalproato de sodio ER es menor que la del divalproato de sodio (divalproato de sodio comprimidos con recubrimiento entérico). En cinco estudios de dosis múltiples en sujetos sanos (N =82) y en sujetos con epilepsia (N =86), cuando se administró bajo condiciones de ayuno y de no ayuno, el divalproato de sodio ER dado una vez al día produjo una biodisponibilidad promedio de 89% en relación con una dosis diaria total igual de divalproato de sodio administrado dos veces al día, tres veces al día, o una vez al día. El tiempo medio a las concentraciones plasmáticas máximas de valproato (Cmáx) después de la administración de divalproato de sodio ER se extendió desde 4 a 17 horas. Después de múltiples dosis únicas diarias de divalproato de sodio ER, la fluctuación entre concentraciones máximas y mínimas de valproato de sodio fue 10-20% más bajo que el de divalproato de sodio regular administrado dos veces al día, tres veces al día, o una vez al día. Conversión de divalproato de sodio a divalproato de sodio ER: Cuando el divalproato de sodio ER se da en dosis 8 a 20% más altas que la dosis diaria total de divalproato de sodio, las dos formulaciones son bioequivalentes. En dos estudios randomizados, cruzados, múltiples dosis diarias de divalproato de sodio se compararon a dosis diarias 8 a 20% superiores de divalproato de sodio ER. En estos dos estudios, los regímenes de divalproato de sodio ER y de divalproato de sodio fueron equivalentes con respecto al área bajo la curva (ABC; una medida de la extensión de la biodisponibilidad). Además, el Cmáx del valproato fue más bajo, y Cmín fue mayor o igual, para divalproato de sodio ER en relación a regímenes de divalproato de sodio (ver la tabla siguiente).
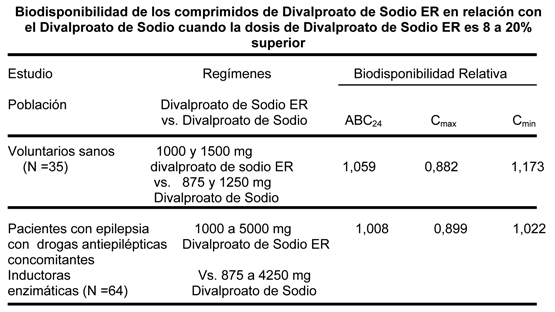
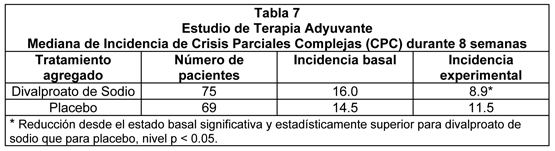
Las drogas antiepilépticas concomitantes (fueron evaluadas topiramato, fenobarbital, carbamazepina, fenitoína, y lamotrigina) que inducen el sistema isoenzima del citocromo P450 no alteraron significativamente la biodisponibilidad del valproato al convertir el Divalproato de Sodio en Divalproato de Sodio ER. Farmacocinética - Distribución: Unión a proteínas: La unión a las proteínas del plasma del valproato es dependiente de la concentración y la fracción libre aumenta desde aproximadamente 10% con 40 mcg/mL a 18,5% con 130 mcg/mL. La unión a las proteínas del valproato se reduce en los ancianos, en pacientes con enfermedades hepáticas crónicas, en pacientes con daño renal, y en la presencia de otras drogas (Ej., aspirina). Inversamente, el valproato puede desplazar ciertas drogas de su unión con proteínas (Ej., fenitoína, carbamazepina, warfarina, y tolbutamida (ver Interacciones para información más detallada sobre las interacciones farmacocinéticas de valproato con otras drogas). Distribución en SNC: Las concentraciones de valproato en el líquido cefalorraquídeo (LCR) se aproximan a las concentraciones libres en el plasma (cerca del 10% de concentración total). Farmacocinética - Metabolismo: El valproato es metabolizado casi enteramente por el hígado. En pacientes adultos con monoterapia, 30 a 50% de una dosis administrada aparece en orina como glucurónido conjugado. La b-oxidación mitocondrial es el otro camino metabólico principal, típicamente involucra a más del 40% de la dosis. Generalmente, menos de 15 a 20% de la dosis es eliminada por otros mecanismos oxidativos. Menos del 3% de una dosis administrada se excreta sin cambios en la orina. La relación entre la dosis y la concentración total de valproato es no lineal; la concentración no aumenta proporcionalmente con la dosis, sino que aumenta en una extensión inferior debido a la unión a proteínas plasmáticas saturables. La cinética de la droga libre es lineal. Farmacocinética - Eliminación: La media de clearance plasmático y volumen de distribución para el valproato total es 0,56 L/hr/1.73 m2 y 11 L/1.73 m2, respectivamente. La media de clearance plasmático y volumen de distribución para el valproato libre es de 4.6 L/hr/1.73 m2 y 92 L/1.73 m2. La media de la vida media terminal para valproato en monoterapia varió desde 9 a 16 horas luego de regímenes de dosis orales de 250 a 1000 mg. Los estimados indicados aplican principalmente a pacientes que no están recibiendo drogas que afectan los sistemas enzimáticos de metabolización hepática. Por ejemplo, los pacientes que están recibiendo drogas antiepilépticas inductoras de enzimas (carbamazepina, fenitoína, y fenobarbital) eliminarán más rápidamente el valproato. Debido a estos cambios en el clearance de valproato, se debe intensificar el monitoreo de las concentraciones del antiepiléptico cada vez que se introducen o retiran antiepilépticos concomitantes. Poblaciones especiales: Recién nacidos: (Nota: La seguridad y efectividad del divalproato de sodio ER en la profilaxis de migraña en pacientes pediátricos no se ha establecido. Por lo tanto, la información abajo es aplicable a la población pediátrica sólo cuando se usa en indicación de epilepsia.) Los niños dentro de los primeros dos meses de vida tienen una capacidad notoriamente reducida para eliminar valproato en comparación con los niños de mayor edad y los adultos. Esto es resultado de un menor clearance (quizás debido a un retardo en el desarrollo de la glucuronosiltransferasa y otros sistemas enzimáticos involucrados en la eliminación de valproato) así como también un mayor volumen de distribución (debido en parte a una menor unión a proteínas plasmáticas). Por ejemplo, en un estudio, la vida media en niños menores de 10 días de edad varió desde 10 a 67 horas en comparación con un rango de 7 a 13 horas en niños mayores a los dos meses. Niños: (Nota: La seguridad y efectividad del divalproato de sodio ER en la profilaxis de migraña en pacientes pediátricos no se ha establecido. Por lo tanto, la información abajo es aplicable a la población pediátrica sólo cuando se usa en indicación de epilepsia.) Los pacientes pediátricos (vale decir, entre 3 meses y 10 años de edad) tienen clearances 50% superiores, expresados en peso (es decir, mL/min/kg) en comparación a adultos. Sobre los 10 años de edad, los niños tienen parámetros farmacocinéticos que se aproximan a los observados en adultos. El perfil farmacocinético del valproato después de la administración de divalproato de sodio ER fue caracterizado en un estudio de dosis múltiple, sin ayuno, abierto, multicéntrico en niños y adolescentes. El divalproato de sodio ER se administró una vez al día en rangos de dosis desde 250 a 1750 mg. La administración de divalproato de sodio ER una vez al día en pacientes pediátricos (10-17 años) produjo unos perfiles de concentración plasmática de ácido valproico-tiempo, similar a aquellos observados en adultos. Ancianos: La capacidad de los pacientes ancianos (rango de edad: 68 a 89 años) para eliminar el valproato ha mostrado estar reducida en comparación con la observada en adultos jóvenes (rango de edad: 22 a 26). El clearance intrínseco se redujo en un 39%; la fracción libre de valproato se aumentó en un 44%. Por consiguiente, en los ancianos se debe reducir la dosis inicial (ver Dosificación). Sexo: No se han observado diferencias en el clearance libre ajustado por área de superficie corporal entre sujetos masculinos y femeninos (4.8 ± 0.17 y 4.7 ± 0.07 L/hr por 1.73 m2, respectivamente). Origen étnico: No se han estudiado los efectos del origen étnico sobre la cinética de valproato. Enfermedad hepática: Ver Contraindicaciones y Advertencias. La enfermedad hepática deteriora la capacidad para eliminar el valproato. En un estudio, el clearance del valproato libre se redujo en un 50% en siete pacientes con cirrosis y en un 16% en cuatro pacientes con hepatitis aguda, comparado con seis sujetos sanos. En dicho estudio, la vida media de valproato se incrementó desde 12 a 18 horas. La enfermedad hepática también está asociada con menores concentraciones de albúmina y mayores fracciones libres (incremento de 2 a 2.6 veces) de valproato. Por consiguiente, el monitoreo de las concentraciones totales puede ser conducente a error dado que las concentraciones libres pueden estar notoriamente elevadas en pacientes con enfermedad hepática mientras que las concentraciones totales pueden parecer normales. Enfermedad renal: Se ha reportado una leve reducción (27%) en el clearance de valproato no unido en pacientes con insuficiencia renal (clearance de creatinina < 10 mL/minuto); sin embargo, la hemodiálisis típicamente reduce las concentraciones de valproato en cerca de un 20%. Por lo tanto, no parece necesario efectuar ajustes de la dosificación en pacientes con insuficiencia renal. La unión a proteínas en estos pacientes se reduce en forma notoria; por lo tanto, el monitoreo de las concentraciones totales puede ser conducente a error. Niveles plasmáticos y Efecto Clínico: La relación entre la concentración plasmática y respuesta clínica no se ha documentado bien. Un factor contribuyente es la unión a proteínas no lineal, concentración-dependiente del valproato, lo cual afecta el clearance de la droga. Por lo tanto, el monitoreo del valproato sérico total no entrega un índice confiable de las especies bioactivas de valproato. Por ejemplo, dado que la unión de valproato a las proteínas plasmáticas es concentración dependiente, la fracción libre aumenta desde aproximadamente 10% en 40 mcg/mL a un 18.5% en 130 mcg/mL. Fracciones libres más altas que lo esperado se presentan en los ancianos, en pacientes hiperlipidémicos y en pacientes con enfermedades hepática y renal. Manía: En un estudio clínico placebo-controlado en manía aguda, los pacientes fueron dosificados para una respuesta clínica con concentraciones plasmáticas mínimas entre 85 y 125 mg/mL. Epilepsia: El rango terapéutico en epilepsia suele considerarse como de ≥50 a 100 mcg/mL de valproato total, aunque algunos pacientes pueden ser controlados con concentraciones plasmáticas más bajas o más elevadas. Estudios Clínicos: Manía: La efectividad de los comprimidos de divalproato de sodio de liberación prolongada para el tratamiento de la manía aguda se basa en parte en los estudios que establecieron la efectividad del divalproato de sodio de liberación retardada para esta indicación. La efectividad de los comprimidos de divalproato de sodio de liberación prolongada fue confirmada en un estudio multicéntrico randomizado, doble ciego, placebo-controlado, grupo paralelo, de tres semanas. El estudio fue diseñado para evaluar la seguridad y la eficacia de los comprimidos de divalproato de sodio de liberación prolongada en el tratamiento del trastorno bipolar I, manía o tipo mixto, en adultos. En este estudio se reclutaron adultos varones y mujeres que tenían un diagnóstico primario actual DSM-IV TR de trastorno bipolar I, manía o tipo mixto, y quiénes fueron hospitalizados por manía aguda. Los comprimidos de divalproato de sodio de liberación prolongada fueron iniciados en una dosis de 25 mg/kg/día una vez al día, aumentando a 500 mg/día al día 3, luego ajustándose para alcanzar concentraciones plasmáticas de valproato en el rango de 85-125 mcg/mL. Las dosis medias diarias de los comprimidos de divalproato de sodio de liberación prolongada para los casos observados fueron 2362 mg (rango: 500-4000), 2874 mg (rango: 1500-4500), 2993 mg (rango: 1500- 4500), 3181 mg (rango: 1500-5000), y 3353 mg (rango: 1500-5500) en los días 1, 5. 10. 15. y 21, respectivamente. Las concentraciones medias de valproato fueron 96.5 mg/mL, 102.1 mcg/mL, 98.5 mcg/mL, 89.5 mcg/mL en los días 5, 10. 15 y 21, respectivamente. Los pacientes fueron evaluados en la Escala de Grado de Manía (MRS; rangos de puntaje 0-52). Los comprimidos de divalproato de sodio de liberación prolongada fueron significativamente más efectivos que placebo en la reducción del puntaje total MRS. Epilepsia: Crisis Parciales Complejas (CPC): La eficacia de divalproato de sodio para reducir la incidencia de crisis parciales complejas (CPC) que se presentan en forma aislada o en combinación con otros tipos de trastornos convulsivos se ha establecido en dos estudios clínicos controlados usando divalproato de sodio (divalproato de sodio comprimidos con recubrimiento entérico). En un estudio multiclínico, controlado con placebo, que utilizó un diseño sumatorio (terapia adyuvante), 144 pacientes que continuaron experimentando ocho o más crisis parciales complejas (CPC) cada ocho semanas, durante un período de ocho semanas de monoterapia con dosis de carbamazepina o fenitoína suficientes para asegurar concentraciones plasmáticas dentro del "rango terapéutico" fueron randomizados para recibir, además de su droga antiepiléptica original (AED), divalproato de sodio o placebo. Los pacientes randomizados debían seguirse por un total de 16 semanas. La tabla 7 presenta los hallazgos.
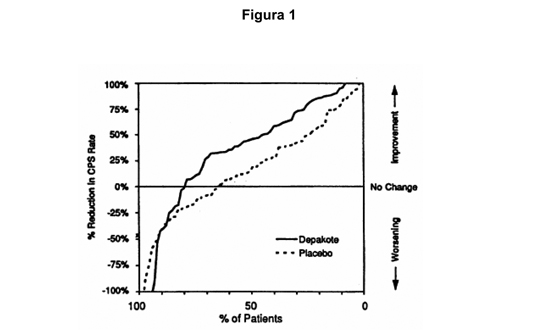
La Figura 1 presenta la proporción de pacientes (eje X) cuyo porcentaje de reducción desde el estado basal en las tasas de crisis parciales complejas fue al menos tan grande como la indicada en el eje Y en el estudio de terapia adyuvante. Un porcentaje de reducción positivo indica una mejoría (es decir, una disminución en la frecuencia de crisis), mientras que un porcentaje de reducción negativo indica un empeoramiento. Por lo tanto, en una imagen de este tipo, la curva para un tratamiento efectivo está desviada hacia la izquierda de la curva para placebo. Esta figura muestra que la proporción de pacientes que lograron algún nivel específico de mejoría fue consistentemente superior para divalproato de sodio que para placebo. Por ejemplo, 45% de los pacientes tratados con divalproato de sodio presentó una reducción de 50% en la tasa de crisis parciales complejas comparado con 23% de los pacientes tratados con placebo.
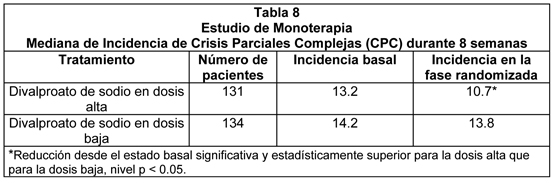
El segundo estudio evaluó la capacidad de divalproato de sodio para reducir la incidencia de crisis parciales complejas (CPC) al ser administrado como droga antiepiléptica (AED) única. El estudio comparó la incidencia de crisis parciales complejas entre los pacientes randomizados ya sea al brazo de tratamiento de dosis alta o baja. Los pacientes calificaban para ingresar a la fase de comparación randomizada de este estudio sólo si: 1) continuaban experimentando una o más crisis parciales complejas por cuatro semanas durante un período de 8 a 12 semanas de duración de monoterapia con dosis adecuadas de una droga antiepiléptica (ej, fenitoína, carbamazepina, fenobarbital, o primidona); y 2) habían realizado una transición exitosa a través de un intervalo de dos semanas a divalproato de sodio. A los pacientes que ingresaron a la fase randomizada se les llevó a su dosis objetivo asignada, reduciendo gradualmente su droga antiepiléptica concomitante, y fueron seguidos durante un intervalo de hasta 22 semanas. Sin embargo, menos del 50% de los pacientes randomizados completaron el estudio. En pacientes convertidos a monoterapia con divalproato de sodio, las concentraciones medias totales de valproato durante monoterapia fueron 71 y 123 mcg/mL en los grupos de dosis baja y alta, respectivamente. La tabla 8 presenta los hallazgos para todos los pacientes randomizados que tuvieron al menos una evaluación post-randomización.
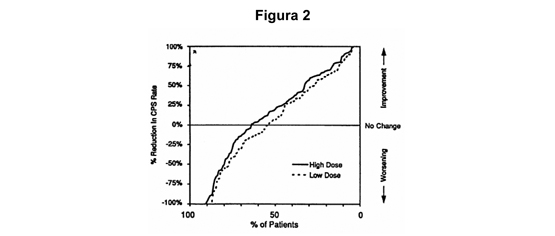
La Figura 2 presenta la proporción de pacientes (eje X) cuya reducción porcentual desde el estado basal en las tasas de convulsiones parciales complejas fue al menos tan elevada como la indicada en el eje Y en el estudio de monoterapia. Una reducción positiva del porcentaje indica una mejoría (ej, un descenso en la frecuencia de las crisis), mientras que una reducción negativa del porcentaje indica empeoramiento. Por lo tanto, en una muestra de este tipo, la curva para un tratamiento más efectivo está desviada hacia la izquierda de la curva para un tratamiento menos efectivo. Esta figura muestra que la proporción de pacientes que lograron cualquier nivel dado de reducción fue consistentemente mayor para la dosis alta de divalproato de sodio que para la dosis baja de divalproato de sodio. Por ejemplo, cuando se cambia de monoterapia con carbamazepina, fenitoína, fenobarbital o primidona a monoterapia con alta dosis de divalproato de sodio, 63% de los pacientes no experimentaron cambio o una reducción en las tasas de convulsiones parciales complejas en comparación con 54% de los pacientes que recibieron baja dosis de divalproato de sodio.
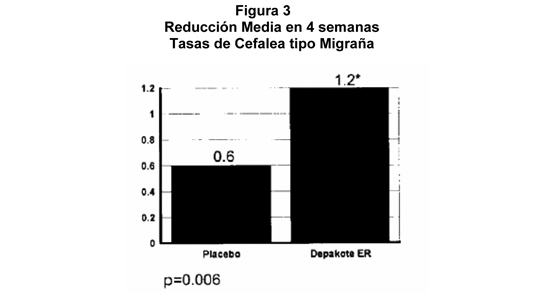
Migraña: Los resultados de un estudio clínico multicéntrico, randomizado, doble ciego, controlado con placebo, grupo paralelo demostraron la efectividad del divalproato de sodio de liberación prolongada en el tratamiento profiláctico de la cefalea tipo migraña. Este estudio reclutó pacientes con una historia de cefalea tipo migraña con o sin aura que ocurrían en promedio dos o más veces al mes por durante los tres meses precedentes. Se excluyeron los pacientes con cefalea tipo "cluster" o cefalea crónica diaria. Se permitieron mujeres en edad fértil en el estudio, si estaban dispuestas a practicar un método eficaz de anticoncepción. Los pacientes quienes experimentaron dos o más cefaleas tipo migraña en un período basal de 4 semanas fueron randomizados en una razón 1:1 a divalproato de sodio de liberación prologada o placebo y tratados por doce semanas. Los pacientes iniciaron tratamiento con 500 mg una vez al día por una semana, y después se aumentó a 1000 mg una vez al día con una opción de disminuir permanentemente la dosis a la anterior de 500 mg una vez al día durante la segunda semana de tratamiento si ocurría intolerancia. Noventa y ocho de 114 pacientes tratados con divalproato de sodio de liberación prologada (86%) y 100 de 110 pacientes tratados con placebo (91%) tratados al menos por dos semanas manteniendo la dosis de 1000 mg una vez al día, por la duración de sus períodos de tratamiento. El resultado del tratamiento fue evaluado basándose en la reducción en la tasa de cefalea tipo migraña en el período de tratamiento de 4 semanas comparado con el período basal. Se trataron pacientes (50 varones, 187 mujeres) en un rango etario de 16 a 69 años, con divalproato de sodio de liberación prologada (n=122) o placebo (n=115). Cuatro pacientes eran menores de 18 años y tres eran mayores de 65 años. Doscientos dos pacientes (101 en cada grupo de tratamiento) completaron el período de tratamiento. La reducción media en la tasa de cefalea tipo migraña en 4 semanas fue 1.2 desde una media basal de 4.4 en el grupo de divalproato de sodio de liberación prolongada, versus 0.6 desde una media basal de 4.2 en el grupo placebo. La diferencia de tratamiento fue estadísticamente significativa (ver Figura 3).
Datos de Seguridad Pre-Clínica: Carcinogénesis, Mutagénesis y Alteración de la Fertilidad: Carcinogénesis: El ácido valproico se administró a ratas Sprague Dawley y ratones ICR (HA/ICR) en dosis de 80 y 170 mg/kg/día (aproximadamente 10 a 50% de la dosis diaria humana máxima en una base de mg/m2) durante dos años. En ambas especies se observaron una variedad de neoplasmas. Los principales hallazgos fueron un incremento estadísticamente significativo en la incidencia de fibrosarcomas subcutáneos en las ratas macho que recibían dosis altas de ácido valproico y una tendencia estadísticamente significativa dosis-relacionada para adenomas pulmonares benignos en ratas macho que recibieron ácido valproico. Se desconoce la significancia de estos hallazgos para seres humanos. Mutagénesis: El valproato no fue mutagénico en un ensayo bacteriano in vitro (test Ames), no produjo efectos letales dominantes en ratas, y no incrementó la frecuencia de aberraciones cromosómicas en un estudio citogenético in vivo en ratas. En un estudio en niños epilépticos que tomaban valproato se ha reportado una mayor frecuencia de intercambio cromátidas hermanas (SCE= Sister Chromatid Exchange), pero esta asociación no se observó en otro estudio realizado en adultos. Existe alguna evidencia que las mayores frecuencias de SCE pueden estar asociadas con epilepsia. Se desconoce la significancia biológica de un incremento en la frecuencia SCE. Alteración de la Fertilidad: Los estudios de toxicidad crónica en ratas y perros jóvenes y adultos demostraron una menor espermatogénesis y atrofia testicular en dosis orales de 400 mg/kg/día o más en ratas (aproximadamente equivalente a o superior a la dosis diaria humana máxima en una base de mg/m2) y 150 mg/kg/día o más en perros (aproximadamente 1.4 veces la dosis diaria humana máxima o más en una base de mg/m2). Los estudios de fertilidad del segmento I en ratas han mostrado que dosis orales hasta 350 mg/kg/día (aproximadamente igual a la dosis diaria humana máxima en una base de mg/m2) durante 60 días no tuvieron efecto sobre la fertilidad. Se desconoce el efecto de valproato sobre el desarrollo testicular y sobre la producción de espermios y fertilidad en seres humanos.
Indicaciones.
Manía: Los comprimidos de Divalproato de Sodio de liberación prolongada están indicados para el tratamiento de episodios maníacos agudos o mixtos asociados con trastorno bipolar, con o sin características psicóticas. Un episodio maníaco es un período distinto de ánimo anormalmente y persistentemente elevado, expansivo, o irritable. Los síntomas típicos de manía incluyen verborrea, hiperactividad motora, poca necesidad de sueño, ideas dispersas, grandiosidad, juicio pobre, agresividad y posible hostilidad. Un episodio mixto es caracterizado por los criterios de un episodio maníaco en conjunto con aquellos para un episodio depresivo mayor (ánimo depresivo, pérdida de interés o de placer en casi todas las actividades). La eficacia de los comprimidos de Divalproato de Sodio de liberación prolongada se basa en parte en los estudios de Divalproato de Sodio comprimidos de liberación retardada en esta indicación, y fue confirmado en un estudio de tres semanas con pacientes que cumplían los criterios DSM-IV para trastorno bipolar I, manía o tipo mixto, quienes fueron hospitalizados por manía aguda. La efectividad de los comprimidos de Divalproato de Sodio de liberación prolongada para el uso a largo plazo en manía, i.e., más de 3 semanas, no se ha demostrado en estudios clínicos controlados. Por lo tanto, los médicos que eligen utilizar los comprimidos de Divalproato de Sodio de liberación prolongada por períodos extensos deben re-evaluar continuamente los riesgos y beneficios a largo plazo de la droga para el paciente individual. Epilepsia: El Divalproato de Sodio comprimidos de liberación prolongada está indicado como monoterapia y terapia adyuvante en el tratamiento de adultos y niños de 10 años o mayores con convulsiones parciales complejas que ocurren ya sea en forma aislada o en asociación con otros tipos de convulsiones. El Divalproato de Sodio comprimidos de liberación prolongada también está indicado como terapia única y adyuvante en el tratamiento de las crisis de ausencia simples y complejas en adultos y niños de 10 años o mayores, y como terapia adyuvante en pacientes adultos y niños de 10 años o mayores con múltiples tipos de trastornos convulsivos que incluyen ausencia. La ausencia simple se define como una muy breve obnubilación sensorial o pérdida de conciencia acompañada de ciertas descargas epilépticas generalizadas sin otros signos clínicos detectables. La ausencia compleja es el término utilizado cuando también están presentes otros signos. Migraña: Los comprimidos de Divalproato de Sodio de liberación prolongada están indicados en la profilaxis de los dolores de cabeza tipo migraña en adultos. No hay evidencia que el Divalproato de Sodio de liberación prolongada sea útil en el tratamiento agudo de los dolores de cabeza tipo migraña. Como el ácido valproico puede ser un peligro para el feto, el Divalproato de Sodio se debe considerar para las mujeres en edad fértil sólo después que este riesgo se ha discutido a fondo con la paciente y se ha pesado contra el potencial beneficio del tratamiento (ver Advertencias - Uso en el Embarazo y Precauciones - Información para los pacientes). Ver Advertencias con respecto a la disfunción hepática fatal.
Dosificación.
General: El Divalproato de Sodio comprimidos de liberación prolongada se ha elaborado para administración oral una vez al día. El Divalproato de Sodio comprimidos de liberación prolongada debe ser tragado entero y no debe ser molido o masticado. Un comprimido de Divalproato de Sodio de liberación prolongada es un producto de liberación prolongada pensado para la administración una vez al día. Manía: Los comprimidos de divalproato de sodio de liberación prolongada se administran por vía oral. La dosis inicial recomendada es 25 mg/kg/día dados una vez al día. La dosis se debe aumentar lo más rápido posible hasta alcanzar la dosis terapéutica más baja que produce el efecto clínico deseado o el rango deseado de concentración plasmática. En un estudio clínico placebo controlado de manía aguda o tipo mixta, se dosificó a los pacientes para obtener una respuesta clínica con una concentración plasmática mínima entre 85 y 125 mg/mL. La dosis recomendada máxima es 60 mg/kg/día. No hay evidencia disponible de estudios controlados para dirigir al médico en el manejo a largo plazo de un paciente con un episodio de manía aguda que mejora con el uso de los comprimidos de divalproato de sodio de liberación prolongada. Sin embargo se está de acuerdo que generalmente el tratamiento farmacológico es deseable para obtener una respuesta rápida en manía, para el mantenimiento de la respuesta inicial y para la prevención de nuevos episodios de manía, no hay datos que apoyen los beneficios de los comprimidos de divalproato de sodio de liberación prolongada en el tratamiento a largo plazo (es decir, más allá de 3 semanas). Epilepsia: El Divalproato de Sodio está indicado como monoterapia y terapia adyuvante en crisis parciales complejas, y en crisis de ausencia simples y complejas en adultos y pacientes pediátricos de 10 años o más. Como la dosis de Divalproato de Sodio se titula en forma ascendente, las concentraciones de fenobarbital, carbamazepina, y/o fenitoína pueden ser afectadas (ver Interacciones). Crisis Parciales Complejas (CPC) para adultos y niños de diez años de edad o más: Monoterapia (Terapia inicial): El Divalproato de Sodio no se ha estudiado en forma sistemática como terapia inicial. Los pacientes deben iniciar la terapia a un rango de 10 a 15 mg/kg/día. La dosificación se debe incrementar en 5 a 10 mg/kg/semana para lograr una óptima respuesta clínica. Normalmente, la respuesta clínica óptima se alcanza con dosis diarias inferiores a 60 mg/kg/día. Si no se ha logrado una respuesta clínica satisfactoria, se deben medir niveles plasmáticos para determinar si se encuentran o no dentro del rango terapéutico generalmente aceptado (50 a 100 mcg/mL). No se pueden efectuar recomendaciones relacionadas con la seguridad de valproato al utilizarse a dosis superiores a 60 mg/kg/día. La probabilidad de trombocitopenia aumenta en forma significativa a concentraciones plasmáticas mínimas de valproato total superiores a 110 mcg/mL en mujeres y 135 mcg/mL en hombres. El beneficio de un mejor control de las crisis con dosis más altas debe ser contrapesado contra la posibilidad de una mayor incidencia de reacciones adversas. Conversión a Monoterapia: Los pacientes deben iniciar la terapia con 10 a 15 mg/kg/día. La dosificación se debe incrementar en 5 a 10 mg/kg/semana para lograr la óptima respuesta clínica. Normalmente, la respuesta clínica óptima se logra con dosis diarias inferiores a 60 mg/kg/día. Si no se ha logrado una respuesta clínica satisfactoria, se deben medir niveles plasmáticos para determinar si están o no en el rango terapéutico generalmente aceptado (50 a 100 mcg/mL). No se pueden efectuar recomendaciones relacionadas con la seguridad de valproato para su uso a dosis superiores a 60 mg/kg/día. Normalmente se puede reducir la dosificación de la droga antiepiléptica (AED) concomitante en aproximadamente un 25% cada dos semanas. Esta reducción se puede comenzar al inicio de la terapia con Divalproato de Sodio, o retardar en una a dos semanas si existe preocupación sobre el riesgo que se presenten crisis con una menor dosificación. La velocidad y duración de la discontinuación de la droga antiepiléptica concomitante puede presentar una amplia variación, y los pacientes se deben monitorear cercanamente durante este período por una mayor frecuencia de crisis. Terapia adyuvante: El Divalproato de Sodio se puede agregar al régimen del paciente a una dosificación de 10 a 15 mg/kg/día. La dosificación se puede incrementar en 5 a 10 mg/kg/semana hasta lograr una óptima respuesta clínica. Normalmente, la respuesta clínica óptima se logra a dosis diarias inferiores a 60 mg/kg/día. Si no se ha logrado la respuesta clínica óptima, se deberán medir niveles plasmáticos para determinar si están o no en el rango terapéutico generalmente aceptado (50 a 100 mcg/mL). No se pueden efectuar recomendaciones en relación a la seguridad de valproato para su uso en dosis superiores a 60 mg/kg/día. En un estudio de terapia adyuvante para crisis parciales complejas en el cual los pacientes estaban recibiendo ya sea carbamazepina o fenitoína en adición a Divalproato de Sodio, no se requirieron ajustes de dosificación de carbamazepina o fenitoína (ver Estudios Clínicos). Sin embargo, puesto que valproato puede interactuar con estas o con otras drogas antiepilépticas administradas concomitantemente así como con otras drogas (ver Interacciones), se recomienda realizar determinaciones periódicas de concentraciones plasmáticas de las drogas antiepilépticas concomitantes durante el curso temprano de la terapia (ver Interacciones). Crisis de ausencia simple y compleja para adultos y niños de 10 años o más: La dosis inicial recomendada es de 15 mg/kg/día, aumentando a intervalos de una semana en 5 a 10 mg/kg/día hasta que se controlen las crisis o los efectos adversos impidan los futuros incrementos. La dosis máxima recomendada es de 60 mg/kg/día. No se ha establecido una buena correlación entre la dosis diaria, las concentraciones séricas y el efecto terapéutico. Sin embargo, una concentración sérica terapéutica de valproato para la mayoría de los pacientes con crisis de ausencia se considera en un rango de 50 a 100 mcg/mL. Algunos pacientes pueden ser controlados con concentraciones séricas más bajas o más altas (ver Farmacología). Dado que la dosificación de valproato de sodio se titula en forma ascendente, se pueden afectar las concentraciones sanguíneas de fenobarbital y/o fenitoína (ver Precauciones). Las drogas antiepilépticas no se deben discontinuar en forma abrupta en pacientes en los cuales la droga se administra para prevenir crisis mayores debido a la fuerte posibilidad de precipitar status epilépticos con hipoxia concurrente y riesgo de vida. Profilaxis de Migraña: La dosis de inicio recomendada es de 500 mg una vez al día por una semana, después de eso aumentando a 1000 mg una vez al día. Aunque las dosis diarias de 1000 mg del Divalproato de Sodio de liberación prolongada no se han evaluado en los pacientes con migraña, el rango de dosis efectiva de Divalproato de Sodio comprimidos cubierta entérica en estos pacientes es de 500 a 1000 mg/día. Como con otros productos de valproato, las dosis de Divalproato de Sodio de liberación prolongada deben ser individualizadas y el ajuste de la dosis puede ser necesario. Los comprimidos de liberación prolongada no son bioequivalentes a los comprimidos de Divalproato de Sodio cubierta entérica (ver Farmacología - Farmacocinética). Si un paciente requiere ajustes más pequeños de la dosis que se dispone de Divalproato de Sodio de liberación prolongada, en su lugar se deben utilizar los comprimidos de Divalproato de Sodio con recubrimiento entérico. Conversión a Divalproato de Sodio ER: En pacientes adultos y pacientes pediátricos de 10 años o más con epilepsia que previamente reciben Divalproato de Sodio, el Divalproato de Sodio ER debe ser administrado una vez al día, a una dosis un 8 a 20% superior a la dosis diaria total de Divalproato de Sodio (ver Tabla 1). Para los pacientes, en los cuales la dosis diaria total de Divalproato de Sodio no se puede convertir directamente a Divalproato de Sodio ER, se debe dar instrucciones a los médicos para aumentar la dosis diaria total de Divalproato de Sodio a la dosis siguiente más alta antes de convertir a la dosis diaria total apropiada de Divalproato de Sodio ER. Hay datos insuficientes para permitir una recomendación del factor de conversión para los pacientes con dosis de Divalproato de Sodio sobre 3125 mg/día.
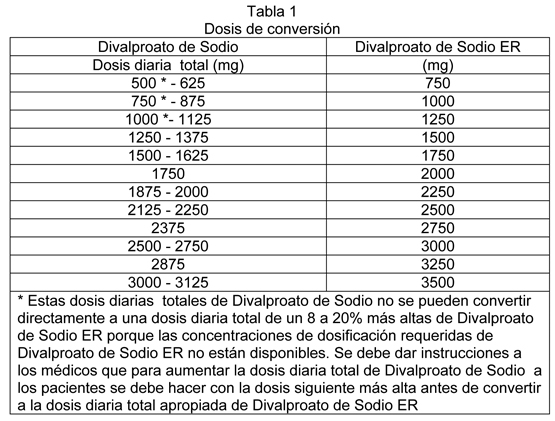
Las concentraciones plasmáticas Cmín de valproato para Divalproato de Sodio ER son equivalentes a Divalproato de Sodio, pero pueden variar a través de pacientes después de la conversión. Si la respuesta clínica satisfactoria no se ha alcanzado, se deben medir niveles plasmáticos para determinar si están o no en el rango terapéutico generalmente aceptado (50 a 100 mcg/mL). Recomendaciones Generales de Dosificación: Dosificación en pacientes ancianos: Debido a una disminución en el clearance del valproato no unido y posiblemente a una mayor sensibilidad a la somnolencia en ancianos, la dosis de inicio se debe reducir en estos pacientes. El comienzo de la dosificación con dosis más bajas de 250 mg sólo puede ser logrado con el uso de otras formulaciones de divalproato de sodio. Las dosis se deben incrementar lentamente y con un monitoreo regular de la ingesta de líquidos y alimentos, deshidratación, somnolencia y otros eventos adversos. Se debe considerar reducción de dosis o discontinuación del valproato en pacientes con una menor ingesta de alimentos o líquidos y en pacientes con excesiva somnolencia. La dosis terapéutica última se debe lograr tanto en base a la tolerancia como a la respuesta clínica (ver Advertencias). Eventos Adversos Dosis relacionados: La frecuencia de efectos adversos (especialmente elevación de las enzimas hepáticas y trombocitopenia) puede estar relacionada con la dosis. La probabilidad de trombocitopenia parece aumentar significativamente en concentraciones de valproato total de ≥110 mcg/mL (mujeres) o ≥135 mcg/mL (hombres) (ver Precauciones). El beneficio de un mejor efecto terapéutico con dosis más altas debe ser sopesado contra la posibilidad de una mayor incidencia de reacciones adversas. Irritación Gastrointestinal: Los pacientes que experimentan irritación GI se pueden beneficiar con la administración de la droga con las comidas o iniciar la terapia con dosis más bajas de Divalproato de Sodio con recubrimiento entérico. Adherencia: Los pacientes deben ser informados de tomar el Divalproato de Sodio de liberación prolongada cada día según lo prescrito. Si se salta una dosis se debe tomar cuanto antes, a menos que casi sea hora para la dosis siguiente. Si se salta una dosis, el paciente no debe doblar la dosis siguiente.
Contraindicaciones.
El Divalproato de Sodio no se debe administrar a pacientes con enfermedad hepática o disfunción hepática significativa. El Divalproato de Sodio está contraindicado en pacientes con hipersensibilidad conocida a la droga. El Divalproato de Sodio está contraindicado en pacientes con trastornos conocidos del ciclo de la urea (ver Advertencias).
Reacciones adversas.
Manía: La incidencia de eventos emergentes del tratamiento ha sido comprobada basado en datos combinados a partir de dos estudios clínicos de tres-semanas, placebo controlado con comprimidos de divalproato de sodio de liberación prolongada en el tratamiento de episodios de manía asociados a trastorno bipolar. La tabla 2 resume estos eventos adversos reportados por los pacientes en estos estudios donde la tasa de incidencia en el grupo tratado con comprimidos de divalproato de sodio de liberación prolongada fue mayor del 5% y mayor que la incidencia de placebo.
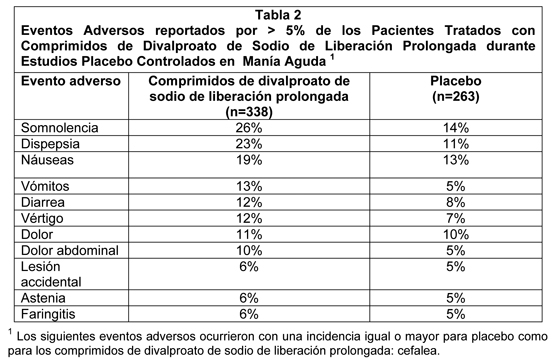
Los siguientes eventos adversos adicionales fueron reportados por más del 1% pero no más que el ≥5% de los pacientes tratados con divalproato de sodio de liberación prolongada comprimidos en estudios clínicos controlados: Cuerpo como un todo: Dolor de espalda, Síndrome Gripal, Infección, Infección por hongos. Sistema Cardiovascular: Hipertensión. Sistema Digestivo: Constipación, Boca seca, Flatulencia. Sistema hematológico y linfático: Equimosis. Trastornos metabólicos y nutricionales: Edema Periférico. Sistema Músculo-esquelético: Mialgia. Sistema Nervioso: Paso Anormal, Hipertonía, Temblor. Sistema Respiratorio: Rinitis. Piel y accesorios: Prurito, Rash. Sentidos Especiales: Conjuntivitis. Sistema Urogenital: Infección del Tracto Urinario, Vaginitis. Epilepsia: Crisis parciales complejas (CPC): Basado en un estudio placebo-controlado de terapia adyuvante para el tratamiento de crisis parciales complejas, el divalproato de sodio fue generalmente bien tolerado con la mayoría de los eventos
adversos graduados como leves a moderados en severidad. La intolerancia fue la razón primaria para la discontinuación del tratamiento (6%) en los pacientes con divalproato de sodio en comparación con 1% de los pacientes tratados con placebo. La Tabla 3 lista los eventos adversos emergentes del tratamiento que fueron reportados por 5% de los pacientes tratados con divalproato de sodio y para los cuales la incidencia fue superior a la observada en el grupo placebo, en el estudio clínico placebo-controlado de terapia adyuvante para el tratamiento de crisis parciales complejas. Puesto que los pacientes también fueron tratados con otras drogas antiepilépticas, no fue posible, en la mayoría de los casos, determinar si los siguientes eventos adversos pueden ser atribuidos a divalproato de sodio solo, o a la combinación de divalproato de sodio y otras drogas antiepilépticas.
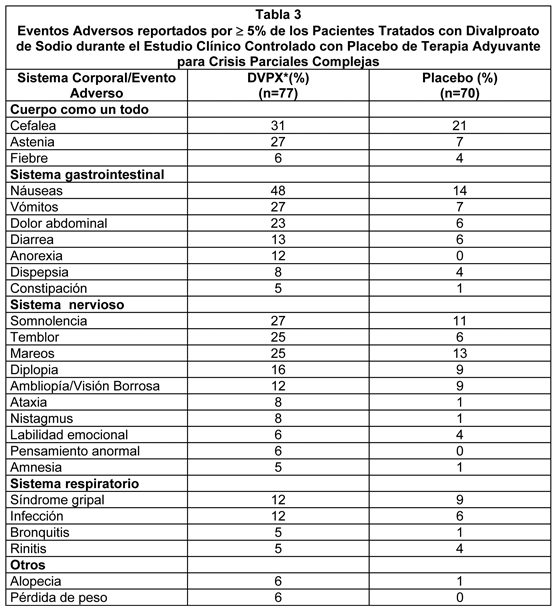
La Tabla 4 lista los eventos adversos emergentes del tratamiento que fueron reportados por 5% de los pacientes en el grupo de divalproato de sodio de dosis alta, y para los cuales la incidencia fue superior que en el grupo de dosis baja, en un estudio clínico controlado de monoterapia con divalproato de sodio en el tratamiento de crisis parciales complejas. Dado que los pacientes estaban siendo retirados de otras drogas antiepilépticas durante la primera parte del estudio, no es posible, en la mayoría de los casos, determinar si los siguientes eventos adversos pueden ser atribuidos al divalproato de sodio solo, o a la combinación de divalproato de sodio y otras drogas antiepilépticas.
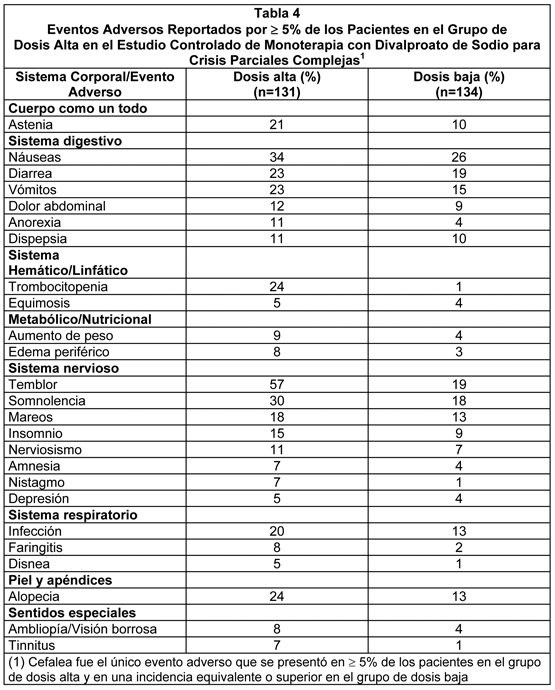
Los siguientes eventos adversos adicionales fueron reportados por más del 1% pero menos del 5% de los 358 pacientes tratados con divalproato de sodio en los estudios controlados de crisis parciales complejas: Cuerpo como un Todo: Lumbago, dolor de pecho, malestar. Sistema cardiovascular: Taquicardia, hipertensión, palpitaciones. Sistema digestivo: Aumento del apetito, flatulencia, hematemesis, eructos, pancreatitis, absceso periodontal. Sistema Hemático y Linfático: Petequias. Trastornos Metabólicos y Nutricionales: elevación de SGOT, elevación de SGPT. Sistema músculo-esquelético: Mialgia, espasmo muscular, artralgia, calambres en las piernas, miastenia. Sistema nervioso: Ansiedad, confusión, trastorno del habla, marcha anormal, parestesia, hipertonía, descoordinación, sueños anormales, trastorno de personalidad. Sistema respiratorio: Sinusitis, incremento en la tos, neumonía, epistaxis. Piel y Apéndices: rash, prurito, piel seca. Sentidos especiales: Perversión del gusto, visión anormal, trastorno del oído, sordera, otitis media. Sistema urogenital: Incontinencia urinaria, vaginitis, dismenorrea, amenorrea, frecuencia de la micción. Profilaxis de Migraña: Basado en los resultados de un estudio multicéntrico, randomizado, doble ciego, controlado con placebo, el divalproato de sodio ER fue bien tolerado en el tratamiento profiláctico de la cefalea tipo migraña. De los 122 pacientes expuestos a divalproato de sodio ER en un estudio controlado con placebo, el 8% discontinuaron por eventos adversos comparado con el 9% para los 115 pacientes con placebo. La Tabla 5 incluye aquellos eventos adversos reportados para los pacientes en el estudio controlado con placebo donde la tasa de incidencia del grupo tratado con divalproato de sodio ER fue mayor al 5% y superior que en los pacientes con placebo.
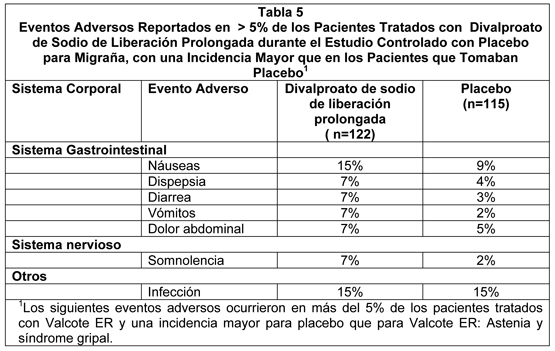
Los siguientes eventos adversos adicionales fueron reportados en más del 1% pero no más del 5% de los pacientes tratados con divalproato de sodio de liberación prolongada y con mayor incidencia que con placebo el estudio clínico controlado con placebo para profilaxis de migraña: Cuerpo como un todo: Lesión accidental, infección viral. Sistema digestivo: Aumento del apetito, trastornos dentales. Trastornos metabólicos y Nutricionales: Edema, ganancia de peso. Sistema nervioso: Marcha anormal, mareo, hipertonía, insomnio, nerviosismo, temblor, vértigo. Sistema respiratorio: Faringitis, Rinitis. Piel y apéndices: Rash. Sentidos especiales: Tinnitus. Basado en dos estudios clínicos controlados con placebo y su extensión a largo plazo, los comprimidos de divalproato de sodio con recubrimiento entérico fueron generalmente bien tolerados con la mayoría de los eventos adversos clasificados como leves a moderados en severidad. De los 202 pacientes expuestos a los comprimidos de divalproato de sodio con recubrimiento entérico en los estudios controlados con placebo, el 17% discontinuaron por intolerancia. Esto se compara a una tasa de 5% para los 81 pacientes con placebo. Incluyendo la extensión del estudio a largo plazo, los eventos adversos reportados como la razón primaria para la discontinuación en ≥1% de 248 pacientes tratados con divalproato de sodio con recubrimiento entérico fueron alopecia (6%), náuseas y/o vómitos (5%), aumento de peso (2%), temblor (2%), somnolencia (1%), SGOT y/o SGPT elevados (1%), y depresión (1%). La Tabla 6 incluye aquellos eventos adversos reportados para pacientes en estudios controlados con placebo donde la tasa de incidencia en el grupo tratado con divalproato de sodio con recubrimiento entérico fue mayor que 5% y fue mayor que en los pacientes tratados con placebo.
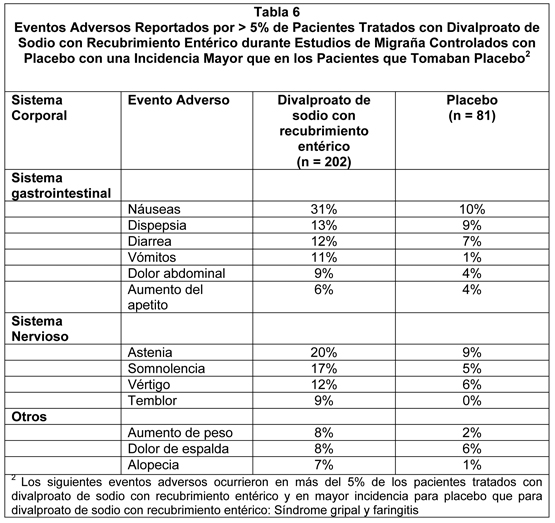
Los siguientes eventos adversos adicionales no referidos arriba fueron reportados por más del 1% pero no más del 5% de los pacientes tratados con divalproato de sodio con recubrimiento entérico y con una mayor incidencia que placebo en los estudios clínicos controlados con placebo: Cuerpo como un todo: Dolor en el pecho. Sistema cardiovascular: Vasodilatación. Sistema digestivo: Constipación, boca seca, flatulencia, estomatitis. Sistema Hemático y linfático: Equimosis. Trastornos Metabólicos y Nutricionales: Edema periférico. Sistema Músculo-esquelético: calambres en las piernas. Sistema nervioso: Sueños anormales, confusión, parestesia, trastornos del habla, pensamiento anormal. Sistema respiratorio: Disnea, sinusitis. Piel y apéndices: Prurito. Sistema urogenital: Metrorragia. Otras poblaciones de pacientes: Los siguientes eventos adversos no enumerados previamente fueron reportados por más del 1% de los pacientes tratados con divalproato de sodio con recubrimiento entérico y con una mayor incidencia que placebo en estudios controlados con placebo de epilepsia o de episodios maníacos asociados con trastorno bipolar: Cuerpo como un todo: Calofríos, calofríos y fiebre, aumento en el nivel de la droga, fiebre, cefalea, malestar, dolor de cuello, rigidez del cuello. Sistema Cardiovascular: Arritmia, hipertensión, hipotensión, palpitación, hipotensión postural. Sistema Digestivo: Anorexia, disfagia, eructos, incontinencia fecal, gastroenteritis, glositis, hemorragia de la encía, hematemesis, ulceración de la boca, absceso periodontal. Sistema Hemático y linfático: Anemia, Aumento en el tiempo de sangría, leucopenia, petequias. Trastornos Metabólicos y Nutricionales: Hipoproteinemia, aumento de SGOT, aumento de SGPT, pérdida de peso. Sistema Músculo-esquelético: Artralgia, artrosis, calambres. Sistema Nervioso: Agitación, amnesia, ataxia, reacción catatónica, depresión, diplopía, disartria, labilidad emocional, alucinaciones, hipokinesia, incoordinación, nistagmo, psicosis, aumento de reflejos, trastorno del sueño, diskinesia tardía. Sistema Respiratorio: Bronquitis, hipo, neumonia. Piel y apéndices: Lupus Eritematoso discoide, piel seca, eritema nodoso, furunculosis, rash máculo papular, seborrea, sudoración, rash. Sentidos Especiales: Ambliopía, conjuntivitis, sordera, ojos secos, trastornos del ojo, dolor del ojo, fotofobia, perversión del gusto. Sistema Urogenital: Cistitis, dismenorrea, disuria, trastorno menstrual, incontinencia urinaria, vaginitis. Los eventos adversos que se han reportado con todas las formas de dosificación de valproato en estudios de epilepsia, informes espontáneos, y otras fuentes son enumerados abajo por sistema corporal. Puesto que el divalproato de sodio se ha utilizado generalmente con otras drogas antiepilépticas en el tratamiento de la epilepsia, no es posible, en la mayoría de los casos, determinar si las reacciones adversas siguientes se pueden atribuir al divalproato de sodio solo, o la combinación de drogas. Gastrointestinal: Los efectos colaterales más comúnmente reportados al inicio de la terapia son náuseas, vómitos e indigestión. Estos efectos suelen ser transitorios y raramente requieren de la discontinuación de la terapia. Se ha reportado diarrea, calambres abdominales y constipación. También se ha reportado anorexia con alguna pérdida de peso y un incremento en el apetito con aumento de peso. En algunos pacientes, mucho de los cuales tienen trastornos gastrointestinales funcionales o anatómicos (incluyendo ileostomía o colostomía) con tiempos reducidos de transito GI, han reportado en la post-comercialización la aparición de los comprimidos en las deposiciones. Efectos sobre el SNC: Se han observado efectos sedantes en pacientes que reciben valproato solo, pero esto sucede con mayor frecuencia en los pacientes que reciben terapia combinada. La sedación generalmente remite con la reducción de otros medicamentos antiepilépticos. Temblor (puede ser dosis-relacionado), alucinaciones, ataxia, cefalea, nistagmo, diplopía, asterixis, "manchas ante los ojos", disartria, mareos, confusión, hiperestesia, vértigo, falta de coordinación y parkinsonismo han sido reportados con el uso de valproato. Casos raros de coma se han presentado en pacientes que reciben valproato solo o en conjunto con fenobarbital. En casos raros, se ha desarrollado encefalopatía con o sin fiebre poco después de la introducción de monoterapia con valproato sin evidencia de disfunción hepática o niveles inadecuadamente altos de valproato plasmático. Aunque se ha informado de recuperación después del retiro de la droga, han existido casos fatales en pacientes con encefalopatía hiperamonémica, particularmente en pacientes con trastornos del ciclo de la urea subyacentes (ver Advertencias - Trastornos del Ciclo de la Urea y Precauciones.) Numerosos reportes han indicado demencia reversible y pseudoatrofia reversible en asociación con la terapia con valproato. Dermatológicos: Caída transitoria del cabello, rash cutáneo, fotosensibilidad, prurito generalizado, eritema multiforme, y síndrome de Stevens-Johnson. Se han reportado casos raros de necrólisis epidérmica tóxica incluyendo un caso fatal de un lactante de seis meses de edad que recibió valproato y numerosos otros medicamentos concomitantes. Un caso adicional de necrosis epidérmica tóxica que resultó en muerte fue reportado en un paciente de 35 años de edad con SIDA que recibía numerosos medicamentos concomitantes y con una historia de múltiples reacciones cutáneas a drogas. Se han reportado reacciones cutáneas serias con la administración concomitante de lamotrigina y valproato (ver Interacciones). Psiquiátrico: Alteración emocional, depresión, psicosis, agresión, hiperactividad, hostilidad y deterioro del comportamiento. Músculo-esquelético: Debilidad: Se han recibido reportes de disminución de la masa ósea, llevando potencialmente a osteoporosis y osteopenia, durante la terapia a largo plazo con medicamentos anticonvulsivantes, incluyendo valproato. Algunos estudios han indicado que el suplemento de calcio y de vitamina D puede ser beneficioso para los pacientes que están en terapia crónica con valproato. Hematológico: Trombocitopenia e inhibición de la fase secundaria de la agregación plaquetaria se pueden reflejar en tiempos de sangrado alterados, petequias, moretones, formación de hematomas, epistaxis y hemorragia franca (ver Precauciones - General e Interacciones). Linfocitosis relativa, macrocitosis, hipofibrinogenemia, leucopenia, eosinofilia, anemia incluyendo macrocítica con o sin deficiencia de folato, supresión de la médula ósea, pancitopenia, anemia aplástica, agranulocitosis y porfiria intermitente aguda. Hepática: Elevaciones menores de transaminasas (ej. SGOT y SGPT) y LDH son frecuentes y parecen ser dosis-relacionadas. Ocasionalmente, los resultados de las pruebas de laboratorio también pueden incluir elevaciones en la bilirrubina sérica y cambios anormales en otros tests de función hepática. Estos resultados pueden reflejar hepatotoxicidad potencialmente seria (ver Advertencias). Endocrino: Menstruaciones irregulares, amenorrea secundaria, agrandamiento de las mamas, galactorrea, e inflamación de la glándula parótida. Test anormales de función tiroidea (ver Precauciones - General). Han existido raros reportes espontáneos de enfermedad de ovario poliquístico. No se ha establecido una relación de causa y efecto. Pancreático: Pancreatitis aguda incluyendo muerte (ver Advertencias). Metabólicas: Hiperamonemia (ver Precauciones), hiponatremia, y secreción inadecuada de ADH. Han existido raros reportes de síndrome de Fanconi presentándose primordialmente en niños. Se ha reportado menores concentraciones de carnitina aunque se desconoce su relevancia clínica. Se ha presentado hiperglicinemia y estuvo asociada con un resultado fatal en un paciente con hiperglicinemia preexistente no cetónica. Genitourinaria: Enuresis e infección del tracto urinario. Sentidos especiales: Se ha reportado pérdida de la audición, ya sea reversible o irreversible; sin embargo, no se ha establecido una relación de causa y efecto. También se ha reportado dolor de oídos. Otros: Reacción alérgica, anafilaxis, edema de las extremidades, lupus eritematoso, dolor óseo, aumento de la tos, neumonía, otitis media, bradicardia, vasculitis cutánea, fiebre e hipotermia.
Precauciones.
Disfunción hepática: Ver Contraindicaciones y Advertencias. Pancreatitis: Ver Advertencias. Hiperamonemia: Se ha reportado hiperamonemia en asociación con terapia con valproato y puede estar presente a pesar de pruebas de función hepática normales. En pacientes que desarrollan inexplicables episodios de letargo y vómitos o cambios en su estado mental, se debe considerar encefalopatía hiperamonémica y se debe medir el nivel de amonio. También se debe considerar hiperamonemia en pacientes que se presentan con hipotermia (ver Precauciones - Hipotermia). Si el amonio aumenta, la terapia de valproato se debe discontinuar. Deben ser iniciadas intervenciones apropiadas para el tratamiento de la hiperamonemia y tales pacientes someterse a investigación para trastornos del ciclo de la úrea subyacente (ver Contraindicaciones y Advertencias - Trastornos del Ciclo de la Urea y Precauciones - Hiperamonemia y Encefalopatía Asociada con el Uso Concomitante de Topiramato). Las elevaciones asintomáticas del amonio son más comunes y cuando se presentan requieren estrecho monitoreo de los niveles de amonio plasmáticos. Si la elevación persiste, se debe considerar la discontinuación de la terapia de valproato. Hiperamonemia y Encefalopatía Asociada al Uso Concomitante de Topiramato: La administración concomitante de topiramato y de ácido valproico se ha asociado con hiperamonemia con o sin encefalopatía en pacientes que han tolerado cualquiera de estas drogas por si solas. Los síntomas clínicos de encefalopatía hiperamonémica a menudo incluyen alteraciones agudas en el nivel de conciencia y/o función cognoscitiva con letargo o vómitos. La hipotermia también puede ser una manifestación de hiperamonemia (ver Precauciones - Hipotermia). En la mayoría de los casos, los síntomas y signos disminuyeron con la discontinuación de cualquiera de las drogas. Este evento adverso no es debido a una interacción farmacocinética. No se sabe si la monoterapia con topiramato se asocia con hiperamonemia. Pacientes con fallas innatas del metabolismo o reducción de la actividad mitocondrial hepática pueden estar en un riesgo mayor de hiperamonemia con o sin encefalopatía. Aunque no está estudiado, una interacción de topiramato y ácido valproico puede exacerbar defectos existentes o desenmascarar deficiencias en personas susceptibles (ver Contraindicaciones y Advertencias - Trastornos del Ciclo de la Urea y Precauciones - Hiperamonemia). Hipotermia: Hipotermia, definido como una caída no intencional en la temperatura del cuerpo a < 35°C (95°F), se ha reportado en asociación con la terapia con valproato tanto en conjunto con como en ausencia de hiperamonemia. Esta reacción adversa también puede ocurrir en pacientes que usan topiramato concomitante con valproato después del inicio del tratamiento con topiramato o después de aumentar la dosis diaria de topiramato (ver Interacciones - Topiramato). Se debe tener consideración para suprimir el valproato en pacientes que desarrollan hipotermia, el cual se puede manifestar por una variedad de anormalidades clínicas que incluyen letargia, confusión, coma y alteraciones significativas en otros sistemas de órganos importantes tales como los sistemas cardiovascular y respiratorio. El manejo y la evaluación clínica deben incluir examen de los niveles de amonio sanguíneo. General: Debido a reportes de trombocitopenia (ver Advertencias), inhibición de la fase secundaria de la agregación plaquetaria, y parámetros de coagulación anormal (por ejemplo, bajo fibrinógeno), se recomienda realizar recuentos de plaquetas, y pruebas de coagulación antes de iniciar la terapia y a intervalos periódicos durante la misma. Se recomienda que los pacientes que reciben divalproato de sodio sean monitoreados con recuento de plaquetas y parámetros de coagulación previa a cirugía electiva. En un estudio clínico de divalproato de sodio como monoterapia en pacientes con epilepsia, 34/126 pacientes (27%) que recibieron aproximadamente 50 mg/kg/día en promedio, presentaron al menos un valor de plaquetas ≤75 x 109/L. Aproximadamente la mitad de estos pacientes discontinuaron el tratamiento, con retorno de los recuentos de plaquetas a los valores normales. En los pacientes restantes, los recuentos de plaquetas se normalizaron mientras continuaban el tratamiento. En este estudio, la probabilidad de trombocitopenia pareció aumentar significativamente a concentraciones totales de valproato de ≥110 mcg/mL (mujeres) o ≥135 mcg/mL (hombres). La evidencia de hemorragia, equimosis o un trastorno de la hemostasis/coagulación es una indicación para reducción de la dosificación o discontinuación de la terapia. Dado que el divalproato de sodio puede interactuar con drogas administradas concomitantemente que son capaces de inducción enzimática, se recomienda la realización de determinaciones periódicas de concentración plasmática de valproato y de las drogas concomitantes durante el curso temprano de la terapia (ver Interacciones de drogas). El valproato se elimina parcialmente en la orina como un ceto-metabolito que puede llevar a una interpretación falsa del test de cetona urinaria. Han existido reportes de pruebas de función tiroidea alterada asociados con valproato. La significancia clínica de la misma es desconocida. Existen estudios in vitro que sugieren que el valproato estimula la replicación de los virus VIH y CMV bajo ciertas condiciones experimentales. La consecuencia clínica de esto, si es que existe alguna, es desconocida. Adicionalmente, la relevancia de estos hallazgos in vitro es incierta para los pacientes que están recibiendo terapia antiretroviral con máxima actividad supresora. A pesar de ello, estos datos se deben tener en mente al interpretar los resultados del monitoreo regular de la carga viral en pacientes VIH infectados que están recibiendo valproato o al realizar el seguimiento clínico de pacientes infectados por CMV. Reacción de Hipersensibilidad Multi-orgánica: Raramente se han reportado reacciones de hipersensibilidad multiorgánica en asociación temporal cercana después del inicio de la terapia con valproato en adultos y pacientes pediátricos (mediana de tiempo a la detección 21 días: rango 1 a 40). Aunque ha habido un número limitado de informes, muchos de estos casos produjeron hospitalización y se ha reportado al menos una muerte. Los signos y síntomas de este trastorno fueron diversos; sin embargo, los pacientes típicamente, aunque no exclusivamente, presentaron fiebre y rash asociado con compromiso de otro sistema, órgano. Otras manifestaciones asociadas pueden incluir linfoadenopatía, hepatitis, pruebas de función hepática alteradas, anormalidades hematológicas (ej., eosinofília, trombocitopenia, neutropenia), prurito, nefritis, oliguria, síndrome hepato renal, artralgia, y astenia. Debido a que el desorden es variable en su expresión, signos y síntomas de otros sistemas, órganos, no mencionados aquí, pueden ocurrir. Si se sospecha esta reacción, el valproato se debe discontinuar y comenzar un tratamiento alternativo. Aunque la existencia de sensibilidad cruzada con otras drogas que producen este síndrome no es clara, la experiencia entre las drogas asociadas con hipersensibilidad multi-orgánica indicaría ésta es una posibilidad. Información para los pacientes: Se debe informar a los pacientes y sus cuidadores que el dolor abdominal, náuseas, vómitos y/o anorexia pueden ser síntomas de pancreatitis, y que, por consiguiente, requieren de una pronta evaluación médica adicional. Los pacientes y sus cuidadores deben ser informados sobre los signos y síntomas asociados con la encefalopatía hiperamonémica (ver Precauciones - Hiperamonemia) y señalarles que deben informar al médico si cualquiera de estos síntomas aparece. Dado que los productos con valproato de sodio pueden producir depresión del SNC, especialmente cuando se combinan con otro depresor del SNC (por ejemplo, alcohol), se debe recomendar a los pacientes que no realicen actividades riesgosas, tales como conducir un automóvil u operar máquinas peligrosas, hasta que se demuestre que no sufren de somnolencia con la droga. Puesto que el divalproato de sodio se ha asociado con ciertos tipos de defectos de nacimiento, a las mujeres en edad fértil que estén considerando el uso de divalproato de sodio deben ser advertidas de los riesgos asociados al uso de divalproato de sodio durante el embarazo (ver Advertencias). Uso Pediátrico: La seguridad y efectividad del divalproato de sodio comprimidos de liberación prolongada para la profilaxis de cefalea tipo migraña no se ha establecido en pacientes menores de 18 años. La seguridad y efectividad de los comprimidos de divalproato de sodio de liberación prolongada para el tratamiento de crisis parciales complejas, crisis de ausencia simple y compleja y múltiples tipos de crisis que incluyen crisis de ausencia, no se han establecido en pacientes pediátricos bajo los diez años de edad. La experiencia ha indicado que los niños menores de dos años presentan un considerable mayor riesgo de desarrollar hepatotoxicidad fatal, especialmente aquellos con las condiciones antes mencionadas (ver Advertencias). Por encima de los 2 años de edad, la experiencia en epilepsia ha indicado que la incidencia de hepatotoxicidad fatal se reduce considerablemente en grupos de pacientes progresivamente mayores. La toxicología básica y manifestaciones patológicas del divalproato de sodio en ratas recién nacidas (4 días de edad) y jóvenes (14 días de edad) son similares a aquellas observadas en ratas adultas jóvenes. Sin embargo, se han reportado hallazgos adicionales, incluyendo alteraciones renales en ratas jóvenes y alteraciones renales y displasia retinal en ratas recién nacidas. Estos hallazgos se presentaron a 240 mg/kg/día, una dosis que es aproximadamente equivalente a la dosis diaria máxima recomendada en seres humanos en una base mg/m2. No se observaron con 90 mg/kg, o 40% de la dosis diaria máxima en seres humanos en una base de mg/m2. Uso Geriátrico: La seguridad y efectividad del divalproato de sodio ER en la profilaxis de migraña en pacientes mayores de 65 años no se ha establecido. No se han reclutado pacientes mayores de 65 años en estudios clínicos prospectivos, doble ciego sobre manía asociada con enfermedad bipolar usando comprimidos de divalproato de sodio de liberación prolongada. En un estudio de revisión de casos de 583 pacientes, 72 pacientes (12%) fueron mayores de 65 años. Un porcentaje más alto de pacientes mayores de 65 años de edad reportó lesión accidental, infección, dolor, somnolencia y temblor. La discontinuación de valproato ocasionalmente se asoció con estos últimos dos eventos. No está claro si estos eventos indican un riesgo adicional o si resultan de enfermedades médicas preexistentes y el uso de medicamentos concomitantes entre estos pacientes. Un estudio de pacientes ancianos con demencia reveló somnolencia relacionada con la droga y discontinuación debido a somnolencia (ver Advertencias - Somnolencia en Ancianos). En estos pacientes se debe reducir la dosis de inicio, y se debe considerar reducción de la dosificación o discontinuación en pacientes con somnolencia excesiva (ver Dosificación).
Advertencias.
Hepatotoxicidad: Se ha presentado insuficiencia hepática con desenlace fatal en pacientes que han recibido ácido valproico. Estos incidentes generalmente se presentaron durante los primeros seis meses de tratamiento. La hepatotoxicidad seria o fatal puede estar precedida de síntomas inespecíficos tales como malestar, debilidad, letargo, edema facial, anorexia y vómitos. En pacientes con epilepsia, también se puede presentar una pérdida del control sobre las crisis. Los pacientes se deben monitorear de cerca por la aparición de estos síntomas. Las pruebas de función hepática se deben realizar antes de la terapia y durante intervalos frecuentes a continuación, especialmente durante los primeros seis meses. Sin embargo, los médicos no deben confiar únicamente en la bioquímica plasmática dado que estas pruebas pueden no ser anormales en todos los casos, sino que también deben considerar los resultados de una cuidadosa historia clínica y el examen físico. Se debe tener precaución al administrar productos con valproato de sodio a pacientes con una historia de enfermedad hepática previa. Los pacientes que reciben múltiples anticonvulsivantes, los niños, aquellos con trastornos metabólicos congénitos, con trastornos convulsivos severos acompañados por retardo mental y aquellos con enfermedad cerebral orgánica pueden estar en un riesgo especial. La experiencia ha indicado que los niños menores de dos años están en un riesgo considerablemente mayor de desarrollar hepatotoxicidad fatal, especialmente aquellos con las condiciones antes mencionadas. Cuando se usa Divalproato de Sodio en este grupo de pacientes, esto se debe hacer con extrema precaución y como agente único. Se deberán sopesar los beneficios de la terapia contra los posibles riesgos. Más allá de este grupo etario, la experiencia en epilepsia ha indicado que la incidencia de hepatotoxicidad fatal se reduce considerablemente en los grupos de pacientes progresivamente mayores. No se recomienda el uso de Divalproato de Sodio de liberación prolongada en niños para la profilaxis del dolor de cabeza tipo migraña (ver Precauciones - Uso en Pediatría). La droga se debe discontinuar inmediatamente en presencia de disfunción hepática significativa, sospechada o aparente. En algunos casos, la disfunción hepática ha progresado a pesar de la discontinuación de la droga. Pancreatitis: Se han reportado casos de pancreatitis con riesgo vital tanto en niños como en adultos que recibieron valproato. Algunos de los casos se han descrito como hemorrágicos con progresión rápida desde los síntomas iniciales a la muerte. Algunos casos se han presentado poco después del uso inicial, mientras que otros después de muchos años de uso. La tasa basada en los casos reportados excede lo esperado para la población general y han existido casos en los cuales la pancreatitis recurrió después de un nuevo tratamiento con valproato. En estudios clínicos, se han descrito dos casos de pancreatitis sin etiología alternativa en 2416 pacientes, representando 1044 pacientes-años de experiencia. Se debe alertar a los pacientes y sus cuidadores que el dolor abdominal, náuseas, vómitos y/o anorexia pueden ser síntomas de pancreatitis que requieren de rápida evaluación médica. Si se diagnostica pancreatitis, normalmente se debe discontinuar el valproato. El tratamiento alternativo para la condición médica subyacente se debe iniciar según indicación clínica (ver Advertencias). Trastornos del Ciclo de la Urea (TCU): La encefalopatía hiperamonémica, algunas veces fatal, se ha reportado después de la iniciación de la terapia con valproato en pacientes con trastornos del ciclo de la urea, un grupo de anormalidades genéticas poco comunes, particularmente deficiencia de la ornitina transcarbamilasa. Previo a la iniciación de la terapia con valproato, se debe considerar una evaluación de TCU en los siguientes pacientes: 1) aquellos con una historia de coma o encefalopatía inexplicable, encefalopatía asociada con carga proteica, encefalopatía relacionada con el embarazo o post parto, retraso mental inexplicable o historia de glutamina o amonio plasmático elevado; 2) aquellos con letargo y vómitos cíclicos, episodios de irritabilidad extrema, ataxia, BUN bajo, que evitan las proteínas; 3) aquellos con una historia familiar de TCU o una historia familiar de muertes de niños inexplicables (particularmente hombres); 4) aquellos con otros signos o síntomas de TCU. Pacientes que desarrollan síntomas de encefalopatía hiperamonémica inexplicable mientras reciben terapia con valproato deben recibir tratamiento rápido (incluyendo discontinuación de la terapia con valproato) y ser evaluado por trastornos del ciclo de la urea subyacente (ver Contraindicaciones y Precauciones). Conducta e Ideación Suicida: Se ha reportado un aumento en el riesgo de pensamientos o conducta suicida en pacientes que toman drogas antiepilépticas (AEDs) para cualquier indicación. El aumento del riesgo de pensamientos o conducta suicida con AEDs se observó tan temprano como una semana después del inicio del tratamiento con AEDs y persistió por la duración del tratamiento evaluado. El riesgo relativo para pensamientos o conducta suicida fue mayor en estudios clínicos para epilepsia que en estudios clínicos para psiquiátricos u otras condiciones, pero las diferencias de riesgo absoluto fueron similares para las indicaciones de epilepsia y psiquiátricas. Los pacientes tratados con un AED por cualquier indicación se deben monitorear para la emergencia o empeoramiento de depresión, pensamientos o conducta suicida, y/o cualquier cambio inusual en el ánimo o conducta. Cualquiera que considere prescribir divalproato de sodio o cualquier otro AED debe balancear el riesgo de pensamientos o conducta suicida con el riesgo de no tratar la enfermedad. La epilepsia y muchas otras enfermedades para las cuales se prescriben AED, están ellas mismas asociadas con morbilidad y un aumento del riesgo de pensamientos o conducta suicida. Si durante el tratamiento emergen pensamientos y conductas suicidas, el prescriptor necesita considerar si la emergencia de estos síntomas en cualquier paciente se puede relacionar a la enfermedad que está siendo tratada. Se debe informar a los pacientes, sus cuidadores y familiares que los AEDs aumentan el riesgo pensamientos y conducta suicida, y deben ser aconsejados sobre la necesidad de estar alertas a la emergencia o empeoramiento de signos y síntomas de depresión, cualquier cambio inusual en el ánimo o conducta, o la emergencia de pensamientos, conducta suicidas, o pensamiento acerca de autoagresión. Conductas de preocupación se deben reportar inmediatamente al personal de salud. Interacción con Antibióticos Carbapenem: Los antibióticos carbapenem (ertapenem, imipenem, meropenem) pueden reducir las concentraciones séricas de ácido valproico a niveles sub-terapéuticos, produciendo pérdida del control de las convulsiones. Las concentraciones séricas de ácido valproico se deben monitorear frecuentemente después del inicio de la terapia con carbapenem. Se deben considerar terapias anticonvulsivantes o antibacterianas alternativas si las concentraciones de ácido valproico caen significativamente o se deteriora el control de las convulsiones (ver Interacciones). Somnolencia en Ancianos: En un estudio multicéntrico, doble ciego de valproato en pacientes ancianos con demencia (edad media = 83 años), las dosis se incrementaron en 125 mg/día a una dosis objetivo de 20 mg/kg/día. Una proporción significativamente mayor de pacientes con valproato presentó somnolencia en comparación con placebo, y aunque no fue estadísticamente significativa, se observó una mayor proporción de pacientes con deshidratación. Las discontinuaciones por somnolencia también fueron significativamente superiores a las observadas con placebo. En algunos pacientes con somnolencia (aproximadamente la mitad), se asoció con una menor ingesta alimenticia y pérdida de peso. Existió una tendencia entre los pacientes que experimentaron estos eventos a presentar una menor concentración basal de albúmina, menor clearance de valproato y un BUN más alto. En los pacientes mayores, la dosificación se debe incrementar más lentamente y con monitoreo regular de la ingesta de líquidos y alimentos, deshidratación, somnolencia y otros eventos adversos. Se debe considerar reducciones de la dosis o discontinuación de valproato en pacientes con una menor ingesta de alimentos o líquidos y en pacientes con excesiva somnolencia (ver Dosificación). Trombocitopenia: La frecuencia de efectos adversos (especialmente niveles elevados de enzimas hepáticas y trombocitopenia (ver Precauciones), puede ser dosis-relacionada. En un estudio clínico de Divalproato de Sodio como monoterapia en pacientes con epilepsia, 34/126 pacientes (27%) que recibieron aproximadamente 50 mg/kg/día en promedio, presentaron al menos un valor de plaquetas ≤ 75 x 109/L. Aproximadamente la mitad de estos pacientes discontinuaron el tratamiento, retornando el recuento de plaquetas a niveles normales. En los pacientes restantes, el recuento de plaquetas se normalizó mientras se continuaba el tratamiento. En este estudio, la probabilidad de trombocitopenia pareció aumentar significativamente en concentraciones totales de valproato de ≥ 110 mcg/mL (mujeres) o ≥ 135 mcg/mL (hombres). El beneficio terapéutico que puede acompañar a las dosis más altas debe por tanto ser sopesado contra la posibilidad de una mayor incidencia de efectos adversos. Uso en Embarazo: De acuerdo a los informes publicados y no publicados, el ácido valproico puede producir efectos teratogénicos, tales como defectos del tubo neural (por ejemplo, espina bífida) en los recién nacidos de mujeres que reciben la droga durante el embarazo. Hay datos que sugieren un aumento en la incidencia de malformaciones congénitas asociadas al uso del ácido valproico durante el embarazo en comparación con algunas otras drogas antiepilépticas. Por lo tanto, el ácido valproico se debe considerar para las mujeres en edad fértil solo después de haber discutido los riesgos a fondo con la paciente y pesado contra los beneficios potenciales del tratamiento. Los datos descritos abajo fueron obtenidos casi exclusivamente de mujeres quienes recibieron valproato para tratar epilepsia. Existen múltiples reportes en la literatura clínica que indican que el uso de drogas antiepilépticas durante el embarazo resulta en una mayor incidencia de defectos de nacimiento en los recién nacidos. Por lo tanto, las drogas antiepilépticas se deben administrar a mujeres en edad fértil sólo si han demostrado ser esenciales para el manejo de su enfermedad. Los datos descritos abajo fueron obtenidos casi exclusivamente de mujeres que recibieron valproato para tratar la epilepsia La incidencia de defectos del tubo neural en el feto puede verse aumentada en mujeres que reciben valproato durante el primer trimestre del embarazo. El Centro para Control de Enfermedades de los Estados Unidos (CDC) ha estimado que el riesgo de las mujeres expuestas a ácido valproico de tener hijos con espina bífida es de aproximadamente 1 a 2%. Se han reportado otras anomalías congénitas (por ejemplo, defectos craneofaciales, malformaciones cardiovasculares y anomalías que comprometen diferentes sistemas corporales), compatibles e incompatibles con la vida. No se dispone de datos suficientes para determinar la incidencia de estas anomalías congénitas. La mayor incidencia de anomalías congénitas en mujeres tratadas con drogas antiepilépticas con trastornos convulsivos no puede considerarse como una relación de causa y efecto. Existen problemas metodológicos intrínsecos para la obtención de datos adecuados sobre la teratogenicidad de drogas en seres humanos; los factores genéticos o la condición epiléptica en si misma, pueden ser más importantes que la terapia farmacológica en la contribución a las anomalías congénitas. Ha habido informes de retraso en el desarrollo, autismo y/o trastornos del espectro del autismo en los recién nacidos de mujeres que han estado expuestas al ácido valproico durante el embarazo. Las pacientes que reciben valproato pueden desarrollar alteraciones de la coagulación. Una paciente que presentaba bajos niveles de fibrinógeno mientras recibía múltiples anticonvulsivantes incluyendo valproato dio luz a un lactante con afibrinogenemia quien posteriormente falleció de hemorragia. Si se utiliza valproato durante el embarazo, se deben monitorear cuidadosamente los parámetros de coagulación. Se ha reportado insuficiencia hepática, resultando en la muerte de un recién nacido y de un lactante, a continuación del uso de valproato durante el embarazo. Se deben considerar exámenes para detector defectos del tubo neural y otros usando procedimientos actualmente aceptados, como parte de la rutina pre-natal en mujeres embarazadas que reciben valproato. Las drogas antiepilépticas no se deben discontinuar abruptamente en pacientes en quienes la droga se administra para prevenir convulsiones mayores debido a la fuerte posibilidad de precipitar un status epiléptico con hipoxia asociada y riesgo de vida. En casos individuales donde la severidad y frecuencia del trastorno convulsivo son tales que la remoción de la dosis del medicamento no lo expone a un riesgo serio para el paciente, la discontinuación de la droga se puede considerar previo a y durante el embarazo, aunque no se puede decir con confianza que aún convulsiones menores no lo expone a algún riesgo para el desarrollo del embrión o feto. Los estudios en animales han demostrado teratogenicidad inducida por valproato. Se ha observado un incremento en la frecuencia de malformaciones, así como también retardo del crecimiento intrauterino y muerte en ratones, ratas, conejos y monos a continuación de la exposición prenatal al valproato. Las malformaciones del sistema esquelético son las anormalidades estructurales más comúnmente observadas en los animales de experimentación, aunque se han observado defectos de cierre del tubo neural en ratones expuestos a concentraciones plasmáticas maternas de valproato que excedieron de 230 mcg/mL (2.3 veces el límite superior del rango terapéutico para la epilepsia en humanos) durante períodos susceptibles del desarrollo embrionario. La administración de una dosis oral de 200 mg/kg/día o más (50% de la dosis diaria humana máxima o más en una base de mg/m2) a ratas preñadas durante organogénesis produjo malformaciones (esqueléticas, cardíacas y urogenitales) y retardo del crecimiento en las crías. Estas dosis resultaron en niveles plasmáticos máximos maternos de valproato de aproximadamente 340 m
cg/mL o más (3.4 veces el límite superior del rango terapéutico para la epilepsia en humanos o más). Se han reportado déficit conductuales en las crías de ratas que recibieron una dosis de 200 mg/kg/día a través de gran parte del embarazo. Una dosis oral de 350 mg/kg/día (aproximadamente el doble de la dosis diaria humana máxima en una base de mg/m2) produjo malformaciones esqueléticas y viscerales en conejos expuestos durante organogénesis. Las malformaciones esqueléticas, retardo del crecimiento y muerte se observaron en monos rhesus a continuación de la administración de una dosis oral de 200 mg/kg/día (igual a la dosis diaria humana máxima en una base de mg/m2) durante organogénesis. Esta dosis resultó en niveles plasmáticos maternos máximos de valproato de aproximadamente 280 mcg/mL (2.8 veces el límite superior del rango terapéutico para la epilepsia en seres humanos).
Interacciones.
Efectos de las Drogas Co-administradas sobre el Clearance de Valproato: Las drogas que afectan el nivel de expresión de las enzimas hepáticas, especialmente aquellas que elevan los niveles de glucuronosiltransferasas, pueden incrementar el clearance de valproato. Por ejemplo, fenitoína, carbamazepina, y fenobarbital (o primidona) pueden duplicar el clearance de valproato. Por ello, los pacientes bajo monoterapia generalmente presentarán vidas medias más prolongadas y concentraciones más altas que los pacientes que están recibiendo politerapia con drogas antiepilépticas. Por el contrario, se puede esperar que drogas que son inhibidoras de las isoenzimas del citocromo P450, por ejemplo, antidepresivos, ejerzan poco efecto sobre el clearance de valproato dado que la oxidación del citocromo P450 mediada microsomalmente es una vía metabólica secundaria relativamente menor en comparación con la glucuronidación y la beta-oxidación. Debido a estos cambios en el clearance de valproato, se debe incrementar el monitoreo de las concentraciones de valproato y de las drogas concomitantes cada vez que se introducen o discontinúan drogas inductoras de las enzimas. El siguiente listado entrega información acerca de la influencia potencial sobre la farmacocinética de valproato de numerosos fármacos de prescripción frecuente. La lista no es exhaustiva, y no puede serlo, dado que continuamente se reportan nuevas interacciones. Aspirina - Un estudio que involucró la administración conjunta de aspirina a dosis antipiréticas (11 a 16 mg/kg) con valproato a pacientes pediátricos (n = 6) reveló una reducción en la unión a proteínas y una inhibición del metabolismo de valproato. La fracción libre del valproato se incrementó en cuatro veces en presencia de aspirina en comparación a lo observado para valproato solo. La vía de b-oxidación consistente de 2-E-ácido valproico, 3-OH-ácido valproico, y 3-ceto ácido valproico se redujo desde un 25% de metabolitos totales excretados con valproato solo a 8.3% en presencia de aspirina. El divalproato de sodio ER no está indicado para uso en niños (ver Precauciones - Pediatría). Si la interacción observada en este estudio aplica o no a adultos se desconoce, pero se debe tener precaución si se co-administran valproato y aspirina. Antibióticos Carbapenem - Se ha reportado una reducción clínicamente significativa en la concentración sérica de ácido valproico en pacientes que reciben antibióticos carbapenem (ertapenem, imipenem, meropenem) y pueden producir pérdida del control de las convulsiones. El mecanismo de esta interacción no está bien entendido. Las concentraciones séricas de ácido valproico se deben monitorear frecuentemente después del inicio de la terapia con carbapenem. Se deben considerar terapias anticonvulsivantes o antibacterianas alternativas si las concentraciones séricas de ácido valproico caen significativamente o se deteriora el control de las convulsiones (ver Advertencias). Felbamato - Un estudio que involucró la administración conjunta de 1200 mg/día de felbamato con valproato a pacientes con epilepsia (n =10) reveló un incremento en las concentraciones máxima medias de valproato en un 35% (de 86 a 115 mcg/mL) comparado con valproato solo. El incremento de la dosis de felbamato a 2400 mg/día elevó las concentraciones máximas medias de valproato a 133 mcg/mL (incremento adicional de 16%). Una reducción en la dosificación de valproato puede ser necesaria cuando se inicie la terapia con felbamato. Rifampicina - Un estudio que involucró la administración de una dosis única de valproato (7 mg/kg), 36 horas después de cinco noches de dosificación diaria con rifampicina (600 mg) reveló un aumento del 40% en el clearance oral de valproato. Puede ser necesario un ajuste en la dosificación de valproato cuando se administra en forma conjunta con rifampicina. Drogas para las Cuales no se ha Observado una Interacción o ésta Probablemente No Sea Clínicamente Importante: Antiácidos - Un estudio que involucró la administración conjunta de 500 mg de valproato con antiácidos de prescripción frecuente (Maalox, Trisogel y Titralac - dosis 160 mEq) no reveló ningún efecto sobre el nivel de absorción de valproato. Clorpromazina - Un estudio que involucró la administración de 100 a 300 mg/día de clorpromazina a pacientes esquizofrénicos que ya estaban recibiendo valproato (200 mg dos veces al día) reveló un incremento de 15% en los niveles plasmáticos mínimos de valproato. Haloperidol - Un estudio que involucró la administración de 6 a 10 mg/día de haloperidol a pacientes esquizofrénicos que ya estaban recibiendo valproato (200 mg dos veces al día) no reveló cambios significativos en los niveles plasmáticos mínimos de valproato. Cimetidina y Ranitidina - Cimetidina y ranitidina no afectan el clearance de valproato. Efectos del Valproato sobre otras Drogas: Valproato ha demostrado ser un inhibidor débil de algunas isoenzimas P450, epóxido de hidrasa y glucuroniltransferasas. El siguiente listado entrega información sobre la potencial influencia de la co-administración de valproato sobre las farmacocinéticas o farmacodinamias de numerosos medicamentos de prescripción frecuente. La lista no es exhaustiva, dado que continuamente se están reportando nuevas interacciones. Drogas para las Cuales se ha Observado una Interacción Potencialmente Importante de Valproato: Amitriptilina/Nortriptilina - La administración de una dosis oral única de 50 mg de amitriptilina a 15 voluntarios normales (10 hombres y cinco mujeres) que recibieron valproato (500 mg dos veces al día) resultó en una reducción de 21% en el clearance plasmático de amitriptilina y un descenso de 34% en el clearance neto de nortriptilina. Se han recibido raros reportes post-comercialización del uso concomitante de valproato y amitriptilina resultando en un incremento en el nivel de amitriptilina. El uso concomitante de valproato y amitriptilina raramente ha estado asociado con toxicidad. Se debe considerar el monitoreo de los niveles de amitriptilina para los pacientes que reciben valproato concomitantemente con amitriptilina. Se debe considerar reducir la dosis de Amitriptilina/Nortriptilina en presencia de valproato. Carbamazepina/carbamazepina-10,11-Epóxido - Los niveles séricos de carbamazepina (CBZ) se redujeron en un 17%, mientras que los de carbamazepina-10,11-epóxido (CBZ-E) aumentaron en un 45% bajo administración conjunta de valproato y CBZ en pacientes epilépticos. Clonazepam - El uso concomitante del ácido valproico y clonazepam puede inducir status de ausencia en pacientes con una historia de trastornos convulsivos tipo ausencia. Diazepam - El valproato desplaza a diazepam desde sus sitios de unión a la albúmina plasmática e inhibe su metabolismo. La administración conjunta de valproato (1500 mg/día) incrementó la fracción libre de diazepam (10 mg) en un 90% en voluntarios sanos (n =6). El clearance plasmático y el volumen de distribución del diazepam libre se redujeron en un 25% y 20%, respectivamente, en presencia de valproato. La vida media de eliminación de diazepam permaneció inalterada con la adición de valproato. Etosuximida - El valproato inhibe el metabolismo de etosuximida. La administración de una dosis única de 500 mg de etosuximida con valproato (800 a 1600 mg/día) a voluntarios sanos (n =6) estuvo acompañada por un incremento de 25% en la vida media de eliminación de etosuximida y una reducción del 15% en su clearence total en comparación con etosuximida sola. Los pacientes que recibieron valproato y etosuximida, especialmente en conjunto con otros anticonvulsivantes, deben ser monitoreados por alteraciones en las concentraciones séricas de ambas drogas. Lamotrigina - En un estudio estado estable que involucró a 10 voluntarios sanos, la vida media de eliminación de lamotrigina aumentó desde 26 a 70 horas con la co-administración de valproato (un incremento de 165%). La dosis de lamotrigina se debe reducir al ser co-administrada con valproato. Se han reportado serias reacciones cutáneas (como síndrome de Stevens-Johnson y necrólisis tóxica epidérmica) con la administración concomitante de lamotrigina y valproato. Ver en el inserto del envase de lamotrigina los detalles de la dosis de lamotrigina en la administración concomitante con valproato. Fenobarbital - Se encontró que valproato inhibe el metabolismo de fenobarbital. La administración conjunta de valproato (250 mg dos veces al día durante 14 días) con fenobarbital a sujetos sanos (n =6) resultó en un incremento de 50% en la vida media y una reducción del 30% en el clearance plasmático de fenobarbital (dosis única de 60 mg). La fracción de la dosis de fenobarbital excretada inalterada se incrementó en un 50% en presencia de valproato. Existe evidencia de depresión severa de SNC, con o sin elevaciones significativas de las concentraciones séricas de barbiturato o valproato. Todos los pacientes que reciben terapia concomitante con barbiturato deben ser monitoreados de cerca por toxicidad neurológica. Se deben obtener, si es posible, concentraciones séricas de barbiturato, y reducir la dosificación del barbiturato, si corresponde. Primidona - La primidona es metabolizada a un barbiturato y por tanto, también puede estar involucrada en una interacción similar con valproato como la indicada para fenobarbital. Fenitoína - Valproato desplaza la fenitoína de sus sitios de unión en la albúmina plasmática e inhibe su metabolismo hepático. La administración conjunta de valproato (400 mg tres veces al día) con fenitoína (250 mg) en voluntarios normales (n =7) se asoció con un incremento del 60% en la fracción libre de fenitoína. El clearance plasmático total y el volumen de distribución aparente de fenitoína aumentaron en un 30% en presencia de valproato. En pacientes con epilepsia, han existido reportes de crisis inesperadas con la combinación de valproato y fenitoína. La dosificación de fenitoína debe ser ajustada según corresponda a la situación clínica. Tolbutamida - A partir de experimentos in vitro, la fracción libre de tolbutamida se incrementó desde un 20% a un 50% cuando se agregó a muestras plasmáticas tomadas de pacientes tratados con valproato. La relevancia clínica de este desplazamiento es desconocida. Topiramato - La administración concomitante de ácido valproico y topiramato se ha asociado con hiperamonemia con y sin encefalopatía (ver Contraindicaciones y Advertencias - Trastornos del Ciclo De la Urea y Precauciones - Hiperamonemia e - Hiperamonemia y Encefalopatía asociada al Uso Concomitante de Topiramato). La administración concomitante de topiramato con ácido valproico se ha asociado con hipotermia en pacientes que han tolerado cualquier droga sola. Se deben medir los niveles de amonio sanguíneos en pacientes que reporten inicio de hipotermia (ver Precauciones - Hipotermia y Precauciones - Hiperamonemia). Warfarina - En un estudio in vitro, valproato aumentó la fracción libre de warfarina hasta un 32.6%. Se desconoce la relevancia terapéutica de esta situación; sin embargo, se deben monitorear los tests de coagulación si se instituye terapia con divalproato de sodio en pacientes que están recibiendo anticoagulantes. Zidovudina - En seis pacientes que eran seropositivos para VIH, el clearence de zidovudina (100 mg cada ocho horas) se redujo en un 38% a continuación de la administración de valproato (250 ó 500 mg cada ocho horas); la vida media de zidovudina no se vio afectada. Drogas con las Cuales No se ha Observado una Interacción o ésta Probablemente No Presenta Importancia Clínica: Acetaminofeno - El valproato no tuvo efecto sobre ninguno de los parámetros farmacocinéticos de acetaminofeno cuando éste se administró en forma conjunta a tres pacientes epilépticos. Clozapina - En pacientes psicóticos (n =11), no se observó interacción alguna cuando valproato se administró en forma conjunta con Clozapina. Litio - La co-administración de valproato (500 mg dos veces al día) y carbonato de litio (300 mg tres veces al día) a voluntarios masculinos sanos (n =16) no tuvo efecto sobre la cinética de estado estable del litio. Lorazepam - La administración concomitante de valproato (500 mg dos veces al día) y lorazepam (1 mg dos veces al día) en voluntarios masculinos sanos (n =9) estuvo acompañada por una reducción de 17% en el clearance plasmático de lorazepam. Anticonceptivos orales esteroidales - La administración de una sola dosis de etinilestradiol (50 mcg)/levonorgestrel (250 mcg) a seis mujeres bajo terapia con valproato (200 mg dos veces al día) durante dos meses no reveló ninguna interacción farmacocinética. Embarazo y lactancia: Embarazo: Ver Advertencias. Madres en lactancia: El valproato se excreta en la leche materna. Se ha reportado que las concentraciones en la leche materna alcanzan entre el 1 y el 10% de las concentraciones séricas. Se desconoce el efecto que esta situación pudiese tener en un lactante. Se debe considerar la discontinuación de la lactancia cuando se administra divalproato de sodio a una mujer que amamanta.
Conservación.
Se recomienda que el Divalproato de Sodio comprimidos de liberación prolongada sea almacenado a temperatura ambiente entre los 20 a 25°C (68 a 77°F).
Sobredosificación.
La sobredosificación con valproato puede resultar en somnolencia, bloqueo cardíaco y coma profundo. Se han reportado fatalidades; sin embargo, los pacientes se han recuperado de niveles de valproato tan altos como 2120 mcg/mL. En situaciones de sobredosificación, la fracción de droga no unida a proteínas es alta y la hemodiálisis o hemodiálisis seguidas más hemoperfusión puede resultar en una significativa remoción de la droga. El beneficio del lavado gástrico o emesis puede variar con el tiempo desde la ingestión. Se deben aplicar medidas generales de soporte con especial atención al mantenimiento de un adecuado débito urinario. Se ha reportado que la naloxona revierte los efectos depresores del SNC de la sobredosificación con valproato. Dado que naloxona también puede, en teoría, revertir los efectos antiepilépticos de valproato, debe ser utilizado con cautela en pacientes con epilepsia.
Presentación.
Divalproato de Sodio ER de 250 mg está disponible como comprimidos blancos ovalados con la insignia corporativa y el logo Abbott-código HF. Cada comprimido de Divalproato de Sodio de liberación prolongada contiene Divalproato de Sodio equivalente a 250 mg de ácido valproico en Blister-Pack de 50. Divalproato de Sodio ER de 500 mg está disponible como comprimidos ovalados grises con la insignia corporativa y el Abbott-código HC. Cada comprimido de Divalproato de Sodio de liberación prolongada contiene Divalproato de Sodio equivalente a 500 mg de ácido valproico, en Blister-Pack de 50.

